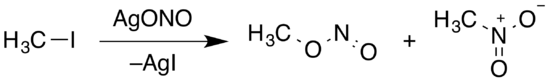Nitrite de méthyle
Le nitrite de méthyle est un composé organique, le plus simple de la famille des nitrites d'alkyle. C'est un gaz incolore particulièrement instable, toxique et inflammable.
| Nitrite de méthyle | |

| |
| Identification | |
|---|---|
| No CAS | |
| No ECHA | 100.009.882 |
| No CE | 210-870-5 |
| PubChem | 12231 |
| SMILES | |
| InChI | |
| Apparence | gaz incolore |
| Propriétés chimiques | |
| Formule | CH3NO2 [Isomères] |
| Masse molaire[1] | 61,04 ± 0,001 8 g/mol C 19,68 %, H 4,95 %, N 22,95 %, O 52,42 %, |
| Propriétés physiques | |
| T° fusion | −40,2 °C[2] |
| T° ébullition | −6,42 °C[2] |
| Solubilité | très peu soluble dans l'eau[2] |
| Masse volumique | 0,991 g·cm-3 à 15 °C[2] |
| Limites d’explosivité dans l’air | 5,3 Vol.-% (137 g·m-3) - 100 Vol.-%[2] |
| Pression de vapeur saturante | > 1 bar à 20 °C[2] |
| Précautions | |
| Directive 67/548/EEC | |
 T  F+ |
|
| Transport[2] | |
| Unités du SI et CNTP, sauf indication contraire. | |
Propriétés
A température ambiante, le nitrite de méthyle existe sous la forme d'un mélange de conformères cis et trans. La forme cis est plus stable de 3,13 kJ mol−1 que la forme trans, avec une barrière d'énergie de rotation de 45,3 kJ mol−1[3].
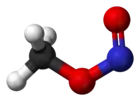 |  |
| cis-nitrite de méthyle | trans-nitrite de méthyle |
Le nitrite de méthyle est un agent oxydant et un explosif sensible à la chaleur ; cette sensibilité s'accroît en présence d'oxydes métalliques. Il explose plus violemment que le nitrite d'éthyle. Il forme des sels explosifs avec les bases inorganiques, ainsi que des mélanges explosifs avec l'air.
Le nitrite de méthyle est un gaz asphyxiant toxique, un puissant agent cyanotique. L'exposition peut entraîner une méthémoglobinémie[4].
Production et synthèse
Le nitrite de méthyle peut être préparé par réaction entre le nitrite d'argent et l'iodométhane. L'un des doublets libres de l'oxygène de l'ion nitrite va attaquer le groupe méthyle (—CH3), libérant de l'iode en solution[5]. Contrairement au nitrite d'argent, l'iodure d'argent est particulièrement insoluble dans l'eau, et forme donc un dépôt solide[6]. À noter cependant que l'azote du groupe nitrite est bien plus nucléophiles que l'oxygène, et donc la plupart des ions nitrites vont réagir par un méacanisme de type SN2 pour produire du nitrométhane. Par exemple, si on faisait réagir du nitrite de sodium ou du nitrite de potassium avec l'iodométhane, on obtiendrait quasiment uniquement du nitrométhane, et très peu de nitrite de méthane. L'utilisation de nitrite d'argent permet au contraire de stabiliser la formation d'un intermédiaire de type carbocation qui favorise la formation de nitrite de méthyle, faisant grimper le rendement, même si du nitrométhane est toujours produit[5].
Le nitrite de méthyle est aussi produit par la combustion de l'essence sans plomb, et pourrait être la cause du déclin d'insectes, ainsi que du moineau domestique et d'autre Passeri en Europe[7].
Utilisations
Du fait de ses propriétés explosives, le nitrite de méthyle est utilisé comme monergol[8].
C'est également un précurseur et un intermédiaire en synthèse organique. Il est par exemple utilisé durant la synthèse de la phénylpropanolamine[4], ou comme agent de méthylation par carbonylation oxydante[9].
Voir aussi
Notes et références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Entrée du numéro CAS « 624-91-9 » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 19 juillet 2010 (JavaScript nécessaire)
- (en) B.J. Van der Veken, R. Maas, G.A. Guirgis, H.D. Stidham, T.G. Sheehan, J.R. Durig, « Infrared spectrum, ab initio calculations, barriers to internal rotation and structural parameters for methyl nitrite », Journal of Physical Chemistry, vol. 94, no 10, , p. 4029–39 (DOI 10.1021/j100373a028)
- METHYL NITRITE – National Library of Medicine HSDB Database. Toxnet.nlm.nih.gov. Retrieved on 2019-03-10.
- Donald L. Pavia, Gary M. Lampman, George S. Kriz, Organic Chemistry, vol. 2, Mason, Ohio, Thompson Custom Publishing, (OCLC 236055357)
- (en) Darrell D. Ebbing et Steven D. Gammon, General Chemistry, Boston, Houghton Mifflin, , 8e éd., 1157 p. (ISBN 978-0-618-39941-3, LCCN 2003110172)
- J. Denis Summers-Smith, « Is unleaded petrol a factor in urban House Sparrow decline? », British Birds, vol. 100, , p. 558 (ISSN 0007-0335)
- Methyl Nitrite. Cameochemicals.noaa.gov
- X.-Z. Jiang, Palladium Supported Catalysts in CO + RONO Reactions, Platinum Metals Rev., 1990, 34, (4), 178–180
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Methyl nitrite » (voir la liste des auteurs).
- Portail de la chimie
- Portail de l’astronautique