زيرالينون
(Zearalenone (ZEN، المعروف أيضًا باسم RAL و F-2 السموم الفطرية ، هو مستقلب استروجين قوي ينتج عن بعض أنواع Fusarium و Gibberella . [1] على وجه الخصوص ، يتم إنتاجه بواسطة Fusarium graminearum و Fusarium culmorum و Fusarium cerealis و Fusarium equiseti و Fusarium verticillioides و Fusarium incarnatum .
| زيرالينون | |
|---|---|
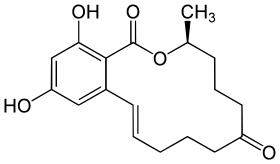 زيرالينون | |
| الاسم النظامي (IUPAC) | |
(3S,11E)-14,16-Dihydroxy-3-methyl-3,4,5,6,9,10-hexahydro-1H-2-benzoxacyclotetradecine-1,7(8H)-dione | |
| أسماء أخرى | |
Mycotoxin F2 | |
| المعرفات | |
| رقم CAS | 17924-92-4 |
| بوب كيم (PubChem) | 5281576 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| |
| الخواص | |
| صيغة كيميائية | C18H22O5 |
| كتلة مولية | 318.36 غ.مول−1 |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
تنتج الفيوزاريوم العديد من الأنواع من المواد السامة ذات أهمية كبيرة لمنتجي الماشية والدواجن، وهي ديوكسينيفالينول وتوكسين T-2 وتوكسين HT-2 و (diacetoxyscirpenol (DAS و زيرالينون. زيرالينون هو السم الأساسي الذي يسبب العقم أو الإجهاض أو مشاكل التكاثر الأخرى، خاصة في الخنازير.
زيرالينون مستقر للحرارة ويوجد في جميع أنحاء العالم في عدد من محاصيل الحبوب ، مثل الذرة والشعير والشوفان والقمح والأرز والذرة الرفيعة . [2] [3]
بالإضافة إلى أعمالها على الكلاسيكية في مستقبلات هرمون الاستروجين ، زيرالينون وجد ليكون بمثابة ناهض من GPER (GPR30). [4]
الخصائص الكيميائية والفيزيائية
زيرالينون مادة صلبة بلورية بيضاء. يعرض التألق الأزرق والأخضر عندما يكون متحمسًا بالضوء فوق البنفسجي ذي الطول الموجي الطويل (360 نانومتر) ووميض أخضر أكثر كثافة عند الإثارة بضوء الأشعة فوق البنفسجية قصير الموجة (260 نانومتر). في الميثانول ، تحدث أقصى درجات امتصاص الأشعة فوق البنفسجية عند 236 (e = 29700) ، و 274 (e = 13909) و 316 نانومتر (البريد = 6020). الحد الأقصى من التألق في الإيثانول يحدث مع التشعيع عند 314 نانومتر ومع انبعاث عند 450 نانومتر. الذوبان في الماء حوالي 0.002 جم / 100 مل. إنه قابل للذوبان بشكل طفيف في الهكسان وبشكل تدريجي أكثر في البنزين والأسيتونيتريل وكلوريد الميثيلين والميثانول والإيثانول والأسيتون . كما أنه قابل للذوبان في القلويات المائية.
يتحول أيزومر عبر (trans-zearalenone (trans-ZEN الذي يحدث بشكل طبيعي إلى الأشعة فوق البنفسجية إلى (cis -zearalenone (cis-ZEN. [5]
التعرض الجلدي
يمكن أن يتخلل زيرالينون عبر جلد الإنسان. [6] ومع ذلك ، لا يتوقع حدوث آثار هرمونية كبيرة بعد ملامسة الجلد في البيئات الزراعية أو السكنية العادية.
التكاثر
يشكل تعرض الإنسان والماشية لـ ZEN من خلال النظام الغذائي قلقًا صحيًا بسبب ظهور العديد من الاضطرابات الجنسية والتغيرات في تطور الجهاز الجنسي . [7] [8] هناك تقارير موثوقة عن حالات البلوغ المبكر في الفتيات المعرضات بشكل مزمن لـ ZEN في مناطق مختلفة من العالم. [9]
أخذ العينات والتحليل
كما هو الحال في السموم الفطرية الأخرى ، يجب أخذ عينات من السلع الغذائية من أجل زيرالينون للحصول على عينات ممثلة للشحنة قيد الاختبار. مذيبات الاستخلاص شائعة الاستخدام عبارة عن مخاليط مائية من الميثانول أو الأسيتونتريل أو أسيتات الإيثيل متبوعة بمجموعة من إجراءات التنظيف المختلفة التي تعتمد جزئيًا على الطعام وطريقة الكشف المستخدمة. تُستخدم طرق كروماتوغرافيا الطبقة الرقيقة (TLC) والكروماتوغرافيا السائلة عالية الأداء (HPLC) بشكل شائع. HPLC وحده غير كافٍ ، لأنه غالبًا ما يؤدي إلى نتائج إيجابية خاطئة. اليوم ، يتم استخدام تحليل HPLC- MS / MS لتحديد وتأكيد وجود زيرالينون.
طريقة TLC لـ زيرالينون هي: ألواح هلام السيليكا ذات الطور الطبيعي ، eluent: 90٪ ثنائي كلورو ميثان ، 10٪ v / v أسيتون أو عكس ألواح السيليكا C18 ؛ الشاطف: 90٪ حجم / حجم ميثانول ، 10٪ ماء. يعطي زيرالينون لمعانًا أزرقًا واضحًا تحت الأشعة فوق البنفسجية. [1]
انظر أيضًا
- α- زيرالينول
- β-Zearalenol
- تاليرانول
- زيرانول
- زيرالانون
المراجع
- "Zearalenone"، فيرمنتك (شركة)، مؤرشف من الأصل في 13 سبتمبر 2018.
- Kuiper-Goodman, T.؛ Scott, P. M.؛ Watanabe, H. (1987)، "Risk Assessment of the Mycotoxin Zearalenone"، Regulatory Toxicology and Pharmacology، 7 (3): 253–306، doi:10.1016/0273-2300(87)90037-7، PMID 2961013.
- Tanaka, T.؛ Hasegawa, A.؛ Yamamoto, S.؛ Lee, U. S.؛ Sugiura, Y.؛ Ueno, Y. (1988)، "Worldwide Contamination of Cereals by the Fusarium Mycotoxins Nivalenol, Deoxynivalenol, and Zearalenone. 1. Survey of 19 Countries"، American Chemical Society، 36 (5): 979–983، doi:10.1021/jf00083a019.
- Prossnitz, Eric R.؛ Barton, Matthias (2014)، "Estrogen biology: New insights into GPER function and clinical opportunities"، Molecular and Cellular Endocrinology، 389 (1–2): 71–83، doi:10.1016/j.mce.2014.02.002، ISSN 0303-7207، PMID 24530924.
- "UV-induced cis-trans isomerization of zearalenone in contaminated maize"، Mycotoxin Res، 29: 221، 2013، doi:10.1007/s12550-013-0178-7.
- Boonen, J.؛ Malysheva, S. V.؛ Taevernier, L.؛ Diana di Mavungu, J.؛ de Saeger, S.؛ de Spiegeleer, B. (2012)، "Human Skin Penetration of Selected Model Mycotoxins"، Toxicology، 301 (1–3): 21–32، doi:10.1016/j.tox.2012.06.012، PMID 22749975.
- Massart, F.؛ Saggese, G. (أبريل 2010)، "Oestrogenic mycotoxin exposures and precocious pubertal development"، International Journal of Andrology، 33 (2): 369–376، doi:10.1111/j.1365-2605.2009.01009.x، PMID 20002219.
- Schoevers, Eric J.؛ Santos, Regiane R.؛ Colenbrander, Ben؛ Fink-Gremmels, Johanna؛ Roelen, Bernard A.J. (أغسطس 2012)، "Transgenerational toxicity of Zearalenone in pigs"، Reproductive Toxicology، 34 (1): 110–119، doi:10.1016/j.reprotox.2012.03.004.
- Hueza, Isis؛ Raspantini, Paulo؛ Raspantini, Leonila؛ Latorre, Andreia؛ Górniak, Silvana (2014)، "Zearalenone, an Estrogenic Mycotoxin, Is an Immunotoxic Compound"، Toxins، 6 (3): 1080–1095، doi:10.3390/toxins6031080، ISSN 2072-6651، PMID 24632555.
روابط خارجية
- Eriksen, G. S.؛ Pennington, J.؛ Schlatter, J. (2000)، "Zearalenone"، WHO International Programme on Chemical Safety - Safety Evaluation of Certain Food Additives and Contaminants، Inchem، WHO Food Additives Series: 44، مؤرشف من الأصل في 20 أغسطس 2020.
- بوابة فطريات
- بوابة الكيمياء