فيروس إيبولا
فيروس إيبولا (EBOV) هو أحد خمسة أنواع معروفة لجنس فيروس إيبولا (genus Ebolavirus). أربعة من الخمسة أنواع المعروفة لفيروس إيبولا تسبب للبشر وغيرهم من الثديات حمى نزفية شديدة ومميتة تسمى مرض فيروس إيبولا (Ebola virus disease) (EVD).وهو سبب وباء فيروس إيبولا 2013-2015 في غرب أفريقيا، الأمر الذي أدى إلى ما لا يقل عن 28616 حالة مشتبه بها، و11310 حالة وفاة مؤكدة.
اضغط هنا للاطلاع على كيفية قراءة التصنيف فيروس إيبولا | |
|---|---|
 | |
| المرتبة التصنيفية | نوع |
| التصنيف العلمي | |
| فوق النطاق | حيويات |
| مملكة | فيروس |
| realm | ريبوفيريا |
| مملكة | Orthornavirae |
| شعبة | فيروسات رنا سالبة السلسلة |
| شعيبة | Haploviricotina |
| طائفة | Monjiviricetes |
| رتبة | فيروسات سلبية أحادية |
| فصيلة | فيروسات خيطية |
| جنس | Filovirus |
| الاسم العلمي | |
| Ebola virus[1] | |
وقد كان فيروس إيبولا يسمى «زائير» نسبة إلى دولة زائير (حالياً جمهورية الكونغو الديموقراطية) حيث تم تشخيص أول حالة، حيث تم تشخيصه على أنه سلالة جديدة من فيروس ماربورغ (Marburg virus) نظراً للارتباط الوثيق بينهم. وتمت إعادة تسميته إلى فيروس إيبولا عام 2010 لتجنب الالتباس. فيروس إيبولا هو أحد أنواع ebolavirus الزائيري، وهو أحد أنواع جنس Ebolavirus وهي عائلة فيروسات خيطية.[2][3] وتعتبر الخفافيش، وخصوصاً خفافيش الفاكهة، المضيف الطبيعي لفيروس إيبولا، وينتقل الفيروس بين البشر والحيوانات عن طريق السوائل الجسدية.[4][5]
ويعرف جينوم فيروس إيبولا على أنه RNA ذو سلسلة واحدة بطول 19000 نيوكليوتيدة تقريباً. ويتضمن سبعة بروتينات بنائية: نيوكليوبروتين (NP) والعامل المساعد للبوليمريز (VP35), و (VP40), و GP, ومنشط النسخ (VP30), و VP24، والرنا بوليمريز.[6]
وبسبب معدل الوفيات المرتفع لفيروس إيبولا (83-90%),[7][8] يصنف فيروس إيبولا على أنه عامل انتقائي، وصنف من ضمن مجموعة الأمراض الخطرة (الدرجة الرابعة) من منظمة الصحة العالمية، وتصنفه منظمة الصحة ومنظمة الحساسية والأمراض المعدية الأمريكية بتصنيف مرض معدي ذو أولوية قصوى، وتصنفه مراكز مكافحة الأمراض الأمريكية على أنه عامل من عوامل الإرهاب الحيوي، كما أنه يعتبر عامل حيوي لرقابة الصادرات الأسترالية.
التركيب
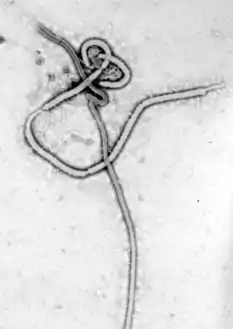
يحمل فيروس الإبولا جين RNA السلبي في فيرون أسطواني ويحتوي على غلاف فيروسي ونيوكليدات كبسولية. والشكل الاسطواني يكون بقطر 80 nm ويحتوي على بروتين سكري فيروسي الشفرة على شكل اشواك بطول 7-10 nm من طبقه الدهون الثنائية. وطول الشكل الاسطواني يكون متغير، عادة يكون 800 nm ولكن يصل أحيانا إلى 1000 nm. الطبقة الخارجية للغلاف الفيروسي يستمد شكلها من خلايا المضيف بحيث يستطيع غرس أشواكه فيها بحيث تكون المسافة بين الاشواك حوالي 10 nm. وتتواجد البروتينات الفيروسية VP40 و VP24 بين الغلاف والنيوكلوسايد في المساحة المطرسية.[9] وفي وسط تركيبه الفيرون يكمن قفيصة منواة (نيوكليوكابسد) المتكون من سلسله من البروتينات الفيروسية متصلة في 18–19 kb بشكل خطي، و RNA سلبي بدون 3-تذييل بعديد الأدينيلات أو بدون 5- غطاء بروتيني. الـRNA الحلزوني والمختلط مع بروتينات NP,VP35,VP30,L. هذا الشكل الحلزوني قطره يساوي 80 nm ويحتوي على قناه وسطيه بقطر 20-30 nm .[10]
الشكل العام للفيريون يتنوع بشكل ملاحظ بعد التنقية (بالتنبيذ الفائق) والتصور (بالمجهر الإلكتروني)، بحيث أن الإسطوانة البسيطة تكون أقل ظهوراً بالإتجاه المعاكس، الجذور والحلقات. ولكن تفاصيل هيكل «المشابه للخيط» له صفات عامة لفيروسات الفيلو.[11]
الجينوم
كل فيرون يحتوي على جزيء خطيّ ذو سلسلة واحده من الـرنا السلبي، ويحتوي على نيوكليوتيدات تمتد في الطول ما بين 18959 إلى 18961، ونهاية الفيرون من الرقم 3 ليست مذيله بعديد الأدينيلات، والنهاية رقم 5 ليست مغطاة.[12] الكود الخاص بهذا الجينوم الفيروسي ينطبق على سبعة تراكيب بروتينية وبروتين واحد غير تركيبي. ترتيب الجين هو 3′ – leader – NP – VP35 – VP40 – GP/sGP – VP30 – VP24 – L – trailer – 5′ يعتبر leader و trailer منطقتين غير منسوختين لذا تقوم بنقل إشارات مهمة للسيطرة على الأستنساخ وعملية التضاعف وتحميل جينومات فيروسية إلى فيرونات جديدة. المنطقة من NP,VP35 والجين L في الفايلوفايروس تم تشخيصها على أنها باطنية النمو في الجينوم في المجموعات الصغيرة من الثدييات. [13][14][15]
تم اكتشاف أن النهاية من 3 يوجد بها 472 من النيوكليوتيدات والنهاية 5 يوجد بها 731 , وهي ضرورية لعملية تضاعف الفيروس الجيني المصغر، ولكنها غير مهمة في العدوى[11] المواد التركيبية الجينيه للجينوم المصغر بطبيعتها غير معدية، لأن البروتينات الفيروسية متواجد بداخلهم RNA بوليماريز، مهم لنسخ الفايروس الجيني بداخل mRNA لأن RNA السلبي الفيروسي وينطبق ذلك على التضاعف في الجينوم الفيروسي.
التسلسل الفيروسي لثمانية وسبعين مريض تم التأكد من إصابتهم بفيروس إيبولا ويمثلون ما يقارب 70% من حالات التشخيص في سيراليون من أواخر شهر ماي إلى منتصف شهر جون من 2014 , أدلة موثوقة أن التضخم للفيروس في 2014 لم يعد بسبب انتقال الفيروس في المضيف الطبيعي له، مثل أي RNA فايروس، الفيروس تحول بشكل سريع من خلال المجمتعات البشرية ومن خلال المضيف داخل المجتمعات. نسبة التحول تقدر بما يقارب 2.0 x 10−3 تحول كل موقع كل سنة وبسرعة تقدر بانتشار الفيروس.[16] ومن المحتمل أن يمثل اختيار انتقائي سريع يعجل بالانتقال بين البشر، ومن المحتمل أن يطرح مقاومة التطعيمات.[17][18] [19][20]
الدخول
هناك موقعان مرشحان للدخول على الخلايا المضيفة. الأول هو البروتين الناقل للكولسترول وترميز المضيف له هو Niemann-pick C1 [الإنجليزية]. والذي اتضح انه ضروري لدخول فيروس ابولا إلى خليه المضيف والتضاعف.[21][22] في دراسة للفئران تحمل نسخه من جين NPC1 ازيلت أظهرت 80% فرصه نجاة بعد 15 يوم من التعرض لفيروس ابولا.[23] بينما 10% من الفئران الغير معدله نجت لهذه المدة.
وفي دراسة أخرى، أظهرت بعض الجزيئات الصغيرة أنها منعت عدوى فيروس الإيبولا عن طريق حجز غلاف البروتين السكري الفيروسي من الارتباط مع NPC1 الذي ظهر انه ضروري لدخول الفيروس.
تعرضت خلايا مرضى نيمان بيك سي التي تفتقر لهذا الناقل لفيروس ابولا في المختبر، نجت الخلايا وأظهرت أنها غير قابلة للإصابة بهذا الفيروس. التحولات الجينية في NPC1 في البشر هي الطريقة محتمله التي جعلت من هؤلاء الافراد مقاومين لهذا الفيروس. نفس الدراسات أظهرت نتائج مماثله بخصوص دور NPC1 في دخول فيروس ماربورغ، الذي من نفس عائلة فيروس إيبولا.[24]
أما المرشح الثاني فهو TIM-1 (المعروف أيضاً بـ HAVCR1). حيث أظهر بأنه يرتبط مع غلاف البروتين السكري الفيروسي لزيادة قابلية الارتباط للخلايا الفيروسية. بتثبيط فعاليته بواسطة siRNA فسوف يمنع عدوى الفيروس.
اقترحت هذه الدراسات السابقة أن NPC1 و TIM-1 من الممكن ان يكونا طريقة لعلاج فيروس إيبولا.
عملية التضاعف
بما أن الفايروس غير خلوي، فهو لا ينتقل عن طريق الأنقسام الخلوي، بل يتم عن طريق مزيج من إنزيمات المضيف وإنزيمات الفيروس بالإضافة إلى الخلية المضيفة. تنتج العديد من نسخات الفيروس لتتجمع تلقائياً لتكون جزيئات فيروسية كبيرة في داخل الخلية المضيفة.
ثم يبدأ الفيروس بالمهاجمة بالتعلق بمستقبلات الخلية عبر البروتين السكري السطحي «بيبلومير», ثم يلتهم بواسطة الماكروبينوسومز إلى الخلية المضيفة. ثم يجب على الغشاء الفيروسي أن يندمج مع الغشاء الحويصلي للخلية للدخول. ثم يتم استخدام ssRNA السلبي كقالب ليتم صناعة العديد من النسخ البروتينية الفيروسية.
ثم نذير بروتين سكري من هذه البروتينات الفيروسية (GP0) ينقسم إلى (GP1) و (GP2) يرتبط بالغليكوزيل باستعمال إنزيمات خلوية. يجتمع هذان الجزيئات اولاً كمثنوي مغايز، ثم كمثولث حتى يصبح سطحه قسيم فولفي.
علم البيئة
فيروس إيبولا هو مرض حيواني المنشأ. وقيل أن المضيف المتوسط هو «أجناس مختلفة من خفافيش الفاكهة.. حول وسط وجنوب الصحراء الأفريقية». وجد دليل لعدوى الخفافيش عبر الاختبارات الجزيئية والسيرولوجية. لكن لم يتم استئصال الفيروس من الخفافيش.[25]
الإنسان والقردة هما المضيفين النهائيين، وتتم الإصابة بينهما أو بين الخفافيش. وجد أن الخنازير في الفلبين
مرض فيروس إيبولا
يعتبر فيروس إيبولا أحد أربعة أنواع من جنس (ebolaviruses) التي تسبب الأمراض للبشر، بمعدل وفيات الأعلى من بين الأربع أنواع 83% منذ أول اندلاع عام 1976, بالرغم من أنه تم تسجيل معدلات تصل إلى 90% في اندلاع 2002. حدث أول اندلاع للمرض 26 أغسطس عام 1976 في قرية يومبكو في الكونغو[26][25][25][32]. سجلت أول قضية لمدرس ابتدائي اسمه مابالو لوكيلا (44 عام). كانت الأعراض تشابه الملاريا، وتلقوا المرضى المشابهين الكينين. وينسب تفشي المرض إلى إعادة استخدام الإبر غير المعقمة والاتصال الشخصي القريب والسوائل الجسدية وكذلك بلمس الأماكن التي لمسها المصاب.
خلال اندلاع 1976 في زائير، سجل إنغوي موشولا أول تشخيص للمرض عندما كان يسافر من بومبا إلى يومبكو، حيث سجل فيها وصف عن الحالات المرضية في سجلاته اليومية.[27]
«يتصف المرض بأعراض منها ارتفاع في درجة الحرارة يصل إلى 39 درجة مئوية، وقيء الدم، وإسهال مع دم، وألم في البطن خلف القص، وإعياء مع شعور بثقل في المفاصل، وتداعيات سريعة تنتهي بالموت خلال مدة ثلاثة أيام».
منذ الاندلاعة الأولى 1976 في زائير، كانت اندلاعة مارس 2014 هي الأخطر حيث وصلت إلى مقاييس وبائية بتعداد ضحايا يصل إلى 8000 ضحية حتى يناير 2015, تمركزت هذه الاندلاعة في غرب أفريقيا حيث لم يسبق أن انتشر فيها المرض قبلها. أكثر الدول ضحايا هي ليبيريا وغينيا وسييرا ليون. وظهرت عدة حالات خارج حدود غرب أفريقيا نتيجة للسياح الذين تعرضوا للعدوى خلال سفرهم في دول غرب أفريقيا.[28]
حدة المرض في البشر تختلف بمختلف الحالات، من موت مباشر إلى ردة فعل عرضية أو حتى بلا أعراض.[29] وفشلت الدراسات في آخر القرن العشرين في إيجاد ارتباط بين حدة المرض والتركيب الجيني للفيروس، وبهذا استنتج الدارسون أن اختلاف حدة المرض يعود إلى الاختلافات الجينية بين الضحايا. وكانت صعوبة الدراسات تكمن في إيجاد عينات اختبار يكون لها ردة فعل للفيروس مماثلة لردة فعل البشر.[30] وفي أواخر أكتوبر 2014 نشرت دراسة تفيد استجابة بعض الفئران المعدلة لفيروس إيبولا الزائيري، وأفادت الدراسات أن التنوع الوراثي هو سبب اختلاف حدة المرض. ويتوقع أن تحدد الدراسات المستقبلية الجينات المسؤولة عن ردة الفعل للفيروس وبالتالي علاجه.
التاريخ والتسمية
فيروس إيبولا تم تشخصية في البداية على أنه سلالة جديدة من فيروس ماربورغ في عام 1976. وفي الوقت نفسه، فريق جديد قدم الفيروس بمسمى «فايروس إيبولا» المشتق من نهر إيبولا عندما إنتشر في عام 1976.[31][32][33] اللجنة الدولية لتصنيف الفيروسات قامت بتصنيف الفيروس على أنه من صنف زائير فيروس إيبولا، الذي ينضم إلى جنس فيروس إيبولا، عائلة الفيروسات الخيطية، رتبة الفيروسات السلبية الأحادية.
نهر الايبولا والذي أشتق منه أسم الفيروس أعتقد أنه قريب من منطقة في جمهورية الكونغو (كانت تسمى زائير) والتي حدث فيها انتشار الإيبولا. [34]
في عام 2000 تم تغيير اسم الفيروس إلى فيروس زائير إيبولا،[35][36] وفي عام 2002 تم تغييره مجدداً إلى صنف فيروس زائير إيبولا،[37][38] ومع ذلك كثير من العلماء استمروا بتسمية الفايروس بفايروس إيبولا وبعضهم بفايروس زائير إيبولا. وبناءً على ذلك، في 2010, مجموعة من الباحثين أقترحوا تسمية الفيروس بإيبولا ويعتبر تصنيف فرعي من فيروس زائير إيبولا ومع استخدام الاختصار (EBOV), الاختصارات السابقة كانت (EBOV-Z) و (ZEBOV). وفي عام 2011, منظمة ICTV رفضت هذا الاقتراح لأن هذه المنظمة لا تقبل الأسامي للأنواع والسلالات والفروع.[39] وحتى الآن، منظمة ICTV ما زالت لا تعترف بفيروس إيبولا في سلم التصنيف وما زالت تعتمد الاسم القديم فيروس إيبولا زائير.
نموذج الفيروس المسمى بماينجا تمت تسميته اشتقاقاً عن ماينجا نيسكا ممرضة توفت في عام 1976 خلال انتشار الفايروس.[40][41][42]
اللقاح
الكثير من لقاحات ابولا المحتملة طورت في العقد الماضي ولكن الآن لم يتم الموافقة عليها من قبل منظمة الدواء والغذاء الأمريكية (FDA) للاستخدام البشري قبل 2014. أظهرت لقاحات إيبولا انها لا تعزز المناعة ضد الفيروس. ولكن هناك العديد من اللقاحات الواعدة التي تحفز الوحدات الفيروسية أظهرت انها تحمي المقدمات غير البشرية من العدوى المميتة.[43][44][45] وهذه تضم ناقلات الفيروسات الغدانية الغير قابلة للتكاثر، وناقلات فيروس التهاب الفم الحويصلي القابلة للتكاثر، وناقلات فيروس نظير الإنفلونزا.[46][47] وتشمل المرحلة الأولى من التجارب السريرية على إعطاء اللقاح لمواضيع البشرية السليمة لتقييم الاستجابة المناعية تحديد أي آثار جانبية، وتحديد الجرعة المناسبة.[48][49] نشرت نتائج في غينيا في شهر يوليو 2015 للقاح فيروس إيبولا المشتق من (ناقلات فيروس التهاب الفم الحويصلي) التي أظهرت نتائج مبشرة.
معايير إدراج الفيروس
أي فيروس من صنف فيروس زائير إيبولا هو فيروس إيبولا إذا كان لديه خصائص فيروس زائير إيبولا ويتشعب جينومه من النموذج المبدئي لفيروس إيبولا بنسبة 10% أو أقل على المستوى النيوكليوتيدي.
مراجع
- العنوان : ICTV Master Species List 1987
- Kuhn, Jens H.; Becker, Stephan; Ebihara, Hideki; Geisbert, Thomas W.; Johnson, Karl M.; Kawaoka, Yoshihiro; Lipkin, W. Ian; Negredo, Ana I et al. (2010).
- WHO.
- Angier, Natalie (October 27, 2014).
- Quammen, David (2014-12-30).
- Nanbo, Asuka; Watanabe, Shinji; Halfmann, Peter; Kawaoka, Yoshihiro (4 Feb 2013).
- "Ebola virus disease Fact sheet N°103". نسخة محفوظة 10 ديسمبر 2017 على موقع واي باك مشين.
- C.M. Fauquet (2005).
- Feldmann, H. K. (1993).
- Biomarker Database.
- Klenk, H-D; Feldmann, H (editor) (2004)، Ebola and Marburg Viruses: Molecular and Cellular Biology، Horizon Bioscience، ISBN 978-1-904933-49-6.
{{استشهاد بكتاب}}:|مؤلف=has generic name (مساعدة)صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Zaire ebolavirus isolate H.sapiens-wt/GIN/2014/Makona-Kissidougou-C15, complete genome, GenBank نسخة محفوظة 24 يناير 2018 على موقع واي باك مشين.
- Taylor, D.; Leach, R.; Bruenn, J. (2010).
- Belyi, V. A.; Levine, A. J.; Skalka, A. M. (2010).
- Taylor, D. J.; Ballinger, M. J.; Zhan, J. J.; Hanzly, L. E.; Bruenn, J. A. (2014).
- Jenkins, G. M.; Rambaut, A; Pybus, O. G.; Holmes, E. C. (2002).
- Richard Preston (27 October 2014).
- Stephen K. Gire with 57 others (2014).
- Tracking a Serial Killer: Could Ebola Mutate to Become More Deadly? نسخة محفوظة 08 يناير 2018 على موقع واي باك مشين.
- Ebola 2014 is Mutating as Fast as Seasonal Flu. نسخة محفوظة 09 سبتمبر 2016 على موقع واي باك مشين.
- Carette JE, Raaben M, Wong AC, Herbert AS, Obernosterer G, Mulherkar N, Kuehne AI, Kranzusch PJ, Griffin AM, Ruthel G, Dal Cin P, Dye JM, Whelan SP, Chandran K, Brummelkamp TR; Raaben; Wong; Herbert; Obernosterer; Mulherkar; Kuehne; Kranzusch; Griffin; Ruthel; Dal Cin; Dye; Whelan; Chandran; Brummelkamp (September 2011).
- Côté M, Misasi J, Ren T, Bruchez A, Lee K, Filone CM, Hensley L, Li Q, Ory D, Chandran K, Cunningham J; Misasi; Ren; Bruchez; Lee; Filone; Hensley; Li; Ory; Chandran; Cunningham (September 2011).
- Flemming A (October 2011).
- Miller EH, Obernosterer G, Raaben M, Herbert AS, Deffieu MS, Krishnan A, Ndungo E, Sandesara RG, Carette JE, Kuehne AI, Ruthel G, Pfeffer SR, Dye JM, Whelan SP, Brummelkamp TR, Chandran K; Obernosterer; Raaben; Herbert; Deffieu; Krishnan; Ndungo; Sandesara; Carette; Kuehne; Ruthel; Pfeffer; Dye; Whelan; Brummelkamp; Chandran (March 2012).
- Feldmann H (May 2014).
- Isaacson, M; Sureau, P; Courteille, G; Pattyn, SR;.
- Bardi, Jason Socrates.
- name: S. Reardan.; N,Engl.
- Gina Kolata (Oct 30, 2014).
- Angela L. Rasmussen with 21 others (Oct 30, 2014).
- Pattyn, S.; Jacob, W.; van der Groen, G.; Piot, P.; Courteille, G. (1977).
- Bowen, E. T. W.; Lloyd, G.; Harris, W. J.; Platt, G. S.; Baskerville, A.; Vella, E. E. (1977).
- Johnson, K. M.; Webb, P. A.; Lange, J. V.; Murphy, F. A. (1977).
- Kuhn, Jens H.؛ Becker, Stephan؛ Ebihara, Hideki؛ Geisbert, Thomas W.؛ Johnson, Karl M.؛ Kawaoka, Yoshihiro؛ Lipkin, W. Ian؛ Negredo, Ana I؛ وآخرون (2010)، "Proposal for a revised taxonomy of the family Filoviridae: Classification, names of taxa and viruses, and virus abbreviations"، Archives of Virology، 155 (12): 2083–103، doi:10.1007/s00705-010-0814-x، PMC 3074192، PMID 21046175.
- Netesov, S. V.; Feldmann, H.; Jahrling, P. B.; Klenk, H. D.; Sanchez, A. (2000).
- Pringle, C. R. (1998).
- Feldmann, H.; Geisbert, T. W.; Jahrling, P. B.; Klenk, H.-D.; Netesov, S. V.; Peters, C. J.; Sanchez, A.; Swanepoel, R.; Volchkov, V. E. (2005).
- Mayo, M. A. (2002).
- "Replace the species name Lake Victoria marburgvirus with Marburg marburgvirus in the genus Marburgvirus". نسخة محفوظة 05 مارس 2016 على موقع واي باك مشين.
- Kuhn, Jens H.؛ Becker, Stephan؛ Ebihara, Hideki؛ Geisbert, Thomas W.؛ Johnson, Karl M.؛ Kawaoka, Yoshihiro؛ Lipkin, W. Ian؛ Negredo, Ana I؛ وآخرون (2010)، "Proposal for a revised taxonomy of the family Filoviridae: Classification, names of taxa and viruses, and virus abbreviations"، Archives of Virology، 155 (12): 2083–103، doi:10.1007/s00705-010-0814-x، PMC 3074192، PMID 21046175.
- Wahl-Jensen, V.; Kurz, S. K.; Hazelton, P. R.; Schnittler, H.-J.; Stroher, U.; Burton, D. R.; Feldmann, H. (2005).
- Kesel, A. J.; Huang, Z; Murray, M. G.; Prichard, M. N.; Caboni, L; Nevin, D. K.; Fayne, D; Lloyd, D. G.; Detorio, M. A.; Schinazi, R. F. (2014).
- "Statement on the WHO Consultation on potential Ebola therapies and vaccines". نسخة محفوظة 03 نوفمبر 2017 على موقع واي باك مشين.
- "2014 Ebola Outbreak in West Africa"[وصلة مكسورة].
- Alison P. Galvani with three others (21 August 2014).
- Hoenen T, Groseth A, Falzarano D, Feldmann H (May 2006).
- Hugues Fausther-Bovendo with two others (2012).
- James Gallagher (31 July 2015).
- Henao-Restrepo, Ana Maria et al. (31 July 2015).
- بوابة طب
- بوابة علم الفيروسات