يوديد البيريليوم
يوديد البيريليوم مركب كيميائي له الصيغة BeI2، ويكون على شكل بلورات إبرية عديمة اللون.
| يوديد البيريليوم | |
|---|---|
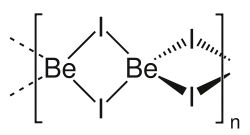 يوديد البيريليوم | |
| الاسم النظامي (IUPAC) | |
Beryllium iodide | |
| المعرفات | |
| رقم CAS | 7787-53-3 |
| بوب كيم (PubChem) | 82231 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | BeI2 |
| الكتلة المولية | 262.82 غ/مول |
| المظهر | بلورات إبرية عديمة اللون |
| الكثافة | 4.32 غ/سم3 |
| نقطة الانصهار | 510 °س |
| نقطة الغليان | 590 °س |
| الذوبانية في الماء | يتفاعل بعنف مع الماء |
| الذوبانية | ينحل في الإيثانول وثنائي إيثيل الإيثر |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
التحضير
يمكن تحضير يوديد البيريليوم من تفاعل فلز البيريليوم مع اليود عند درجات حرارة تتراوح بين 500 إلى 700 °س: [2][3]
كما يتشكل يوديد البيريليوم عندما يتفاعل كربيد البيريليوم مع يوديد الهيدروجين في الطور الغازي فقط عند درجات حرارة تتراوح بين 600-700 °س:[3]
الخواص
إن مركب يوديد البيريليوم ساحب للرطوبة، وهو يتفاعل بعنف مع الماء، حيث يتحرر يوديد الهيدروجين.[2]
من السهل استبدال اليود في يوديد البيريليوم بهالوجينات أخرى؛ إذا تفاعل مع الفلور أعطى فلوريد البيريليوم وفلوريدات اليود، ومع الكلور يعطي كلوريد البيريليوم، ومع البروم يعطي بروميد البيريليوم.
يتفاعل يوديد البيريليوم بعنف مع العوامل المؤكسدة مثل فوق منغنات البوتاسيوم أو كلورات البوتاسيوم ليعطي بخاراً بنفسجياً (أرجواني) من اليود.[4]
يوجد يوديد البيريليوم في الحالة الغازية على شكل ثنائي وحدات، وعند درجة حرارة تبلغ 1200 °س يتفكك بخار BeI2 إلى العناصر الأولية البيريليوم واليود.[3] تبلغ
توجد ثلاثة أشكال بلورية من يوديد البيريليوم وذلك حسب مجال درجة الحرارة.[3]
البنى البلورية لمركب يوديد البيريليوم وأبعاد الشبكة البلورية بالأنغستروم Å
| مجال درجة الحرارة | النظام البلوري | a | b | c | β |
|---|---|---|---|---|---|
| إلى 290 °س | نظام بلوري معيني قائم | 11.18 | 5.94 | 6.04 | - |
| 290 °س إلى 370 °س | نظام بلوري معيني قائم | 18.0 | 16.69 | 11.43 | - |
| فوق 370 °س | نظام بلوري رباعي | 5.84 | 5.70 | - | - |
احتياطات الأمان
إن البيريليوم ومركباته الكيميائية هي مواد سامّة ومسرطنة، حيث يمكن أن تسبب مرض التسمم بالبيريليوم. لذا ينبغي أخذ الحيطة والحذر عند التعامل مع هذه المركبات.
المراجع
- العنوان : Beryllium diiodide — مُعرِّف "بَب كِيم" (PubChem CID): https://pubchem.ncbi.nlm.nih.gov/compound/5463524 — تاريخ الاطلاع: 14 أكتوبر 2016 — الرخصة: محتوى حر
- Perry, Dale؛ Phillips, Sidney (1995)، Handbook of inorganic compounds، CRC Press، ص. 63، ISBN 978-0-8493-8671-8
- Walsh, Kenneth (2009)، Beryllium chemistry and Processing، ASM International، ص. 118
- Parsons (1909)، The Chemistry and Literature of Beryllium، مؤرشف من الأصل في 5 مارس 2017
- بوابة الكيمياء