Oxácido
Un oxácido es un ácido que contiene oxígeno. Específicamente, es un compuesto que contiene hidrógeno, oxígeno y al menos otro elemento, con al menos un átomo de hidrógeno unido al oxígeno que puede disociarse para producir el catión H+ y el anión del ácido.[1] Esto quiere decir que son compuestos ternarios (formados por tres tipos de átomos), y que siempre mantienen el mismo orden (Hidrógeno, 1 no metal y oxígeno). También podemos decir que se forman por reacción de un óxido no metálico y agua.
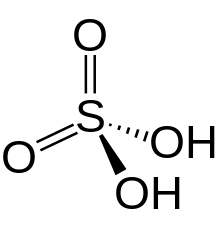
Su fórmula responde al patrón HaAbOc, donde A es un no metal o metal de transición.
Ejemplos de oxácidos:[2][3][4][5]
- Ácido sulfúrico (H2SO4). Formado por la reacción de síntesis de una molécula de H2O con una molécula de óxido de azufre SO3:
- SO3 + H2O → H2SO4
- Ácido sulfuroso (H2SO3). Formado por la reacción de síntesis de una molécula de H2O con una molécula de óxido sulfuroso SO2:
- SO2 + H2O → H2SO3
- Ácido hiposulfuroso (H2SO2). Formado por la reacción de síntesis de una molécula de H2O con una molécula de óxido hiposulfuroso SO:
- SO + H2O → H2SO2
Escritura de un oxácido
Primero va el Hidrógeno, en el medio el no metal y por último el Oxígeno. (Ej: H S O )
con el número de oxidación del no metal siendo par
- Si el número de oxidación del no metal es par, al Hidrógeno le corresponde el subíndice 2.
- Se suma el número de oxidación del no metal con el 2 del Hidrógeno y se divide por el número de oxidación del Oxígeno, que es -2, y el resultado es el subíndice del Oxígeno.
+4 -2
Ej: H2 S O3
(4+2): 2=3 queda H2SO3
con el número de oxidación del no metal siendo impar
- Si el número de oxidación del no metal es impar, al Hidrógeno le corresponde el subíndice 1.( cuando el no metal es el fósforo, el subíndice es 3)
- Se suma el número de oxidación del no metal con el 1 del Hidrógeno y se divide por el número de oxidación del Oxígeno, que es -2, y el resultado es el subíndice del Oxígeno.
+3 -2
Ej: H1 N O2
1(+1)+ (+3)= 2 (-2), cargas positivas y negativas igualadas
(3+1): 2=2 queda HNO2
Clasificación
Nota: La nomenclatura usada en este artículo para nombrar los compuestos ha sido la tradicional. Los oxácidos son ácidos formados por hidrógeno (H), un elemento no-metálico (X) y oxígeno (O). Dependiendo del número de oxidación, un óxido covalente con agua forma un ácido u otro. Por ejemplo, el anhídrido nítrico (N2O5) formará el ácido nítrico (HNO3) cuando se combina con agua: N2O5 + H2O → H2N2O6 → 2HNO3 Cada ácido, al perder su(s) hidrógeno(s) produce su(s) respectivo(s) anión(es) con tantas cargas negativas como hidrógenos haya perdido. Dependiendo del número de H que tengan se dividen en 4 grupos. A continuación se han clasificado los ácidos dependiendo del número de H y ejemplos:
Grupo de Cloro, Bromo, Yodo, Cianógeno
Los tres últimos deben llevar el prefijo meta-.
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| HXO | Ácido (meta)hipo...oso | XO- | (Meta)Hipo...ito. |
| HXO2 | Ácido (meta)...oso | XO2- | (Meta)...ito. |
| HXO3 | Ácido (meta)...ico | XO3- | (Meta)...ato. |
| HXO4 | Ácido (meta)per....ico | XO4- | (Meta)Per....ato. |
| Ejemplos concretos | |||
| HIO | Ácido hipoyodoso | IO- | Hipoyodito |
| HIO2 | Ácido yodoso | IO2- | Yodito |
| HIO3 | Ácido yódico | IO3- | Yodato |
| HIO4 | Ácido peryódico | IO4- | Peryodato |
Grupo de Azufre, Selenio y Teluro
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| H2XO2 | Ácido hipo...oso | XO22- | Hipo...ito |
| H2XO3 | Ácido ...oso | XO32- | ...ito |
| H2XO4 | Ácido ...ico | XO42- | ...ato |
| Ejemplos concretos | |||
| H2SO2 | Ácido hiposulfuroso | SO22- | Hiposulfito |
| H2SeO3 | Ácido selenioso | SeO32- | Selenito |
| H2SO4 | Ácido sulfúrico | SO42- | Sulfato |
| H2TeO4 | Ácido telúrico | TeO42- | Telurato |
Grupo de Nitrógeno, Fósforo, Arsénico y Antimonio
También se pueden nombrar con el prefijo orto-.
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| H3XO2 | Ácido (orto)hipo...oso | XO23- | (Orto)Hipo...ito |
| H3XO3 | Ácido (orto)...oso | XO33- | (Orto)...ito |
| H3XO4 | Ácido (orto)...ico | XO43- | (Orto)...ato |
| Ejemplos concretos | |||
| H3SbO2 | Ácido (orto)hipoantimonioso | SbO23- | (Orto)Hipoantimonito |
| H3AsO3 | Ácido (orto)arsenioso | AsO33- | (Orto)Arsenito |
| H3PO4 | Ácido (orto)fosfórico. | PO43- | (Orto)Fosfato |
Grupo de Fósforo, Arsénico y Antimonio
Deben llevar el prefijo piro- o di-.
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| H4X2O3 | Ácido dihipo...oso o pirohipo...oso | X2O34- | Dihipo...ito o p |
| H4X2O7 | Ácido di...ico o piro...ico | X2O74- | Di...ato o piro...ato |
| Ejemplos concretos | |||
| H4Sb2O5 | Ácido dihipoantimonioso o piroantimonioso | Sb2O34- | Dihipoantimonito o piroantimonito |
| H4As2O5 | Ácido diarsenioso o piroarsenioso | As2O54- | Diarsenito o piroarsenito |
| H4P2O7 | Ácido difosfórico o pirofosfórico | P2O74- | Difosfato o pirofosfato |
Además, según la nomenclatura tradicional, los números de oxidación, la estructura de los compuestos y demás factores, hay ácidos más especiales como el tiociánico (HSCN) que aparentemente no se parecen a los citados anteriormente:
Con Boro
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| HBO2 | Ácido metabórico | BO2- | Metaborato. |
| H3BO3 | Ácido (orto)bórico | BO33- | (Orto)Borato |
Con Silicio
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| H2SiO3 | Ácido metasilícico | SiO32- | (Meta)Silicato. |
| H4SiO4 | Ácido (orto) silícico | SiO44- | (Orto) silicato |
Con Azufre
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| H2S2O7 | Ácido disulfúrico o pirosulfúrico | S2O72- | Disulfato o pirosulfato. |
| H2S2O8 | Ácido peroxodisulfúrico o peroxopirosulfúrico | S2O82- | Peroxodisulfato o peroxopirosulfato |
| H2SO5 | Ácido peroxosulfúrico | SO52- | Peroxosulfato |
| H2S2O3 | Ácido tiosulfúrico | S2O32- | Tiosulfato |
Con Carbono
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| H2CO2 | Ácido carbonoso | CO22- | Carbonito |
| H2CO3 | Ácido carbónico | CO32- | Carbonato |
Con Manganeso
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| H2MnO4 | Ácido mangánico | MnO42- | Manganato |
| HMnO4 | Ácido permangánico | MnO4- | Permanganato |
Con Cromo
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| H2CrO4 | Ácido crómico | CrO42- | Cromato |
| H2Cr2O7 | Ácido dicrómico | Cr2O72- | Dicromato |
Con Carbono y Nitrógeno
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| HOCN | Ácido ciánico | OCN- | Cianato |
| HSCN | Ácido tiociánico | SCN- | Tiocianato |
Otros
Otro compuesto importante es el Ácido acético o etanoico CH3-COOH (C2H4O2), con el acetato o etanoato CH3-COO- ([C2H3O2]−)
Como hemos visto, los oxácidos tienen aniones que se forman al perder todos los hidrógenos que tenían pero también pueden perder solo 2 o solo 3. Por ejemplo el ácido sulfúrico (H2SO4) puede perder sus 2 o solo 1 hidrógeno, si pierde los 2 el anión se llamará sulfato (SO42-) pero si solo pierde 1 se llamará hidrogenosulfato (HSO4-) que es un anión ácido. El Ácido difosfórico (H4P2O7) puede perder los 4: difosfato (P2O74-), 3: hidrogenodifosfato (HP2O73-), 2: dihidrogenodifosfato (H2P2O72-), 1: trihidrogenodifosfato (H3P2O7-).
Sales ternarias
Las sales ternarias no son más que la combinación de un anión o anión ácido con otro elemento.[6]
Ejemplos:
- Ca(IO)2 - Hipoyodito de calcio
- Ca(HCO3)2 - Hidrogenocarbonato o bicarbonato de calcio
- AlSbO3 - Antimonito u Ortoantimonito de aluminio
- Pb(H2As2O7)2 - Dihidrogenopiroarseniato o Dihidrogenodiarseniato de plomo (IV)
- CaS2O3 - Tiosulfato de calcio
- CsH3SiO4 - Trihidrogenoortosilicato de cesio
- ZnSiO3 - Silicato o Metasilicato de zinc
- Rb3PO2 - Hipofosfito de rubidio
- Na4As2O3 Dihipoarsenito de sodio
- NiSeO3 - Selenito de níquel (II)
Iones poliatómicos especiales de uso frecuente
| ÁCIDO | ANIÓN | ||
|---|---|---|---|
| NH4+ | Catión amonio | CN- | Cianuro |
| Hg22+ | Catión mercuroso | OCN- | Cianato |
| O22- | Peróxido | SCN- | Tiocianato |
| S22- | Disulfuro | MnO42- | Manganato |
| S32- | Trisulfuro | MnO4- | Permanganato |
| Sn2- | Polisulfuro | CrO42- | Cromato |
| C22- | Acetiluro | Cr2O72- | Dicromato |
| OH- | Hidróxido | CH3-COO- | Acetato |
Referencias
- Chemistry, International Union of Pure and Applied. «IUPAC Compendium of Chemical Terminology». iupac.org (IUPAC). doi:10.1351/goldbook.O04374.
- Dianelys Ondarse Álvarez (7 de junio de 2022). «Oxácidos (u oxiácidos)». La enciclopedia de ejemplos. Ejemplos de oxiácidos u oxácidos. Consultado el 27 de noviembre de 2022.
- «Ejemplos de Ácidos Oxácidos». Químicas. 5 de octubre de 2015. Ejemplos de Ácidos Oxácidos. Consultado el 27 de noviembre de 2022.
- Gabriel Bolívar (9 de enero de 2019). «Oxácido: qué son, características, cómo se forman, ejemplos». Lifeder. Consultado el 27 de noviembre de 2022.
- Anne Marie Helmenstine (22 de octubre de 2019). «Common Oxoacid Compounds». Consultado el 27 de noviembre de 2022.
- Julian C. Ibarra Quintero. «Formulación química». Sales Ternarias.