1,1,1,3-tetracloro-4-metilpentano
El 1,1,1,3-tetracloro-4-metilpentano es un compuesto orgánico de fórmula molecular C6H10Cl4. Es un haloalcano no lineal de seis carbonos con cuatro átomos de cloro, tres de ellos unidos a uno de los carbonos terminales.[2][3][4]
| 1,1,1,3-tetracloro-4-metilpentano | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| 1,1,1,3-tetracloro-4-metilpentano | ||
| General | ||
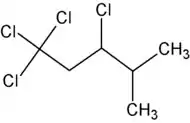
| Fórmula semidesarrollada | Cl3C-CH2-ClCH-CH(CH3)-CH3 | |
| Fórmula molecular | C6H10Cl4 | |
| Identificadores | ||
| Número CAS | 62103-09-7[1] | |
| ChemSpider | 101104 | |
| PubChem | 112804 | |
|
CC(C)C(CC(Cl)(Cl)Cl)Cl
| ||
| Propiedades físicas | ||
| Densidad | 1287 kg/m³; 1,287 g/cm³ | |
| Masa molar | 2239 g/mol | |
| Punto de fusión | −16 °C (257 K) | |
| Punto de ebullición | 209 °C (482 K) | |
| Presión de vapor | 0,3 ± 0,4 mmHg | |
| Índice de refracción (nD) | 1,477 | |
| Propiedades químicas | ||
| Solubilidad en agua | 4 mg/L | |
| log P | 4,40 | |
| Familia | Haloalcano | |
| Peligrosidad | ||
| Punto de inflamabilidad | 345 K (72 °C) | |
| Compuestos relacionados | ||
| cloroalcanos |
1-clorohexano 2-clorohexano 1-cloro-3,3-dimetilbutano | |
| dicloroalcanos |
1,6-diclorohexano 3,4-diclorohexano | |
| policloroalcanos | Tetracloruro de pentaeritritilo | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Propiedades físicas y químicas
El 1,1,1,3-tetracloro-4-metilpentano tiene una densidad de 1,287 g/cm³. Hierve a 209 °C mientras que su punto de fusión es -16 °C, siendo ambos valores estimados. Su punto de inflamabilidad es 72 ± 16 °C.[3]
El valor del logaritmo de su coeficiente de reparto, logP = 4,40, indica que es más soluble en disolventes apolares que en disolventes polares. Es prácticamente insoluble en agua.[3]
Síntesis
El 1,1,1,3-tetracloro-4-metilpentano se sintetiza haciendo reaccionar 3-metil-1-buteno con un tetrahaluro de carbono, preferiblemente tetraclorometano. Esta reacción requiere un catalizador, que puede ser un peróxido (como peróxido de benzoílo, terc-butilperoxiacetato o ácido terc-butilperoximaleico), azobisisobutironitrilo o un complejo de coordinación (como butilamina-cloruro férrico hexahidrato). La condensación se realiza en atmósfera inerte, por ejemplo nitrógeno o argón, a una temperatura de 80 - 110 °C.[5] Utilizando cloruro de cobre y ciclohexilamina a 80 °C se alcanza un rendimiento del 92%.[6]
Usos
El 1,1,1,3-tetracloro-4-metilpentano se utiliza en la preparación de 1,1-dicloro-4-metil-1,3-pentadieno, importante intermediario en la fabricación de insecticidas piretroides como la permetrina y la cipermetrina. Esto se puede hacer por deshidrocloración de 1,1,1,3-tetracloro-4-metilpentano mediante tratamiento con N,N-dimetilformamida, calentando la mezcla de reacción a una temperatura de 130 - 160 °C.[7] Con este procedimiento, empleando un cloruro inorgánico de amonio, litio, sodio o potasio, entre otros, se consigue un rendimiento cercano al 100%.[8] Análogamente, el uso de cloruro de estaño (IV) conlleva un endimiento del 88%.[9]
El 1,1,1,3-tetracloro-4-metilpentano también se emplea como intermediario en la elaboración de carbamatos de bencimidazol con actividad antihelmíntica.[10]
Referencias
- Número CAS
- 1,1,1,3-Tetrachloro-4-methylpentane (PubChem)
- 1,1,1,3-Tetrachloro-4-methylpentane (ChemSpider)
- 1,1,1,3-Tetrachloro-4-methylpentane (Chemical Book)
- Process to 1,1-dihalo-4-methyl-1,3-pentadienes, pyrethroid insecticide intermediates (1976) Lupichuk, A. Patente US4070404A
- Method for preparation of halogenated organic compounds (1980) Милан Гайек et al. Patente SU1703636A1
- Method of 1,1-dichloro-4-methyl-1,3-pentadiene preparation (1989) Hajek, M.; Cermak, J.; Silhavy, P.; Novak, M.; Spirkova, B. Patente CS273876B1
- Process for 1,1-dihalo-4-methyl-1,3-pentadienes (1980) Robbins, J.D.; Mihailovski, A. Patente CA1147350A
- Process for the manufacture of 1,1-dihalo-4-methyl-1,3-pentadienes (1978) Pitt, H.M Patente US4271325A
- Method of benzimidazole-carbamates production (1979) Piccardi, P.; Confalonieri, G.; Lino Da Col.; Ramella, P.G. Patente CS242859B2