Tetracloruro de pentaeritritilo
El tetracloruro de pentaeritritilo es un compuesto orgánico de fórmula molecular C5H8Cl4. En este compuesto organoclorado, cuatro grupos clorometil (-CH2-Cl) se hallan unidos a un mismo carbono cuaternario. Recibe también los nombres de tetrakis(clorometil)metano, tetracloruro de pentaeritritol y, en nomenclatura IUPAC, 1,3-dicloro-2,2-bis(clorometil)propano.[2][3][4]
| Tetracloruro de pentaeritritilo | ||
|---|---|---|
 | ||
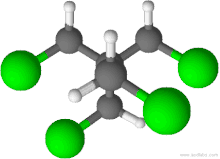 | ||
| Nombre IUPAC | ||
| 1,3-dicloro-2,2-bis(clorometil)propano | ||
| General | ||
| Otros nombres |
Tetrakis(clorometil)metano 2,2-bis(clorometil)-1,3-dicloropropano Tetracloruro de pentaeritritol | |
| Fórmula semidesarrollada | ClCH2-C(CH2Cl)2-CH2Cl | |
| Fórmula molecular | C5H8Cl4 | |
| Identificadores | ||
| Número CAS | 3228-99-7[1] | |
| ChemSpider | 69160 | |
| PubChem | 76700 | |
|
C(C(CCl)(CCl)CCl)Cl
| ||
| Propiedades físicas | ||
| Apariencia | Sólido beige | |
| Olor | Inodoro | |
| Densidad | 1327 kg/m³; 1,327 g/cm³ | |
| Masa molar | 2660 g/mol | |
| Punto de fusión | 96 °C (369 K) | |
| Punto de ebullición | 233 °C (506 K) | |
| Presión de vapor | 0,1 mmHg | |
| Índice de refracción (nD) | 1,481 | |
| Propiedades químicas | ||
| Solubilidad en agua | 26 mg/L | |
| log P | 3,47 | |
| Familia | Haloalcano | |
| Peligrosidad | ||
| NFPA 704 |
0
1
0
| |
| Compuestos relacionados | ||
| dicloroalcanos | 1,5-dicloropentano | |
| policloroalcanos |
1,1,1-tris(clorometil)etano 1,1,1,3-tetracloro-4-metilpentano | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Propiedades físicas y químicas
El tetracloruro de pentaeritritilo es un sólido inodoro de color beige con una densidad de 1,327 g/cm³. Su punto de fusión es 96 °C y su punto de ebullición, a 12 mmHg de presión, es 110 °C mientras que a presión normal es en torno a 233 °C.[3] El valor del logaritmo de su coeficiente de reparto, logP = 3,474, indica que es más soluble en disolventes apolares que en disolventes polares. Es prácticamente insoluble en agua.[3]
En cuanto a su estabilidad, este compuesto no es compatible con agentes oxidantes fuertes.[5]
Síntesis
El tetracloruro de pentaeritritilo se puede preparar calentando triclorhidrina de pentaeritritol con pentacloruro de fósforo a 150 °C. También se puede elaborar calentando disulfito de pentaeritritol con un oxicloruro sulfuroso, como cloruro de tionilo, en presencia de un catalizador de hidrocloruro de piridina. Otra vía de síntesis es haciendo reaccionar pentaeritritol con cloruro de p-toluenosulfonilo en presencia de cantidades sustanciales de piridina a una temperatura superior a 100 °C.[6]
La reacción de tetraclorometano con diazometano bajo irradiación es otra forma de preparar tetracloruro de pentaeritritilo, obteniéndose un rendimiento del 61%. La reacción se lleva a cabo en un flujo de nitrógeno durante dos horas. Sin embargo, si se sustituye el tetraclorometano por cloroformo, el principal producto que se forma es 1-cloro-2,2-bis(clorometil)propano.[7]
Usos
El tetracloruro de pentaeritritilo sirve para preparar pentaeritritil tetramina (PETA) por amonólisis. Se pueden emplear diversos catalizadores para esta reacción, tales como haluros de amonio cuaternario, aminas terciarias o epóxidos de olefinas, entre otros.[8] En este sentido, el tratamiento del tetracloruro de pentaeritritilo con un exceso de amoníaco caliente muy comprimido produce pentaeritritil tetramina con un rendimiento del 57%; dicha amonólisis puede realizarse en amoníaco supercrítico solo o utilizando metanol como disolvente.[9]
Asimismo, este cloroalcano se usa para producir pentaeritritiol, lo que se consigue tratando el tetracloruro de pentaeritritilo con tetrasulfuro disódico en un disolvente polar aprótico (como N,N-dimetilformamida), seguido de reducción con polvo metálico de platino, paladio, níquel o zinc.[10]
Otros usos del tetracloruro de pentaeritritilo son como agente de acoplamiento en la fabricación de polímeros de caucho,[11] en membranas asimétricas para su uso en nanofiltración[12] y como disolvente en composiciones que se usan para fabricar láminas semiconductoras de alta movilidad.[13]
Véase también
El siguiente compuesto es isómero del tetracloruro de pentaeritritilo:
Referencias
- Número CAS
- Pentaerythrityl tetrachloride (PubChem)
- 1,3-dichloro-2,2-bis(chloromethyl)propane (ChemSpider)
- Pentaerythrityl tetrachloride (Chemical Book)
- Pentaerythrityl tetrachloride. Safety data sheet (Acros)
- Process for producing chlorohydrins of polyhydric alcohols (1944) Rapoport, H. Patente US2441595A
- Ulrich, H. (2007). «35.1.1.9.4.1 Variation 1: By Insertion of Methylene into C—Cl Bonds». Science of Synthesis 35: 129. Consultado el 29 de enero de 2020.
- Catalysts for the ammonolysis of pentaerythrityl tetrachloride (1977) Anderson, W.S. Patente US4117013A
- Anderson, W.S.; Hyer, H.J.; Sundberg, J.E.; Rudy, T.P. (2000). «Pentaerythrityltetramine». Ind. Eng. Chem. Res. 39 (11): 4011-4013. Consultado el 29 de enero de 2020.
- Production of pentaerythrithiol (1992) Kanemura, Y.; Kobayashi, S.; Sasagawa, K. Patente JPH05279321A
- Method for preparation of rubber coupled with pentaerythrityl tetrachloride (1993) 오정훈; 유동선; 윤동일 Patente KR970005479B1
- Asymmetric membranes for use in nanofiltration (2010) Livingston, A.G.; Bhole, Y.S. Patente CA2805780A1
- Semiconductor composition (2011) Wu, Y.; Wigglesworth, A.J.; Liu, P. Patente US20130140494A1
