Iodure de cadmium
L'iodure de cadmium est un composé chimique inorganique de cadmium et d'iode, de formule CdI2. Ce corps cristallin est connu pour sa structure cristalline, hexagonale, typique des composés de la forme MX2 avec de forts effets de polarisation, qui sert de référence à de nombreux autres composés.
| Iodure de cadmium | |

| |
| __ Cd2+ __ I− | |
| Identification | |
|---|---|
| Nom UICPA | iodure de cadmium(II) |
| No CAS | |
| No ECHA | 100.029.294 |
| No CE | 232-223-6 |
| No RTECS | EV1290000 |
| SMILES | |
| InChI | |
| Apparence | cristaux incolores à marron foncé, inodores, poudre gris jaune |
| Propriétés chimiques | |
| Formule | CdI2 [Isomères] |
| Masse molaire[1] | 366,22 ± 0,008 g/mol Cd 30,7 %, I 69,31 %, |
| Propriétés physiques | |
| T° fusion | 388 °C[2] |
| T° ébullition | 787 °C[2] |
| Solubilité | 1 850 g·l-1 (eau, 20 °C)[3] |
| Masse volumique | 5,670 g·cm-3 (30 °C)[3] |
| Thermochimie | |
| ΔvapH° | 115 kJ·mol-1 (1 atm, 744 °C)[4] |
| Cristallographie | |
| Symbole de Pearson | [5] |
| Classe cristalline ou groupe d’espace | P3m1 (no 164) [5] |
| Strukturbericht | C6[5] |
| Précautions | |
| SGH[2] | |
   Danger |
|
| SIMDUT[6] | |
 D1B, D2A, |
|
| NFPA 704[2] | |
| Transport[3] | |
| Classification du CIRC | |
| Groupe 1[2] | |
| Inhalation | Toxique en cas d'inhalation. Peut irriter le système respiratoire[2]. |
| Peau | Nocif en cas d'absorption par la peau. Peut provoquer une irritation de la peau[2]. |
| Yeux | Peut provoquer une irritation des yeux[2]. |
| Ingestion | Toxique en cas d'ingestion[2]. |
| Écotoxicologie | |
| DL50 | 166 mg/kg (souris, oral)[7] 222 mg/kg (rat, oral)[8] |
| Unités du SI et CNTP, sauf indication contraire. | |
Propriétés physiques et chimiques
L'iodure de cadmium est un solide stable, blanc nacré ou blanc très brillant, souvent sous forme de plaquettes hexagonales, ce qui permet de le fendre facilement[9]. Il est inaltérable à l'air, mais très soluble dans l'eau et l'alcool.
La solubilité maximales dans 100 g d'eau s'élève à 86,2 g de CdI2 à 25 °C, et à 125 g à 100 °C. Les solubilités sont encore plus grandes dans les alcools C1 ou C2, soient pour le solvant éthanol à 20 °C 110,5 g et le solvant méthanol à 25 °C 206,7 g, pour 100 g de solvant[10].
Dans l'acétone à 25 °C, la valeur maximale de solubilité n'est que de 41 g pour 100 g de solvant.
Le iodure de cadmium est très peu soluble dans le solvant ammoniac.
La liaison Cd-I est principalement ionique, mais avec un caractère covalent partiel[11].
Synthèse ou préparation
L'iodure de cadmium peut être synthétisé à température assez élevée à partir du cadmium et de vapeur de diiode,
- Cd vapeur ou métal mou chauffé + I2 gaz → CdI2
Il peut être préparé par l'action lente - ce qui se nommait "digestion chimique" - de l'iode liquide sur le métal solide, en présence de quantités très faibles d'eau, c'est-à-dire de traces d'eau apportés par humectation :
- Cd métal humecté d'eau + I2 liquide → CdI2
Il peut aussi être préparé par réaction de l'acide iodhydrique avec, au choix, le cadmium métal, son oxyde, son hydroxyde ou son carbonate. Le résultat est alors un iodure de cadmium hydraté qui peut être converti en iodure de cadmium anhydre par réaction avec le chlorure de thionyle[12]
Structure cristalline
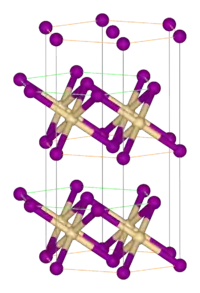
Dans l'iodure de cadmium, l'anion iodure forme une structure hexagonale compacte de groupe d'espace P63mc avec les paramètres a = 425 pm et c = 1367 pm, contenant deux molécules par maille élémentaire[13], les cations cadmium remplissant les sites octaédriques en couches alternées. Les ions cadmium sont donc au centre d'un octaèdre, entouré par six ions d'iodure . Chaque ion iodure est le sommet d'un pyramide trigonale dont la base est constitué de trois ions cadmium (coordination = 6:3). Les liaisons entre chaque couche d'iodure de cadmium individuelle sont faibles, résultant de forces de Van der Waals.
Sur les composés de même structure cristalline que CdI2
L'iodure de cadmium cristallise avec les mêmes caractéristiques de symétrie que les iodures avec cations modérément polarisant, les bromures et les chlorures avec cation fortement polarisant, les hydroxydes avec dications (M(OH)2) et les sulfures, séléniures et tellurures (chalcogénures) de tétracations (composés de formule MX2, où X = S, Se, Te).
- Chalcogénures de M4+ : TiS2, ZrS2, SnS2, α-TaS2, PtS2 ; TiSe2, ZrSe2, SnSe2, PtSe2 ; SiTe2, TiTe2, CoTe2, NiTe2, PdTe2, PtTe2.
Iodure de cadmium en solution aqueuse
L'iodure de cadmium CdI2 donne en solution aqueuse une gamme de divers ions en fonction de la concentration, il s'agit principalement de Cd2+aqueux, CdI+, CdI2, CdI3−, CdI42−...
Le caractère covalent de l'iodure de cadmium le distingue par exemple du fluorure de cadmium ionique. Les halogénures de cadmium sont moins ionisables que les halogénures de zinc et offre une plus grande facilité en solution pour la complexation.
Utilisation
L'iodure de cadmium est utilisé comme réactif pour la détection d'alcaloïdes - il se combine avec les bases hétérocycliques - et de l'acide nitreux.
L'iodure de cadmium est utilisé en lithographie, galvanoplastie et électrogalvanisation au cadmium. Il est employé en photographie et photogravure, par exemple dans certains procédés photographiques dit à ferrotype[9]. L'iodure de cadmium était employé autrefois en photographie pour sensibiliser le collodion.
Il est important dans la fabrication de matériaux phosphorescents (en) et de couches luminescentes[14].
Il s'agit d'un nématocide, à l'instar de l'oxyde de cadmium. Il est également utilisé en médecine.
Références
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Fiche Sigma-Aldrich du composé Cadmium iodide, consultée le 13 octobre 2012.
- Entrée « Cadmium iodide » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 13 octobre 2012 (JavaScript nécessaire)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-4200-9084-0)
- « The ω (C6) Phase », sur http://cst-www.nrl.navy.mil/ (consulté le )
- « Iodure de cadmium » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 24 avril 2009
- Aktual'nye Problemy Gigieny Truda. Current Problems of Labor Hygiene, Tarasenko, N.Y., ed. Moscow, Pervyi Moskovskii Meditsinskii Inst., Vol. -, p.14, 1978.
- Evaluation of the Impact of Cadmium on the Health of Man, Oxford, UK. Pergamon Press Ltd., Vol. -, p.67, 1978.
- (de) Cadmiumiodid. In: Römpp Chemie-Lexikon. Thieme Verlag, Stand März 2002.
- Bernard M. et Busnot F.,Usuel de chimie générale et minérale. Dunod, Paris, 1996, § solubilité
- (en) Norman N. Greenwood et Alan Earnshaw, Chemistry of the Elements, Butterworth-Heinemann, , 1211–1212 p. (ISBN 0080379419)
- (de) Arnold Holleman et Nils Wiberg, Lehrbuch der anorganischen Chemie, Berlin, New York, de Gruyter, , 1490 p. (ISBN 978-3-11-017770-1).
- (de) P. Villars, K. Cenzual: Structure types. Part 4: Space Groups (189) - (174). In: Landolt-Börnstein - Group III Condensed matters, Springer, Berlin 2006.
- (en) Pradyot Patnaik, Handbook of inorganic chemicals, New York, McGraw-Hill, , 1086 p. (ISBN 0-07-049439-8)
- (en)/(de) Cet article est partiellement ou en totalité issu des articles intitulés en anglais « Cadmium iodide » (voir la liste des auteurs) et en allemand « Cadmiumiodid » (voir la liste des auteurs).
- Portail de la chimie

