Réaction de couplage
En chimie organique, une réaction de couplage est une transformation qui permet l'association de deux radicaux hydrocarbures, en général à l'aide d'un catalyseur métallique. Deux classifications sont possibles en fonction de la nature du produit formé ou de celle des réactifs mis en jeu :
- dans le premier cas, si le produit est symétrique (formé par l'association de deux molécules identiques), on parle d'homocouplage. Il s'agit en général de la réaction d'un halogénure aromatique avec une deuxième molécule identique ou de celle d'un organométallique de la même manière. Si le produit n'est pas symétrique, on parle de couplage croisé, qui fait en général intervenir un composé organométallique et un halogénure (ou pseudo-halogénure) ;
- la seconde classification, d'origine mécanistique, s'applique principalement (mais pas seulement) aux homocouplages qui peuvent être soit oxydants, si les carbones associés voient leur nombre d'oxydation augmenter au cours de la réaction, soit réducteurs dans le cas où les nombres d'oxydation diminuent. Pour des raisons de contrôle des produits formés, il est difficile d'étendre ce mode de réaction aux couplages croisés, mais des études se fondant sur une cinétique bien maîtrisée des réactions concurrentes ont été mises au point récemment.
La réaction d'Ullmann est d'un exemple d'homocouplage : il s'agit de la réaction catalysée par du cuivre métallique de deux molécules d'un halogénure d'aryle afin de former un biaryle. La réaction d'Ullmann nécessite parfois de très hautes températures, et peut être parfois remplacée en chimie de synthèse par des réactions catalysée par du palladium.
De nombreuses réactions de couplage concernent les phénols. Le BINOL est le produit de réaction C-C du napht-2-ol avec du chlorure de cuivre (II) et le 2,6-xylénol dimérise avec le diacétate d'iodosobenzène.
Un des métaux les plus communs pour ce type de réactions est le palladium, parfois ajouté sous la forme du tétrakis(triphénylphosphine) palladium (0). De nombreux autres métaux, tels le nickel, le cobalt, le fer, le rhodium et le manganèse, sont également utilisés.
Alors que de nombreuses réactions de couplage impliquent des réactifs extrêmement sensibles à la présence d'eau ou d'oxygène, il est raisonnable d'affirmer que toutes les réactions de couplages doivent être réalisées en stricte absence d'eau. Il est possible de réaliser des réactions de couplage avec du palladium dans des solutions aqueuses en utilisant des phosphines sulfonées solubles dans l'eau synthétisées par la réaction de la triphénylphosphine avec de l'acide sulfurique. En général, l'oxygène de l'air est encore plus capable de faire avorter les réactions de couplages : en effet, nombre de ces réactions se produisent grâce à des complexes de métaux insaturés ne possédant pas 18 électrons de valence. Ainsi, les couplages croisés par nickel ou palladium un complexe à valence nulle avec deux sites vacants (ou ligands labiles) réagit avec la liaison carbone-halogène afin de former une liaison métal-halogène et une liaison métal-carbone. Un tel complexe à valence zéro avec des ligands labiles ou des sites de coordination vides est normalement très réactif à l'oxygène.
Types de couplages
Les réactions de couplages incluent (liste non exhaustive):
| Réaction | Année | Réactif A | Réactif B | Homo-/croisé | Catalyseur | Remarque | ||
| Réaction de Wurtz | 1855 | R-X | sp3 | homo- | Na | |||
| Couplage de Glaser | 1869 | R-X | sp | homo- | Cu | |||
| Réaction d'Ullmann | 1901 | R-X | sp2 | homo- | Cu | |||
| Réaction de Gomberg-Bachmann | 1924 | R-N2X | sp2 | homo- | Base requise | |||
| Couplage de Cadiot-Chodkiewicz | 1957 | alcyne | sp | R-X | sp | croisé | Cu | Base requise |
| Couplage de Castro-Stephens | 1963 | R-Cu | sp | R-X | sp2 | croisé | ||
| Couplage de Kumada | 1972 | R-MgBr | sp2, sp3 | R-X | sp2 | croisé | Pd ou Ni | |
| Réaction de Heck | 1972 | alcène | sp2 | R-X | sp2 | croisé | Pd | Base requise |
| Couplage de Sonogashira | 1973 | alcyne | sp | R-X | sp3 sp2 | croisé | Pd et Cu | Base requise |
| Couplage de Negishi | 1977 | R-Zn-X | sp2 | R-X | sp3 sp2 | croisé | Pd ou Ni | |
| Couplage croisé de Stille | 1977 | R-SnR3 | sp2 | R-X | sp3 sp2 | croisé | Pd | Base requise |
| Réaction de Suzuki | 1979 | R-B(OR)2 | sp2 | R-X | sp3 sp2 | croisé | Pd | Base requise |
| Couplage de Hiyama | 1988 | R-SiR3 | sp2 | R-X | sp3 sp2 | croisé | Pd | Base requise |
| Réaction de Buchwald-Hartwig | 1994 | R2-NH | sp2 | R-X | sp2 | croisé | Pd | Couplage N-C, la seconde génération libère l'amine. |
| Aperçu des réactions de couplages. Voir les liens pour les références | ||||||||
Réactions diverses
Une réaction de couplage inhabituelle a été décrite dans laquelle un composé organomolybdénien, [Mo3(CCH3)2(OAc)6(H2O)3](CF3SO3)2, est non seulement resté sur une étagère pendant 30 ans sans aucun signe de dégradation mais s'est aussi décomposé dans l'eau pour générer du 2-butyne qui est l'adduit de couplage de ses deux ligands éthylidyne[1]. Cela ouvre, selon les chercheurs, une autre voie pour la chimie organométallique aqueuse.
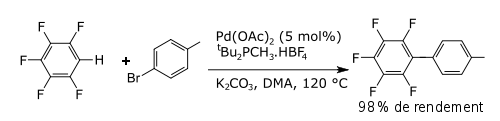
Une méthode pour les réactions de couplages croisés des halogénures d'aryle avec des arènes fluorés catalysées par palladium utilisant du DMA a été décrite. Elle est inhabituelle du fait qu'elle comprend une fonctionnalisation sur un arène déficitaire en électrons[2].
Références
- (en) A. Bino, M. Ardon et al., « Formation of a Carbon-Carbon Triple Bond by Coupling Reactions In Aqueous Solution », Science, vol. 308, no 5719, , p. 234-235 (ISSN 0036-8075, DOI 10.1126/science.1109965).
- (en) M. Lafrance, C. N. Rowley et al., « Catalytic Intermolecular Direct Arylation of Perfluorobenzenes », J. Am. Chem. Soc., vol. 128, no 27, , p. 8754–8756 (ISSN 0002-7863, DOI 10.1021/ja062509l).
- Portail de la chimie