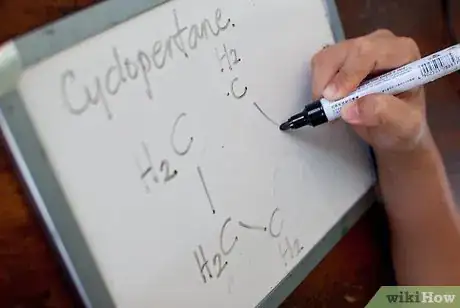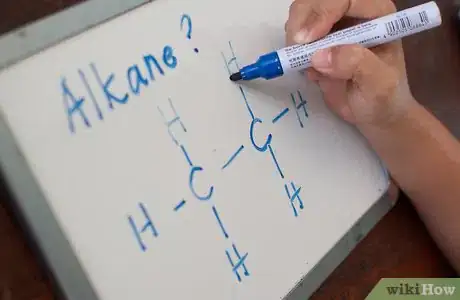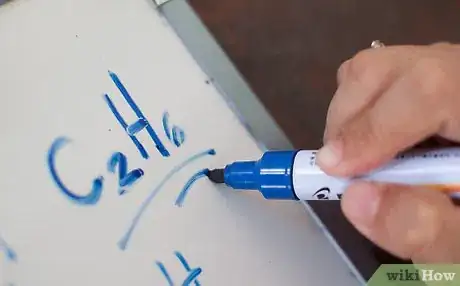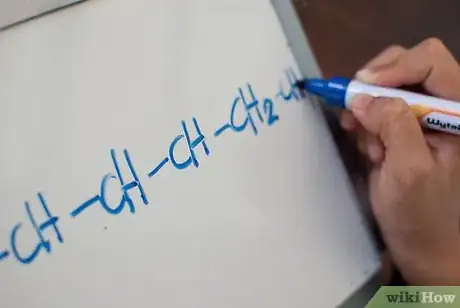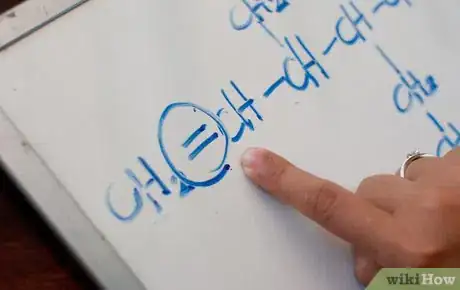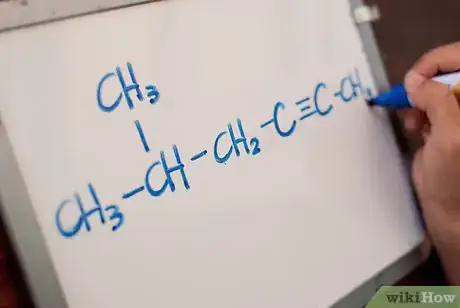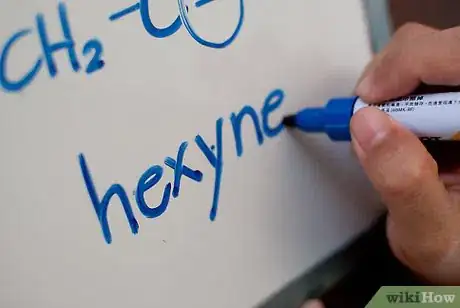X
wikiHow est un wiki, ce qui veut dire que de nombreux articles sont rédigés par plusieurs auteurs(es). Pour créer cet article, 33 personnes, certaines anonymes, ont participé à son édition et à son amélioration au fil du temps.
Cet article a été consulté 4 331 fois.
Composés d’une chaine d’hydrogènes et de carbones, les hydrocarbures forment la base de la chimie organique. La méthode communément acceptée pour nommer ces molécules suit les standards de l’UICPA (l’Union internationale de chimie pure et appliquée). Vous devrez donc vous référer à ces standards si vous voulez apprendre à nommer les hydrocarbures.
Étapes
-
1Renseignez-vous sur le pourquoi de ces règles. Les standards de l’UICPA ont été créés pour remplacer progressivement les anciens termes (comme le terme « toluène ») et les remplacer par un système plus cohérent qui fournit des informations sur l’emplacement des substituants (les atomes et (ou) molécules attachés à la chaine d’hydrocarbure).
-
2Gardez une liste des préfixes sous la main. Ces préfixes vous aideront à trouver le nom de vos hydrocarbures. Ils sont basés sur le nombre de carbones formant la chaine principale (et non pas sur la totalité des carbones de la molécule). Par exemple, CH3-CH3 correspond à l’éthane. Votre professeur ne s’attendra probablement pas à ce que vous connaissiez des préfixes au-delà de 10. Si c’est tout de même le cas, prenez des notes. Voici les 10 premiers préfixes utilisés :
- 1 : méth-
- 2 : éth-
- 3 : prop-
- 4 : but-
- 5 : pent-
- 6 : hex-
- 7 : hept-
- 8 : oct-
- 9 : non-
- 10 : dec-
-
3Entrainez-vous. Pour retenir les règles de l’UICPA, il faut s’entrainer. Lisez les méthodes proposées ici et inspirez-vous des exemples donnés, puis faites des exercices pratiques que vous trouverez sur Internet.Publicité
Méthode 1
Méthode 1 sur 5:Se familiariser avec les alcanes
Méthode 1
-
1Vous devez comprendre ce qu’est un alcane. Il s’agit d’une chaine hydrocarbonée qui ne contient aucune double ou triple liaison entre les molécules de carbone. Le suffixe à la fin d’un alcane est toujours -ane.
-
2Dessinez votre molécule. Vous pouvez choisir la formule développée plane ou la formule topologique. Trouvez celle que votre professeur vous a demandé d’utiliser et gardez cette méthode de représentation.
-
3Numérotez les atomes de carbone sur la chaine principale. Il s’agit de la chaine de carbone continue la plus longue dans la molécule. Commencez par le substituant le plus proche. Chaque substituant sera notifié par sa position numérique sur la chaine principale.
-
4Assemblez les noms par ordre alphabétique. Les substituants doivent être nommés alphabétiquement (sans prendre en compte les préfixes comme di-, tri- ou tétra-) et non pas par ordre de numérotation.
- Si vous avez deux substituants similaires sur une chaine, placez le préfixe « di » devant le substituant. Même s’ils sont attachés à la même chaine carbonée, notez deux fois la position du substituant.
Publicité
Méthode 2
Méthode 2 sur 5:Connaitre les alcènes
Méthode 2
-
1Vous devez savoir ce qu’est un alcène. Il s’agit d’une chaine hydrocarbonée qui contient au moins une double liaison carbone-carbone, mais aucune triple liaison. Le suffixe à la fin d’un alcène doit toujours être -ène.
-
2Dessinez votre molécule.
-
3Localisez la chaine principale. La chaine principale d’un alcane doit contenir au moins une double liaison carbone-carbone. De plus, elle doit être numérotée à partir de l’extrémité la plus proche de cette liaison.
-
4Notez où se trouve la double liaison. En plus de noter la position des substituants, vous devez noter la position de la double liaison. Faites cela de façon à ce que le numéro de la position soit le plus faible possible.
-
5Modifiez le suffixe en vous basant sur le nombre de doubles liaisons. Si la chaine principale a deux doubles liaisons, le nom de la molécule va se terminer par « -diène ». Trouvez trois doubles liaisons et la molécule se terminera « -triène », etc.
-
6Nommez les substituants par ordre alphabétique. Comme pour les alcanes, vous devez lister les substituants par ordre alphabétique, sans prendre en compte les préfixes di-, tri- et tétra-.Publicité
Méthode 3
Méthode 3 sur 5:Apprendre les alcynes
Méthode 3
-
1Sachez identifier un alcyne. Il s’agit d’une chaine hydrocarbonée présentant au moins une triple liaison carbone-carbone. Le suffixe est toujours -yne.
-
2Dessinez votre molécule.
-
3Localisez la chaine principale. La chaine principale d’un alcyne présente au moins une triple liaison. Numérotez à partir de l’extrémité la plus proche de la triple liaison carbone-carbone. La chaine principale de l’alcyne doit contenir au moins une triple liaison. Numérotez à partir de l’extrémité la plus proche de cette triple liaison.
- Si votre molécule possède à la fois des doubles et des triples liaisons, commencez à numéroter à partir de l’extrémité la plus proche de n’importe quelle liaison multiple.
-
4Notez la position de la triple liaison. En plus de noter la position des substituants sur la chaine alcène, vous devez noter la position de la triple liaison. Faites cela de sorte à utiliser le numéro le plus bas de la triple liaison.
- Si la molécule contient des doubles liaisons ainsi que des triples liaisons, vous devez également les localiser.
-
5Modifiez le suffixe. Pour ce faire, il faut se baser sur le nombre de triples liaisons dans la chaine principale. Si celle-ci comprend deux triples liaisons, le nom se terminera en « -diyne ». Si elle en a trois, elle se terminera par « -triyne », etc.
-
6Nommez les substituants par ordre alphabétique. Comme pour les alcanes et les alcènes, vous devez lister les substituants par ordre alphabétique. Ne tenez pas compte des préfixes tels que di-, tri- et delta-.
- Si votre molécule contient des doubles liaisons en plus des triples liaisons, les doubles doivent être nommées en premier.
Publicité
Méthode 4
Méthode 4 sur 5:Reconnaitre les hydrocarbures cycliques
Méthode 4
-
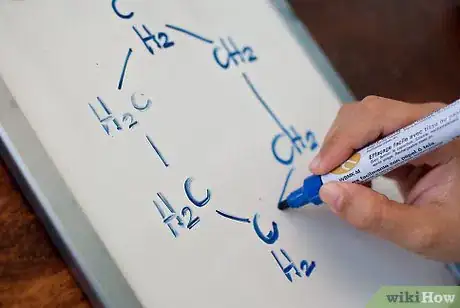
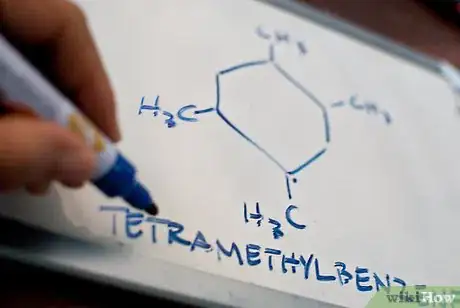
1Trouvez le type d’un hydrocarbure cyclique. Les hydrocarbures cycliques (ou aromatiques) fonctionnent comme les hydrocarbures non cycliques. Ceux qui ne contiennent aucune liaison multiple sont des cycloalcanes (ou cyclanes), deux contenant des doubles liaisons sont des cycloalcènes, ceux contenant des triples liaisons sont des cycloalcynes. Par exemple, un aromatique de 6 carbones avec aucune liaison multiple est un cyclohexane.
-
2Apprenez la raison de qualifier un hydrocarbure de cyclique. Il existe quelques différences notables entre des hydrocarbures cycliques et non cycliques :
- Tous les carbones d’un hydrocarbure cyclique sont égaux, c’est pourquoi il n’est pas nécessaire d’utiliser un chiffre si votre hydrocarbure ne présente qu’un seul substituant.
- Si le groupe alkyle attaché à l’hydrocarbure cyclique est plus long ou plus complexe que ce dernier, alors il peut devenir la chaine principale. L’hydrocarbure aromatique devient alors un substituant de cette chaine.
- Si deux substituants sont sur l’anneau, ils sont numérotés par ordre alphabétique. Le premier substituant (alphabétique) est le n°1, le suivant est numéroté dans le sens inverse des aiguilles d’une montre ou dans le sens des aiguilles d’une montre, selon ce qui donnera le numéro le plus faible pour le second substituant.
- Si l’anneau présente plus d’un substituant, le premier par ordre alphabétique est considéré comme attaché à la première molécule de carbone. Les autres sont numérotés dans le sens inverse des aiguilles d’une montre ou dans le sens des aiguilles d’une montre, selon ce qui donnera le numéro le plus faible.
- Comme tous les hydrocarbures non cycliques, la molécule finale est nommée dans l’ordre alphabétique, excepté les préfixes tels que di-, tri- et tétra-.
Publicité
Méthode 5
Méthode 5 sur 5:Se familiariser avec les dérivés du benzène
Méthode 5
-
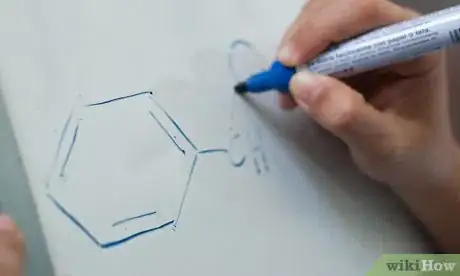
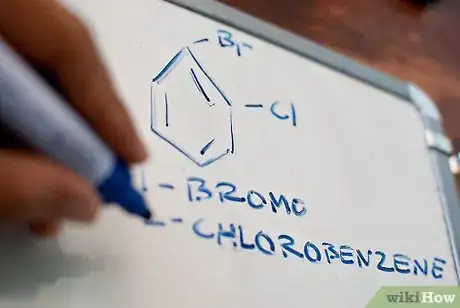
1Comprenez ce qu’est un dérivé du benzène. Il s’agit d’une molécule de benzène, soit C6H6, avec trois doubles liaisons espacées régulièrement.
-
2Ne numérotez pas s’il n’y a qu’un substituant. Comme pour tous les hydrocarbures cycliques, il n’est pas nécessaire de placer un chiffre sur l’anneau s’il n’y a qu’un seul substituant.
-
3Apprenez les conventions pour nommer les benzènes. Il est possible de nommer votre molécule de benzène comme vous le feriez pour n’importe quelle autre molécule d’hydrocarbure aromatique, c’est-à-dire par ordre alphabétique avec le premier substituant puis en continuant dans un sens ou dans l’autre. Cependant, les positions des substituants du benzène ont droit à une nomenclature spéciale :
- ortho ou o- : les deux substituants sont situés en position 1 et 2
- méta ou m- : les deux substituants sont situés en position 1 et 3
- para ou p- : les deux substituants sont situés en position 1 et 4
-
4Nommez une molécule à 3 substituants. Si votre molécule de benzène possède trois substituants, nommez-la comme vous nommeriez un hydrocarbure cyclique normal.Publicité
Conseils
- S’il y a deux possibilités pour la chaine la plus longue, choisissez celle avec le plus de branches. Si les deux chaines possèdent le même nombre de branches, choisissez celle qui forme une branche le plus tôt. Si les deux molécules forment une branche au même endroit, choisissez au hasard.
- Si un groupe OH (hydroxyle) est attaché quelque part sur un hydrocarbure, cela devient un alcool. Le composé est alors nommé avec le suffixe -ol au lieu de -ane.
- Continuez à vous entrainer ! Lorsque vous rencontrez ce type de problème en examen, il est probablement posé de façon à ce qu’il n’y ait qu’une seule bonne réponse. N’oubliez pas les règles de base et allez-y pas à pas.
Publicité
Avertissements
- De nombreux composés sont encore appelés par un autre nom que celui issu des standards de l’UIPCA. Par exemple, le groupe isopropyl composant une chaine latérale devrait s’appeler 1-méthyléthyl selon les standards de l’UIPCA. Faites attention à ne pas vous tromper dans les standards.
Publicité
À propos de ce wikiHow
Publicité