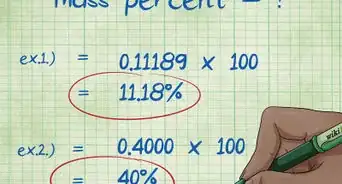Cet article a été coécrit par Bess Ruff, MA. Bess Ruff est doctorante en géographie à l'université d'État de Floride. Elle a obtenu un master en sciences et gestion de l'environnement à l'université de Californie, Santa Barbara, en 2016. Elle a aussi mené des enquêtes pour des projets de planification des espaces marins dans les Caraïbes et a contribué à la recherche en tant que boursière d'études supérieures pour Sustainable Fisheries Group.
En chimie, un composé chimique (ou corps composé) est une substance composée de deux ou plusieurs éléments. Il existe de nombreuses méthodes pour séparer et observer les éléments d’un composé chimique. Pour les fluides (liquides et gaz), il existe une technique connue sous le nom de chromatographie sur couche mince. Elle repose sur la différence de comportement entre une phase mobile courante et une phase fixe (ou stationnaire). En clair, les différents éléments du composé migrent (par exemple, sur un support papier) ou se transforment selon des modalités qui leur sont propres. La chromatographie est donc fondamentalement une technique de séparation.
Étapes
Partie 1
Partie 1 sur 3:Préparer la bandelette de chromatographie
-
1Récupérez ou découpez une bandelette de chromatographie. Une telle bandelette est poreuse : plongée dans un fluide (liquide, gaz) d’une certaine façon, elle permet de visualiser, sous forme de bandes, les composants d’un soluté. La bandelette est appelée « phase stationnaire », le fluide « phase mobile ». Si vous voulez un résultat parfait, vous pouvez acheter dans le commerce des bandelettes pour chromatographie, sinon vous les préparez-vous même en découpant dans un filtre à café en papier des bandes de 2,5 cm de large et d’une quinzaine de centimètres de long [1] .
- En fait, vous pouvez aussi prendre n’importe quel papier un peu absorbant, de l’essuietout par exemple.
-
2Tracez un trait dans le bas de la bandelette. Dans cette expérience, nous allons mettre en évidence les composants d’un feutre ou d’un marqueur noir (à encre délébile), l’encre étant le composé chimique. Tracez ce trait perpendiculairement à la bande à environ 2,5 cm du bas. En fait, le trait doit être à une hauteur telle que le bas de la bande soit immergé sans que le trait le soit [2] .
- Certains tracent un point un peu gros au lieu d’un trait, mais souvent le résultat est plus difficile à interpréter.
-
3Fixez solidement la bandelette. La bandelette sera fixée verticalement au centre du récipient, le trait de marqueur en bas. L’expérience durant quelques minutes, il est préférable de fixer la bandelette sur un axe rigide (crayon posé en travers) avec un bout d'adhésif ou une pince à linger, ainsi elle ne bougera pas. La bandelette ne touchera pas le fond, mais en sera proche. Comme les éléments migrent vers le haut, il ne faut pas qu’ils soient arrêtés par la pince [3] .
- Nous le disions, la fixation peut aussi se faire avec du ruban adhésif, et si la suspension se fait généralement au centre du récipient, elle peut être décalée à condition de ne pas toucher les bords.
Publicité
Partie 2
Partie 2 sur 3:Réaliser une chromatographie
-
1Versez de l’eau dans un gobelet. Ici, nous ferons chromatographie élémentaire avec de l’eau agissant comme phase mobile : en cas, cette dernière est appelée « éluant ». Versez un fond d’eau dans un récipient propre (bécher, verre) : pour être plus explicite, la bandelette va être plongée dans cette eau, il ne faut pas qu’elle atteigne le produit qui doit être analysé [4] .
-
2Plongez la bandelette dans l’eau. Elle sera introduite verticalement. Là n’est pas l’étape la plus délicate ; c’est sa fixation qui l’est, car la bandelette devra rester dans la même position, sans bouger, le temps de la migration des éléments. Si l’extrémité de la bandelette doit être immergée, ce n’est pas le cas du produit à analyser (ici, l’encre d’un feutre sous forme d’un trait). Si vous veniez à mouiller le trait, il ne vous resterait plus qu’à utiliser une autre bandelette [5] .
- Récupérez un crayon que vous poserez en travers du récipient, ainsi qu’une pince à linge. Approchez et disposez la bandelette comme cela a été dit, puis fixez-la avec une pince à linge. Vérifiez une dernière fois votre dispositif.
-
3Contentez-vous de regarder. Par capillarité, l’eau va remonter dans la bandelette, traverser le trait de feutre, embarquant au passage vers le haut les éléments constitutifs de l’encre du feutre. Les éléments légers migreront plus rapidement et plus haut que les éléments plus lourds. C’est ce qui va créer des bandes (en quelque sorte de dépôt) sur la bandelette. Cette décomposition est assez lente. Considérez que la migration est terminée quand l’eau est montée dans les trois quarts de la bandelette [6] .
- La durée de l’expérience dépend en fait, et c’est assez simple à comprendre, de la nature du matériau utilisé pour la bandelette.
- Ne bougez plus l’installation durant la migration et bien entendu, il est hors de question de remuer le mélange sous peine de fausser les résultats.
Publicité
Partie 3
Partie 3 sur 3:Analyser les bandes apparues
-
1Sortez la bandelette. Placez-la sur une surface lisse et attendez son séchage.
-
2Comptez le nombre de bandes. Une fois posée, votre bandelette ne doit plus bouger. Dans cette position, vous allez compter du mieux que vous pouvez les différentes bandes. Cela vous donnera une première idée du nombre de composants de votre soluté, ici l’encre du marqueur [7] .
-
3Relevez les différentes couleurs de bandes. Certes, l’encre du marqueur est noire, mais cette couleur est obtenue grâce à différents pigments qui physiquement et chimiquement ont des propriétés propres, dont certaines couleurs. Lors de la migration, ces pigments révèlent leur couleur d’origine. Même si elles ne sont pas toujours très faciles à définir, ces couleurs sont celles qui donnent le noir de départ [8] .
-
4Notez les caractéristiques des bandes. Vous ferez une liste des couleurs du haut vers le bas de la bandelette. Plus vous vous éloignez du haut de la bandelette, plus les éléments piégés sont lourds. Vous constaterez, cela peut varier d’un composé à l’autre, que les couleurs claires (associées aux éléments légers) sont plutôt en haut, tandis que les couleurs foncées sont plutôt vers le bas (éléments lourds). Eh oui ! La gravité joue même sur les éléments chimiques [9] !
- Le rapport de la distance parcourue par le soluté (L1) divisé par la distance parcourue par le front de l’éluant (L2) est appelé Rf : Rf = L1/L2. Cette formule s’applique sans restriction aucune à toutes les bandes, le dénominateur restant commun. Si vous avez 5 bandes, utilisez 5 fois la même formule, seul L1 va varier… et bien sûr Rf [10] .
- Vous venez de réaliser un test et vous avez une bande de couleur à 2 cm du trait d’encre, alors que l’eau est montée jusqu’à 5 cm du même trait. La formule de Rf se présente de la façon suivante :
- Rf = 2 cm / 5 cm
- Rf = 0,4
Publicité
Conseils
- Si vous voulez des résultats bien plus précis, vous devez acheter des bandelettes de papier pour chromatographie, ce papier étant particulier. Les bandes sont plus nettes, plus tranchées et leur analyse est donc plus fiable. Ces bandelettes s’achètent facilement sur des sites spécialisés dans le matériel de laboratoire.
- Si vous testez différentes encres, vous pourrez peut-être en tirer des conclusions sur la migration de telle ou telle couleur. C’est par exemple utile pour des analyses comparatives.
- En laboratoire, les chimistes utilisent des appareils spéciaux pour réaliser une chromatographie, laquelle peut être couplée avec une analyse au spectromètre de masse. La phase stationnaire peut être un fluide.
- L’encre utilisée doit être délébile. Les stylos-feutres donnent de bons résultats. Les stylos BIC, les crayons de couleur et les surligneurs ne donnent pas de bons résultats.
- Explication technique : les pigments qui ont servi à fabriquer la couleur ont chacun une structure chimique particulière, laquelle explique l’étagement des bandes chromatiques. En fait, chaque constituant est caractérisé par un coefficient de partage (K) qui est le rapport entre la concentration du soluté dans la phase stationnaire et celle de la concentration du soluté dans la phase mobile.
Avertissements
- Faites très attention à ne pas immerger le trait de marqueur dans l'éluant : la migration vers le haut des éléments ne pourrait se faire.
- Avant de faire le test, au tout début de l'expérience donc, laissez bien sécher le trait de marqueur.
Éléments nécessaires
- Une pince à linge
- Un filtre à café en papier
- Une paire de ciseaux
- De l'eau
- Une tasse (gobelet)
- Un marqueur noir
Références
- ↑ http://www.scienceprojectlab.com/paper-chromatography-experiment.html
- ↑ http://www.scienceprojectlab.com/paper-chromatography-experiment.html
- ↑ http://www.birdandlittlebird.com/blog/2012/08/kitchen-table-science-simple-chromatography.html
- ↑ http://www.birdandlittlebird.com/blog/2012/08/kitchen-table-science-simple-chromatography.html
- ↑ http://www.scienceprojectlab.com/paper-chromatography-experiment.html
- ↑ http://www.scienceprojectlab.com/paper-chromatography-experiment.html
- ↑ http://www.scienceprojectlab.com/paper-chromatography-experiment.html
- ↑ http://www.birdandlittlebird.com/blog/2012/08/kitchen-table-science-simple-chromatography.html
- ↑ http://www.birdandlittlebird.com/blog/2012/08/kitchen-table-science-simple-chromatography.html