إضافة بروتون
إضافة البروتون أو البرتنة (Protonation) هي إضافة بروتون (H+) لذرة، أو جزيء، أو أيون.[1][2]
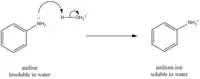
وعلى سبيل المثال ننظر إلى برتنة الأمونيا (NH3) بواسطة حمض الهيدروكلوريك (HCl),:
- يعطي حمض الهيدروكلوريك (مادة عاطي بروتون) بروتون إلى جزيئ الأمونيا. بذلك يتكون أنيون الكلور السالب الشحنة، وكاتيون الأمونيا موجب الشحنة. البروتون في الكيمياء هو أيون الهيدروجين وهو موجب الشحنة.
ويستخدم تفاعل وضع بروتون كثيرا لتنشيط مركب كيميائي للدخول في تفاعل. كما نستخدمه بغرض تأيين مركب، مثلما نعمل عند إجراء مطيافية الكتلة على أحد المواد.
المعادلة العامة
نقابل عملية وضع كاتيون الهيدروجين في مركب كيميائي في تفاعلات حمض-قاعدة. فيكتسب الجزيئ المستهدف عددا من الشحنات الموجبة مسازية لعدد البرونونات المعطاة له. وتوصف المادة التي أخذت بروتونا «مركب مبرتن»، وتلك المواد التي تقبل أخذ بروتونا أو أكثر تسمى مادة آخذ بروتون. وأما العملية العكسية وهي تفكك بروتون من مركب فتسمى نزع بروتون.
إذا كان لدينا حمضا HA فيمكنه إعطاء بروتون إلى مركب B فيصبح المركب «مبرتنا» طبقا للمعادلة:
ولكي تتم تلك العملية لا بد من وجود حمض وقاعدة طبقا لتعريف يوهانس نيكولاوس برونستد وتوماس لوري. وتمثل قوة الحمض بثابت تفكك الحمض pKa حيث a تأتي من كلمة Acid K
وقوة القاعدة بثابت تفكك القاعدة pKb حيث b تأتي من base، وهذا يعتمد على التوازن الكيميائي فإما أن يكون في صالح وضع بروتون في المركب أو نزع بروتون منه.
اقرأ أيضاً
مراجع
- Zumdahl, S. S. (1986)، Chemistry، Lexington, MA: Heath، ISBN 0-669-04529-2.
{{استشهاد بكتاب}}: تحقق من التاريخ في:|سنة=/|تاريخ=mismatch (مساعدة) - Kramarz, K. W.؛ Norton, J. R. (1994)، "Slow Proton Transfer Reactions in Organometallic and Bioinorganic Chemistry"، Progress in Inorganic Chemistry، 42: 1–65، doi:10.1002/9780470166437.ch1.
- بوابة الكيمياء
