شلل الأطفال
شلل الأطفال أو التهاب سنجابية النخاع[ar 1] (بالإنجليزية: Poliomyelitis) هو مرض معدٍ تُسببه الفيروسة السنجابية[2]، حوالي 0.5% من حالات شلل الأطفال تعاني من وهن عضلي يؤدي إلى شلل رخو، ويمكن أن يحدث هذا على مدى بضع ساعات إلى بضعة أيام[ar 2][2][3]، غالبًا ما يشمل الوهن الساقين، وبصورة أقل شيوعًا قد يشمل عضلات الرأس والعنق والحجاب الحاجز، يتعافى العديد من الأشخاص تمامًا من المرض، لكن الأشخاص الذين يعانون من ضعف العضلات يموت من الأطفال منهم حوالي 2-5% ومن البالغين 15-30%[2] لا تظهر أية أعراض على 70% من المصابين، بينما يعاني 25% من المصابين من أعراض بسيطة مثل الحمى والتهاب الحلق، ويعاني ما يصل إلى 5% من الصداع وتيبس الرقبة وآلام في الذراعين والساقين.[2][3] عادة ما يعود هؤلاء الأشخاص إلى طبيعتهم في غضون أسبوع أو أسبوعين[2]، لكن بعد سنوات من التعافي قد تحدث متلازمة ما بعد شلل الأطفال والتي يصحبها تطور بطيء لضعف العضلات مماثل لذلك الذي أصيب به الشخص أثناء العدوى الأولية.[5]
| شلل الأطفال | |
|---|---|
| (الاسم العلمي: Poliomyelitis) | |
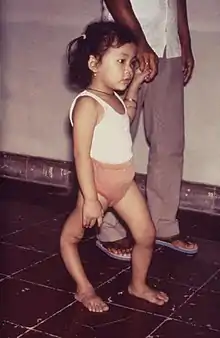
 رجل ذو ساق أيمن أصغر بسبب إصابته بشلل الأطفال. رجل ذو ساق أيمن أصغر بسبب إصابته بشلل الأطفال. | |
| معلومات عامة | |
| الاختصاص | أمراض معدية، وطب الجهاز العصبي، وجراحة العظام |
| من أنواع | مرض فيروسي، واعتلال الأعصاب المحيطية، وداء العصبون الحركي المكتسب ، وأمراض الجهاز العصبي المركزي الفيروسية، ومرض |
| الموقع التشريحي | جهاز عصبي محيطي[1] |
| الأسباب | |
| الأسباب | انتشار الفيروسة السنجابية عبر طريق فموي-شرجي.[2] |
| طريقة انتقال العامل المسبب للمرض | طريق فموي-شرجي، وانتقال بالاتصال |
| المظهر السريري | |
| البداية المعتادة | في غضون ساعات لأيام.[2][3] |
| الأعراض | وهن عضلي يُسبِّب شلل رخو.[2] |
| الإدارة | |
| الوقاية | لقاح شلل الأطفال.[3] |
| العلاج | الرعاية الداعمة.[3] |
| الوبائيات | |
| انتشار المرض | 136 شخصًا (في عام 2018).[4] |
| التاريخ | |
| وصفها المصدر | الموسوعة السوفيتية الأرمينية، وموسوعة بلوتو ، والموسوعة السوفيتية الكبرى |
عادةً ما ينتشر فيروس شلل الأطفال من شخص لآخر من خلال انتقال المواد البرازية للشخص المصاب عن طريق الفم، وقد ينتشر أيضًا عن طريق الطعام أو الماء المحتوي على براز المصاب، وبصفة أقل شيوعًا عن طريق لعاب الشخص المصاب[5]، قد ينقل المصابون المرض لمدة تصل إلى ستة أسابيع حتى في حالة عدم ظهور أعراض، ويمكن تشخيص المرض من خلال إيجاد الفيروس في البراز أو اكتشاف الأجسام المضادة له في الدم، ويحدث المرض بشكل طبيعي في البشر فقط.
يمكن الوقاية من المرض باستخدام لقاح شلل الأطفال ومع ذلك فهناك حاجة لجرعات متعددة لتكون فعالة، توصي المراكز الأمريكية للسيطرة على الأمراض والوقاية منها بتعزيزات التطعيم ضد شلل الأطفال للمسافرين والذين يعيشون في البلدان التي يحدث فيها المرض[6]، لكن بمجرد الإصابة لا يوجد علاج محدد[3]، في عام 2018 كانت هناك 33 حالة شلل أطفال بري و 104 حالة شلل أطفال مشتق من اللقاح[4]، وهذا يقل كثيرًا عن ظهور 350 ألف حالة لشلل الأطفال البري عام 1988، في عام 2018 انتشر المرض البري في أفغانستان وباكستان، وفي عام 2019 كانت هناك 175 حالة لشلل الأطفال البري و 364 حالة لشلل الأطفال المشتق من اللقاح.[7]
وُجِد شلل الأطفال منذ آلاف السنين مع تصوير للمرض في الفن القديم، تم التعرف على المرض لأول مرة كحالة مميزة بواسطة الطبيب الإنجليزي مايكل أندروود في عام 1789[2]، وتم تحديد الفيروس الذي يسببه لأول مرة في عام 1908 من قبل عالم المناعة النمساوي كارل لاندشتاينر[8]، بدأ المرض في التفشي في أواخر القرن التاسع عشر في أوروبا والولايات المتحدة،[2] وأصبح في القرن العشرين واحدًا من أكثر أمراض الطفولة إثارة للقلق في هذه المناطق[9]، تم تطوير أول لقاح شلل الأطفال في الخمسينيات من قبل جوناس سولك[10]، وبعد فترة وجيزة طوَّر ألبرت سابين لقاحًا عن طريق الفم والذي أصبح اللقاح المعياري العالمي.[11]
العلامات والأعراض
| النتيجة | نسبة الحالات[2] |
|---|---|
| لا أعراض | 72% |
| تعب بسيط | 24% |
| التهاب السحايا العقيم غير الشللي | 1–5% |
| التهاب سنجابية النخاع الشللي | 0.1–0.5% |
| التهاب سنجابية النخاع النخاعي | 79% من الحالات المشلولة |
| التهاب سنجابية النخاع البصلي-النخاعي | 19% من الحالات المشلولة |
| التهاب سنجابية النخاع البصلي | 2% من الحالات المشلولة |
يستخدم مصطلح «شلل الأطفال» لتحديد المرض الناتج عن أي من الأنماط المصلية الثلاثة لفيروس شلل الأطفال، وُصِفَ نمطان أساسيان لعدوى شلل الأطفال: مرض طفيف لا يشمل الجهاز العصبي المركزي (CNS) يُطلق عليه أحيانًا التهاب شلل الأطفال المجهض، ومرض رئيسي يصيب الجهاز العصبي المركزي والذي قد يكون شللي أو غير شللي[12]، في معظم الأشخاص الذين يعانون من أهلية مناعية تكون عدوى فيروس شلل الأطفال عديمة الأعراض، نادرًا ما تنتج العدوى أعراضًا طفيفة قد تشمل: عدوى الجهاز التنفسي العلوي (التهاب الحلق والحمى) واضطرابات الجهاز الهضمي (الغثيان أو القيء أو آلام البطن أو الإمساك أو نادرًا الإسهال) وأمراض شبيهة بالإنفلونزا.[ar 3] يدخل الفيروس إلى الجهاز العصبي المركزي في حوالي 1% من حالات العدوى. معظم المرضى الذين يعانون من إصابة الجهاز العصبي المركزي بالتهاب السحايا العقيم غير الشللي، يصابون بأعراض صداع وآلام الرقبة والظهر والبطن والأطراف والحمى والقيء والخمول والتهييج،[13][14] يتطور ما يقرب من واحد إلى خمسة من كل 1000 حالة إلى شلل حيث تصبح العضلات ضعيفة ومرنة وضعيفة التحكم وأخيرًا مشلولة تمامًا، تُعرف هذه الحالة بالشلل الرخو الحاد[15] بناءً على موقع الشلل يُصنَّف التهاب سنجابية النخاع الشللي إلى: نخاعي أو بصلي أو نخاعي بصلي، يمكن أن يحدث التهاب الدماغ -عدوى في أنسجة المخ نفسها- في حالات نادرة وعادة ما يقتصر على الرضع، وهو يتميز بالارتباك وتغيرات في الحالة العقلية والصداع والحمى وبصفة أقل شيوعًا نوبات الصرع والتقبضات.[16]
الأسباب
يحدث شلل الأطفال بسبب الإصابة بأحد أعضاء جنس الفيروس المعوي المعروف باسم الفيروسة السنجابية (PV)، هذه المجموعة من فيروسات الحمض النووي الريبوزي (RNA) تستعمر الجهاز الهضمي[17] -على وجه التحديد البلعوم والأمعاء-، يتراوح وقت الحضانة (إلى العلامات والأعراض الأولى) من ثلاثة إلى 35 يومًا لكن الفترة الأكثر شيوعًا من ستة إلى 20 يوماً[2]، تصيب الفيروسة السنجابية وتسبب المرض للبشر فقط[18]، يكون هيكلها بسيطًا للغاية، يتألف من جينوم من الحمض النووي الريبوزي المفرد موجب الاتجاه مغلف بقشرة بروتينية تُسمَّى قفيصة[19][ar 4]، بالإضافة إلى حماية المادة الوراثية للفيروس فإن قفيصة البروتينات أيضًا تُمكِّن فيروس شلل الأطفال من إصابة أنواع معينة من الخلايا، تم التعرف على ثلاثة أنماط مصلية لفيروس شلل الأطفال: فيروس شلل الأطفال النوع الأول (PV1) والنوع الثاني (PV2) والنوع الثالث (PV3)، لكل منها قفيصة بروتينات مختلفة قليلاً[19]، لكن الثلاثة لهم نفس الحدَّة ويُنتجون نفس أعراض المرض[18]، يُعد (PV1) هو الشكل الأكثر شيوعًا والأكثر ارتباطًا بالشلل.[20]
تتطوَّر مناعة الأفراد الذين يتعرضون للفيروس إما عن طريق العدوى أو عن طريق التحصين بلقاح شلل الأطفال وفي الأفراد المُحصَّنين توجد الأجسام المضادة غلوبيولين مناعي أ ضد فيروس شلل الأطفال في اللوزتين والجهاز الهضمي وتكون قادرة على منع تكاثر الفيروس، كما يمكن للأجسام المضادة غلوبيولين مناعي ج وغلوبيولين مناعي م التي تكوَّنت ضد فيروس شلل الأطفال أن تمنع انتشار الفيروس إلى الخلايا العصبية الحركية في الجهاز العصبي المركزي[21]، لا توفر العدوى أو التطعيم بنوع مصلي واحد من فيروس شلل الأطفال مناعة ضد الأنماط المصلية الأخرى، وتتطلب المناعة الكاملة التعرض لكل نمط مصلي.[21] يمكن أن تنتج حالة نادرة مع عرض مماثل- وهو ما يُعرف بـ«التهاب سنجابية النخاع غير المسبِّب للشلل»- عن العدوى بالفيروسات المعوية غير السنجابية.[22][ar 5]
انتقال المرض
يُعد شلل الأطفال مُعديًا للغاية بواسطة الطريق البرازي-الفموي (مصدر معوي) والطريق الفموي-الفموي (مصدر فموي بلعومي)، في المناطق الموبوءة يمكن أن تصيب فيروسات شلل الأطفال البرية جميع البشر تقريبًا[23]، وهي موسمية في المناخات المعتدلة مع ذروة انتقال تحدث في الصيف والخريف[21]، هذه الاختلافات الموسمية أقل وضوحًا بكثير في المناطق الاستوائية، عادة ما تكون الفترة بين التعرض الأول والأعراض الأولى -والمعروفة باسم فترة الحضانة- من 6 إلى 20 يومًا وبحد أقصى 3 إلى 35 يومًا[24]، تُفرَز جزيئات الفيروس في البراز لعدة أسابيع بعد الإصابة الأولية، ينتقل المرض في المقام الأول بواسطة الطريق البرازي-الفموي عن طريق تناول الطعام أو الماء الملوث[ar 6]، وينتقل أحيانًا بواسطة الطريق الفموي-الفموي، وهو طرز مرئي بشكل خاص في المناطق ذات الصرف الصحي والنظافة الجيدة، يكون شلل الأطفال أكثر عدوى 7-10 أيام قبل ظهور الأعراض وبعدها، ولكن الانتقال ممكنًا طالما بقي الفيروس في اللعاب أو البراز.[20] العوامل التي تزيد من خطر الإصابة بشلل الأطفال أو تؤثر على شدة المرض تشمل: نقص المناعة[25] وسوء التغذية[26] والنشاط البدني مباشرة بعد ظهور الشلل[27] وإصابة العضلات الهيكلية بسبب حقن اللقاحات أو العوامل العلاجية[28] والحمل[29]، وعلى الرغم من أن الفيروس يمكن أن يعبر الحاجز بين الأم والجنين أثناء الحمل لا يبدو أن الجنين يتأثر بإصابة الأم أو بالتطعيم ضد شلل الأطفال[30]، تعبر الأجسام المضادة للأمهات أيضًا المشيمة مما يوفر مناعة سلبية تحمي الرضيع من عدوى شلل الأطفال خلال الأشهر القليلة الأولى من الحياة.[31][ar 7]
الفيزيولوجيا المرضية
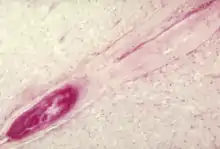
يدخل فيروس شلل الأطفال للجسم من خلال الفم مسببًا الإصابة لأول خلايا يلامسها وهي البلعوم والغشاء المخاطي للأمعاء، يتمكن من الدخول عن طريق الارتباط بمستقبل شبيه بالغلوبولين المناعي المعروف بمستقبل فيروس شلل الأطفال أو CD155 الموجود على جدار الخلية[32]، يختطف الفيروس آلية الخلية المضيفة ويبدأ بالتكاثر، ينقسم فيروس شلل الأطفال في الخلايا المعدية المعوية لمدة أسبوع، ومنها ينتشر إلى اللوزتين (وعلى وجه التحديد الخلايا المتغصنة الجرابية الموجودة في المراكز الجرثومية اللوزية) والنسيج الليمفاوي المعوي بما فيه من خلايا مركل في لطخة باير والعقد الليمفاوية المساريقية والعنقية العميقة حيث تتضاعف بكثرة، ويُمتَصّ الفيروس بعد ذلك إلى مجرى الدم.[33]
يعد تفيرس الدم[34] هي وجود الفيروس في مجرى الدم مما يمكنه من الانتشار بصورة أوسع خلال الجسم، يمكن للفيروس أن يبقى حيًا ويتضاعف في الدم والليمف لفترات طويلة تصل في بعض الأوقات إلى 17 أسبوعًا[35]، ويمكن أن ينتشر ويتضاعف في مواقع أخرى مثل نسيج الدهن البني وأنسجة جملة البلعميات والوحيدات والعضلات بنسب قليلة[36]، يُسبب التضاعف المستدام تفيرس دم رئيسي، ويمكن أن يتطور إلى أعراض تشبه الأنفلونزا، كما يمكن في حالات نادرة أن يتطور الفيروس ويغزو الجهاز العصبي المركزي ويثير استجابة التهابية موضعية، قد يُسبِّب في معظم الحالات التهاب ذاتي في السحايا (طبقات الأنسجة المحيطة بالمخ) والمعروف باسم التهاب السحايا المُعقَّم غير الشللي[13]، لا يوفِّر اختراق الجهاز العصبي المركزي أية فائدة معروفة للفيروس، وربما يكون مجرد انحراف عرضي لعدوى معوية-معدية طبيعية[37]، وتعتبر آلية انتشار فيروس شلل الأطفال في الجهاز العصبي المركزي غير مفهومة، ولكن يظهر أنها في المقام الأول حدثت صدفة ليست لها علاقة -إلى حد كبير- بالسن أو الجنس أو الوضع الاقتصادي الاجتماعي للفرد.[37]
التهاب سنجابية النخاع المُسَبِّب للشلل
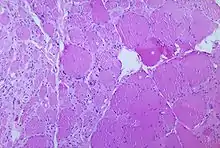
ينتشر فيروس شلل الأطفال في حوالي 1% من الإصابات في مسارات ألياف عصبية معينة، حيث يُفضَّل التضاعف فيها وتدمير الخلايا العصبية الحركية في النخاع الشوكي أو جذع المخ أو القشرة الحركية، يؤدي هذا إلى تطور شلل الأطفال الشللي، وتتنوع أشكاله المختلفة من (نخاعي، بصلي، بصلي نخاعي) وذلك بناءً على كمية التدمير العصبي والالتهاب الحادث والمنطقة المتأثرة في الجهاز العصبي المركزي.
ينتج عن تدمير الخلايا العصبية آفات في العقد الجذرية ويمكن أن يحدث هذا أيضًا في التشكل الشبكي والنوى الدهليزية ودودة المخيخ ونواة المخيخ العميقة[37]، يٌحدث الالتهاب المصاحب لتدمير الخلايا العصبية تغيُّر في لون وظهور المنطقة الرمادية من العمود الفقري مما يتسبب في ظهورها أكثر حمرة وانتفاخًا[13]، تحدث التغيرات التدميرية الأخرى المرتبطة بمرض الشلل في الدماغ الأمامي وخصوصًا منطقة المهاد وتحت المهاد[37]، تعتبر الآليات الجزيئية التي يعمل بها فيروس شلل الأطفال مسببًا الشلل غير مفهومة.
تشمل بداية أعراض شلل الأطفال الشللي ارتفاع في درجة الحرارة أو الصداع أو تصلب في الظهر والرقبة أو ضعف غير مماثل في عضلات مختلفة أو حساسية من اللمس أو عسر البلع أو ألم عضلات أو فقد الانعكاسات السطحية والعميقة أو الخدران (الشعور بدبابيس وإبر) أو تهيج أو إمساك أو صعوبة في التبول، يظهر الشلل عادة بعد يوم إلى عشرة أيام من بداية ظهور الأعراض ويتطور من يومين إلى ثلاتة أيام، ويكتمل عادة مع فترات الحمى.[38]
تزداد احتمالية الإصابة بشلل الأطفال الشللي بتقدم العمر وكذلك بمدى الشلل، فاحتمالية حدوث التهاب السحايا غير الشللي في الأطفال أكثر نتيجة لتدخل الجهاز العصبي المركزي، ويحدث الشلل لحالة واحدة من كل 1000 حالة، بينما يحدث الشلل في البالغين في حالة واحدة من كل 75 حالة[39]، يعتبر الشلل الحادث في ساق واحد هو الأكثر انتشارًا في الأطفال تحت عمر الخمس سنوات، بينما يعتبر الشلل واسع المدى المؤثر في الصدر والبطن بالإضافة إلى الأربعة أطراف -شلل رباعي- هو الأكثر احتمالية في البالغين[40]، تختلف نسب الشلل تبعًا للنمط المصلي لفيروس شلل الأطفال المؤثر؛ حيث ترتبط أعلى نسب الشلل (حالة في كل 200 شخص) بالنوع الأول من فيروس شلل الأطفال، بينما ترتبط أقل النسب (حالة في كل 2000 شخص) بالنوع الثاني.[41]
شلل الأطفال النخاعي
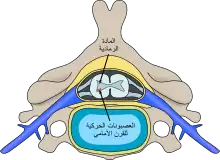
يعتبر شلل الأطفال النخاعي أكثر أنواع شلل الأطفال انتشارًا، وهو يحدث نتيجة لغزو فيروسي بواسطة الخلايا العصبية الحركية للخلايا القرنية الأمامية أو المادة الرمادية الباطنية (الأمامية) في العمود الفقري والمسؤولة عن حركة العضلات بما في ذلك الجذع والأطراف والعضلات بين الأضلاع[15]، يُسبب الغزو الفيروسي التهاب الخلايا العصبية مما يؤدي إلى تلف أو دمار العقد العصبية الحركية، وعند موت الخلايا العصبية النخاعية يحل محلها تنكس واليرياني، مما يؤدي إلى ضعف في تلك العضلات التي كانت تُغذَّى سابقًا بواسطة الخلايا العصبية التي تسبَّب المرض في موتها[42]، لا تستطيع العضلات بعد تلف الخلايا العصبية استقبال الإشارات من المخ أو الحبل الشوكي؛ ومع عدم وجود إثارة عصبية يحدث ضمور للعضلات وتصبح ضعيفة ومرنة وضعيفة التحكم وفي النهاية مشلولة تمامًا[15]، يتطور الشلل إلى أقصى حد سريعًا (يومين إلى أربعة أيام)، وعادة يتضمن حمى وألم في العضلات، كما تتأثر أيضًا استجابة منعكس الشد العميق وعادة ما تختفي أو تضعف بشكل تام، ومع ذلك فإنه لا يتأثر الإحساس (القدرة على الشعور) في الأطراف المشلولة.[43]
يعتمد مدى امتداد الشلل النخاعي على منطقة الحبل الشوكي المتأثرة حيث يمكن أن تكون عنقية أو صدرية أو قطنية[44]، ويمكن للفيروس أن يؤثر في عضلات جانبي الجسم، ولكن الشائع أكثر أن الشلل يكون لا متناظر[33]، يمكن لأي طرف أو مجموعة من الأطراف أن تتأثر: ساق واحدة أو ذراع واحد أو كلا الساقين أو كلا الذراعين، وغالبًا ما يكون الشلل قريبًا (حيث يلتحق الطرف بالجسم) أكثر من كونه بعيدًا (أطراف الأصابع وأصابع القدم).[33]
شلل الأطفال البصلي
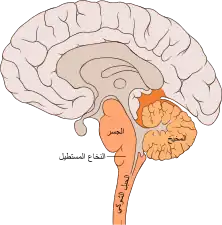
يُشكِّل شلل الأطفال البصلي حوالي 2% من حالات شلل الأطفال، ويحدث عندما يغزو فيروس شلل الأطفال الأعصاب الموجودة في المنطقة البصلية في جذع المخ ويدمرها[2]، تعتبر المنطقة البصلية هي مسار المادة البيضاء التي تصل القشرة المخية بجذع المخ، يؤدي تدمير هذه الأعصاب إلى ضعف في العضلات والتي تدعمها الأعصاب القحفية مما ينتج أعراض التهاب الدماغ الذي يُسبِّب ضيق النفس وصعوبة التحدُّث والبلع[14]، من الأعصاب الحرجة التي تتأثر أيضًا:
- العصب البلعومي اللساني (الذي يتحكم بشكل جزئي في البلع ووظائف في المرئ وحركة اللسان وحاسة التذوق).
- العصب المبهم (الذي يرسل الإشارات إلى القلب والأمعاء والرئتين).
- العصب الإضافي (الذي يتحكم في حركة العنق العلوية).
ينتج عن التأثير على البلع زيادة في إفراز المخاط في مجرى الهواء مما يسبب اختناق[38]، كما تتضمن الإشارات والأعراض الأخرى:
- ضعف وجهي (بسبب تلف العصب ثلاثي التوائم والعصب الوجهي حيث يتداخل مع الخدود والقنوات الأنفية الدمعية واللثة وعضلات الوجه من بين التراكيب الأخرى).
- ازدواج الرؤية وصعوبة في المضع وخلل في وتيرة التنفس وعمقه واتزانه (من الممكن أن يؤدي إلى توقف التنفس)، كما يمكن لوذمة الرئة والصدمة أن تكونا قاتلتين.[44]
شلل الأطفال البصلي النخاعي
لدى 19% تقريبًا من حالات شلل الأطفال الشللي أعراض الشلل البصلي والنخاعي، يسمى هذا النوع الفرعي بشلل الأطفال الرئوي أو البصلي النخاعي[2]، يؤثر الفيروس في هذا النوع على الجزء العلوي من العمود الفقري العنقي (من الفقرة العنقية الثالثة إلى الخامسة)، ويحدث أيضًا شلل للحجاب الحاجز ويكون العصب الحجابي من الأعصاب الحرجة المتأثرة (حيث يحث الحجاب الحاجز على نفخ الرئتين) مما يحث العضلات اللازمة في عملية البلع، يؤثر هذا النوع من شلل الأطفال على التنفس بتدمير تلك الأعصاب، ويجعل من الصعب أو من المستحيل أن يتمكن المريض من التنفس بدون مساعدة جهاز تنفس اصطناعي، يمكن أن يؤدي ذلك إلى شلل في الذراعين والقدمين ومن الممكن أيضًا أن يؤثر على البلع ووظائف القلب.[45]
التشخيص
قد يُشتبه طبيًا في الإصابة بشلل الأطفال الشللي في الأفراد الذين يعانون من أعراض حادة من الشلل الرخوي في طرف واحد أو أكثر من طرف مع قلة أو انعدام في المنعكس الوتري في الأطراف المتأثرة -الذي لا يمكن أن يُنسب إلى سبب آخر واضح- وبدون فقدان الإحساس والإدراك.[46]
يعتمد التشخيص المعملي عادة على فحص التعافي من شلل الأطفال بواسطة فحص عينة من البراز أو مسحة من البلعوم، ويمكن تشخيص الأجسام المضادة لفيروس شلل الأطفال التي عادة ما تُكتَشف في دم المرضى المصابين بالعدوى في مرحلة مبكرة من مراحل العدوى[2]، كما يُظهر تحليل السائل الدماغي الشوكي (CSF) للمريض -الذي يتم جمعه عن طريق البزل القطني- زيادة في عدد خلايا الدم البيضاء (الخلايا الليمفاوية الأولية) وارتفاع طفيف في مستوى البروتين، ويعتبر اكتشاف الفيروس في تحليل (CSF) هو تشخيص للإصابة بشلل الأطفال ولكن هذا نادرًا ما يحدث.[2]
إذا تم فصل فيروس شلل الأطفال من مريض مصاب بشلل رخوي حاد عادة ما يتم اختباره عن طريق موضعة قليل النوكليوتيد (البصمة الوراثية)، ومؤخرًا عن طريق تفاعل البوليمراز المتسلسل (PCR) لتحديد ما إذا كان نوع الفيروس «نوعًا بريًا» (أي أن الفيروس هو نفسه الذي وُجِد في الطبيعة) أم «نوعًا لقاحيًا» (مشتق من سلالة من فيروس شلل الأطفال المستخدمة لإنتاج لقاح لشلل الأطفال)[47]، يعتبر من المهم تحديد مصدر الفيروس وذلك لأن حالات شلل الأطفال الشللي التي تم الإبلاغ عنها والناتجة عن فيروس شلل الأطفال البري تُقدر بنحو 200 إلى 3000 حالة ناقلة للعدوى عديمة الأعراض.[48]
الوقاية
التمنيع اللافاعل
في عام 1950 قام ويليام هامون في جامعة بيتسبرغ بتنقية غلوبولين غاما -إحدى مكونات بلازما الدم للأشخاص المتعافين-[49]، اقترح هامون أن غلوبولين غاما الذي يحتوي على أجسام مضادة لفيروس شلل الأطفال يمكن استخدامه لوقف عدوى فيروس شلل الأطفال ومنع المرض وتقليل شدة المرض في المرضى الآخرين الذين أصيبوا بشلل الأطفال، كانت النتائج لتجربة سريرية كبيرة واعدة تبين أن غلوبولين غاما فعال بنسبة 80% تقريبًا لمنع تطور التهاب سنجابية النخاع الشللي[50]، وقد ثَبُت أيضًا أنه يقلل من شدة المرض لدى المرضى الذين أصيبوا بشلل الأطفال[2] وذلك بسبب الامتداد المحدود لغلوبولين غاما بلازما الدم والذى اعتُبِر لاحقًا أنه غير عملي للاستخدام على نطاق واسع وركز المجتمع الطبي على تطوير لقاح شلل الأطفال.[51]
اللقاح


يتم استخدام نوعين من اللقاحات في جميع أنحاء العالم لمكافحة شلل الأطفال، يؤدي كلا النوعين إلى الحصانة ضد شلل الأطفال مما يمنع بشكل فعال انتقال فيروس شلل الأطفال البري من شخص لآخر، وبالتالي حماية كل من متلقي اللقاح الفردي والمجتمع عامةً (وهو ما يسمى بمناعة جماعية).[52]
تم تطوير أول لقاح مرشح لشلل الأطفال بناءً على نمط مصلي واحد لفيروس حي لكنه موهن (ضعيف) من قبل عالم الفيروسات هيلاري كوبرويسكي، وقد أُعطَى لقاح كوبرويسكي النموذجي لصبي يبلغ من العمر ثماني سنوات يوم 27 فبراير 1950[53]، واصل كوبرويسكي العمل على اللقاح طوال الخمسينات مما أدى إلى تجارب واسعة النطاق في الكونغو البلجيكية آنذاك وتطعيم سبعة ملايين طفل في بولندا ضد الأنماط المصلية PV1 و PV3 بين عامي 1958 و1960[54]، بينما طُوِّرَ لقاح فيروس شلل الأطفال الثاني المعطل في عام 1952 من قبل جوناس سولك في جامعة بيتسبرغ وأُعلن للعالم في 12 أبريل 1955[55]، يُعد لقاح سولك أو لقاح فيروس شلل الأطفال المعطل مبنيًا على فيروس شلل الأطفال المزروع في نوع من أنسجة كلية القرد (خلية فيرو) والذي يُعطَّل كيميائيًا باستخدام الفورمالين.[56]
بعد جرعتين من لقاح فيروس شلل الأطفال المعطل (الذي يُعطَى عن طريق الحقن) يُطَوِّر 90% أو أكثر من الأشخاص أجسامًا مضادة للحماية لجميع الأنماط المصلية الثلاثة لفيروس شلل الأطفال و99% على الأقل يُصبح محصنًا ضد فيروس شلل الأطفال بعد ثلاث جرعات.[57]
في وقت لاحق طوَّر ألبرت سابين لقاحًا حيًا آخر لشلل الأطفال يؤخذ عن طريق الفم، وقد أُنتِج عن طريق المرور المتكرر للفيروس عبر الخلايا غير البشرية في درجات حرارة دون فيزيولوجية[58]، يتكاثر فيروس شلل الأطفال الموهن في لقاح سابين بكفاءة عالية في القناة الهضمية وهو الموقع الأساسي لعدوى فيروس شلل الأطفال وتكاثره، لكن سلالة اللقاح غير قادرة على التكاثر بكفاءة داخل أنسجة الجهاز العصبي[59]، جرعة واحدة من لقاح شلل الأطفال الفموي تنتج مناعة ضد جميع الأنماط المصلية الثلاثة لفيروس شلل الأطفال في حوالي 50% من المتلقين، بينما ثلاث جرعات من لقاح الفم الحي الموهن تنتج أجسامًا مضادة للحماية من جميع أنواع فيروس شلل الأطفال الثلاثة في أكثر من 95% من المتلقين[60]، وقد بدأت التجارب السريرية على لقاح سابين في عام 1957[61]، وفي عام 1958 تم اختياره في منافسة مع اللقاحات الحية لكوبرويسكي وباحثين آخرين من قبل المعاهد الوطنية الأمريكية للصحة[54]، تم ترخيصه في عام 1962[61] وأصبح بسرعة لقاح شلل الأطفال الوحيد المستخدم في جميع أنحاء العالم[54]، ولأن لقاح شلل الأطفال الفموي غير مكلف وسهل الإدارة ويُنتج مناعة ممتازة في الأمعاء (مما يساعد على منع العدوى بالفيروس البري في المناطق التي يستوطن فيها المرض) فأصبح هو اللقاح المفضل لمكافحة شلل الأطفال في العديد من البلدان[62]، وفي حالات نادرة جدًا (حوالي حالة واحدة لكل 750 ألف متلقٍ للقاح) يتحول الفيروس الموهن في لقاح شلل الأطفال الفموي إلى شكل يمكن أن يسبب المرض مرة أخرى[63]، في عام 2017 فاق عدد الحالات الناجمة عن فيروس شلل الأطفال المشتق من اللقاح (cVDPV) حالات فيروس شلل الأطفال البري للمرة الأولى بسبب حالات شلل الأطفال البرية التي انخفض عددها انخفاضًا قياسيًا[64]، اتجهت معظم الدول المتقدمة إلى لقاح شلل الأطفال المعطل -الذي لا يمكن عكس عمله- إما باعتباره اللقاح الوحيد ضد شلل الأطفال أو بالاشتراك مع لقاح شلل الأطفال الفموي.[65]
العلاج
لا يوجد علاج لشلل الأطفال، لذلك يركز العلاج الحديث على التخفيف من حدة الأعراض وتعجيل التعافي ومنع المضاعفات، وتضمن التدابير الداعمة المضادات الحيوية لمنع العدوى للعضلات الضعيفة بالإضافة إلى المسكنات لتخفيف الألم والتمارين المتوسطة ونظام غذائي مغذ[66]، كما يتطلب علاج شلل الأطفال إعادة تأهيل طويلة المدى تضمن علاج وظيفي وعلاج فيزيائي وسنادات وأحذية مُصلحة -وفي بعض الحالات- جراحة للعظام.[44]
ويمكن أن يتطلب أجهزة تنفس اصطناعية لدعم التنفس، وقديمًا تم استخدام أجهزة التنفس بالضغط السلبي غير التداخلي والتي أطلق عليها اسم الرئة الحديدية للحفاظ على التنفس اصطناعيًا أثناء عدوى حادة من شلل الأطفال حتى يتمكن الشخص من التنفس بشكل مستقل (عادة لمدة أسبوع أو أثنين)، يستخدم حاليًا الكثير من الناجين من شلل الأطفال المصابين بشلل تنفسي دائم أجهزة تنفس حديثة على شكل سترة لها تهوية ميكانيكية تُلبس على الصدر والبطن.[67]
تشمل العلاجات التاريخية الأخرى لشلل الأطفال: العلاج بالماء والعلاج الكهربي وتمارين التدليك والحركة السلبية والعلاجات الجراحية مثل إطالة الأوتار وزراعة الأعصاب.[15]
المآل
يتعافى المرضى الذين يعانون من عدوى شلل الأطفال المجهضة تمامًا، بينما الذين يصابون بالتهاب السحايا العقيم فقط يُتَوقع استمرار الأعراض لمدة يومين إلى عشرة أيام يتبعها الشفاء التام[68]، وفي حالات شلل الأطفال النخاعي إذا تم تدمير الخلايا العصبية المصابة بالكامل فسيكون الشلل دائمًا والخلايا التي لم يتم تدميرها ولكنها فقدت وظيفتها مؤقتًا قد تتعافى في غضون أربعة إلى ستة أسابيع بعد ظهورها.[69] يتعافى نصف مرضى شلل الأطفال النخاعي بالكامل ويتعافى الربع بإعاقة خفيفة بينما الربع المتبقي يظل بإعاقة شديدة[70]، من المرجح أن تكون درجة الشلل الحاد والشلل المتبقي متناسبة مع درجة الإصابة بتفيرس الدم وتتناسب عكسًيا مع درجة المناعة[71]، نادرًا ما يكون شلل الأطفال النخاعي مميتًا.[72] بدون دعم الجهاز التنفسي فإن عواقب التهاب سنجابية النخاع التي تصيب الجهاز التنفسي تشمل الاختناق أو ذات الرئة الشفطية[73]، وبشكل عام يموت 5-10% من مرضى شلل الأطفال بسبب شلل العضلات المستخدمة في التنفس[ar 2]، يختلف معدل الوفيات (CFR) حسب العمر: فحوالي 2-5% من الأطفال وما يصل إلى 15-30% من البالغين يموتون،[74] غالبًا ما يتسبب شلل الأطفال البصلي في الوفاة إذا لم يتم توفير الدعم التنفسي، ويتراوح معدل الوفيات بين 25 و75% اعتمادًا على عمر المريض،[74][75] وعندما تتوفر تهوية بالضغط المتقطع قد تنخفض نسبة الوفيات إلى 15%.[76]
التعافي
تؤدي العديد من حالات شلل الأطفال إلى شلل مؤقت فقط[77] حيث تعود النبضات العصبية إلى العضلات المشلولة سابقًا في غضون شهر وعادة ما يكتمل التعافي في غضون ستة إلى ثمانية أشهر[69]، تعتبر العمليات الفزيولوجية العصبية المشاركة في التعافي بعد التهاب سنجابية النخاع الشللي الحاد فعالة إلى حد ما حيث أن العضلات قادرة على الاحتفاظ بالقوة الطبيعية لها حتى في حالة فقد نصف الخلايا العصبية الحركية الأصلية[78]، ومن المحتمل أن يكون الشلل المتبقي بعد عام شللًا دائمًا على الرغم من وجود تعاف بسيط لقوة العضلات بعد فترة من 12 إلى 18 شهرًا من الإصابة.[79]
إحدى الآليات التي تشارك في التعافي هي تفريخ (تبرعم) نهايات العصبون، حيث تُطوّر الخلايا العصبية الحركية المتبقية في جذع الدماغ والحبل الشوكي فروعًا جديدة أو براعم عصبونية محورية[80]، يمكن لهذه البراعم أن تعيد التزويد العصبي الألياف العضلية اليتيمة التي تم حرمانها من التزويد العصبي بواسطة عدوى شلل الأطفال الحادة[81] مما ينتج عنه استعادة قدرة الألياف على الانكماش وتحسين قوتها[82]، قد ينتج عن تبرعم النهايات العصبية عدد قليل من الخلايا العصبية الحركية المتضخمة بشكل كبير والتي تقوم بالعمل الذي كانت تؤديه سابقا عدد يقارب من أربع أو خمس وحدات من الخلايا العصبية الحركية[83] فالخلية العصبية التي كانت تتحكم في 200 خلية عضلية تتحكم الآن في من 800 إلى 1000 خلية عضلية، من الآليات الأخرى التي تحدث أثناء مرحلة إعادة التأهيل والتي تساهم في استعادة قوة العضلات: تضخم الألياف العضلية، وتوسيع ألياف العضلات من خلال التمرين والنشاط وتحويل ألياف العضلات من النوع الثاني إلى ألياف العضلات من النوع الأول.[75][81]
بالإضافة إلى هذه العمليات الفسيولوجية يمتلك الجسم عددًا من الآليات التعويضية للحفاظ على الوظيفة في وجود الشلل المتبقي ويشمل ذلك: استخدام عضلات أضعف ذات شدة أعلى من المعتاد نسبة إلى السعة القصوى للعضلة وتعزيز التطوُّر الرياضي للعضلات التي لم تكن تُستخدم من قبل بالإضافة إلى استخدام الأربطة لتحقيق الثبات مما يسمح بحركة أكبر.
المضاعفات
غالبًا ما تحدث المضاعفات المتبقية لشلل الأطفال بعد عملية الشفاء الأولية، يمكن أن يؤدي شلل العضلات الجزئي والشلل في بعض الأحيان إلى تشوهات في الهيكل العظمي وشد المفاصل وإعاقة الحركة، وبمجرد أن تصبح عضلات الطرف رخوة قد تتداخل مع وظيفة العضلات الأخرى، ومن المظاهر النموذجية لهذه المشكلة القدم المستدقة (التي تُشبه حنف القدم)، يتطور هذا التشوه عندما تعمل العضلات التي تسحب أصابع القدم لأسفل ولكن تلك التي تسحبها لأعلى لا تعمل وتميل القدم بشكل طبيعي إلى السقوط نحو الأرض، وإذا تُركت المشكلة دون علاج فإن أوتار أخيل في الجزء الخلفي من القدم تتراجع ولا يمكن للقدم أن تتخذ وضعًا طبيعيًا، لا يمكن لضحايا شلل الأطفال الذين يصابون باعوجاج القدم المشي بشكل صحيح لأنهم لا يستطيعون وضع كعبهم على الأرض، يمكن أن يحدث وضع مماثل إذا أصيب الذراعان بالشلل[84]، وفي بعض الحالات يتباطأ نمو الساق المصابة بشلل الأطفال بينما تستمر الساق الأخرى في النمو بشكل طبيعي، والنتيجة أن ساق واحدة أقصر من الأخرى ويعرج الشخص ويميل إلى جانب ما مما يؤدي بدوره إلى تشوهات العمود الفقري (مثل انحراف العمود الفقري جانبيًا)[85]، وقد تحدث هشاشة العظام وزيادة احتمالية كسور العظام، يمكن أن يكون التدخل لمنع أو تقليل التفاوت في الطول هو إجراء جراحة تثبيت المشاشة على عظام الفخد البعيدة واللقمات الظنبوبية/الشظوية بحيث يُعاق نمو الأطراف اصطناعيًا، وبحلول وقت إغلاق الصفيحة المشاشية تكون الساقان أكثر مساواة في الطول، وبدلاً من ذلك يمكن تزويد الشخص بالأحذية المخصصة التي تصحح الفرق في أطوال الساق، قد يكون من المفيد أيضًا إجراء جراحة أخرى لإعادة التوازن إلى اختلالات ناهض/مضاد العضلات، قد يؤدي الاستخدام المطوَّل للسنادات أو الكراسي المتحركة إلى متلازمة الانضغاط العصبي بالإضافة إلى فقدان الوظيفة المناسبة للأوردة في الساقين بسبب تجمع الدم في الأطراف السفلية المشلولة[86]، تشمل مضاعفات توقُّف الحركة المطوَّل: وذمة الرئة والكليتين والقلب وذات الرئة الشفطية وعدوى الجهاز البولي وحصوات الكلى وتغلف معوي والتهاب عضلة القلب ومرض القلب الرئوي.
متلازمة ما بعد شلل الأطفال
يمكن أن تظهر بين 25% و 50% من الأفراد الذين تعافوا من شلل الأطفال في سن الطفولة أعراض إضافية بعد عقود من التعافي من العدوى الحادة[87] ولا سيما ضعف العضلات الجديد والتعب الشديد، تُعرف هذه الحالة باسم متلازمة ما بعد شلل الأطفال (PPS) أو عواقب ما بعد شلل الأطفال[82]، يُعتقد أن أعراض هذه المتلازمة تنطوي على فشل الوحدات الحركية الضخمة التي تم إنشاؤها أثناء مرحلة الشفاء من المرض الشللي[88][89]، ومن العوامل التي تُساهم في زيادة خطر الإصابة بمتلازمة ما بعد شلل الأطفال: الشيخوخة مع فقدان وحدات الخلايا العصبية ووجود ضعف متبقي دائم بعد الشفاء من المرض الحاد وإفراط استخدام أو عدم استخدام الخلايا العصبية، تُعَد متلازمة ما بعد شلل الأطفال مرضا بطيئا وازدياديا ولا يوجد له علاج محدد[82]، إن متلازمة ما بعد شلل الأطفال ليست معدية لكن الأشخاص الذين يعانون من المتلازمة لا يتخلصون من فيروس شلل الأطفال.[57]
علم الأوبئة
 | ||||
| الدولة | الحالات البرية | الحالات المشتقة
من اللقاح |
حالة الانتقال | الأنواع |
|---|---|---|---|---|
| 21 | 0 | متوطن | WPV1 | |
| 12 | 0 | متوطن | WPV1 | |
| 0 | 20 | cVDPV فقط | cVDPV2 | |
| 0 | 1 | cVDPV فقط | cVDPV1 | |
| 0 | 1 | cVDPV فقط | cVDPV2 | |
| 0 | 10 | cVDPV فقط | cVDPV2 | |
| 0 | 34 | cVDPV فقط | cVDPV2 | |
| 0 | 26 | cVDPV فقط | cVDPV1 | |
| 0 | 12 | cVDPV فقط | cVDPV2/3 | |
| المجموع | 33 | 104 | ||
انخفضت حالات الإصابة بشلل الأطفال بشكل كبير في العديد من الدول المتقدمة بعد الاستخدام الواسع للقاح شلل الأطفال في منتصف الخمسينات، وقد بدأ جهد عالمي للقضاء على شلل الأطفال في عام 1988 بقيادة منظمة الصحة العالمية واليونيسف ومؤسسة الروتاري،[92] فأدت هذه الجهود إلى خفض عدد الحالات التي يتم تشخيصها كل عام بنسبة 99.9% من حوالي 350 ألف حالة في عام 1988[ar 8] إلى مستوى منخفض بلغ 483 حالة في عام 2001، وبعد ذلك بقي عند مستوى حوالي 1000-2000 حالة سنويًا لعدد من السنوات[93][94]، في أبريل 2012 أعلنت جمعية الصحة العالمية أن الانتهاء من استئصال شلل الأطفال حالة برامجية طارئة للصحة العامة العالمية.[95]
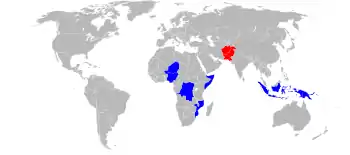
وفي عام 2015 أعتُقد أن شلل الأطفال لا يزال ينتشر بشكل طبيعي في دولتين فقط باكستان وأفغانستان[96][97][98][99] على الرغم من استمرار تفشي المرض في البلدان المجاورة الأخرى بسبب انتقاله الخفي أو المعاود[100]، في عام 2015 انخفضت الحالات إلى 98 وازداد انخفاضها في عام 2016 إلى 37 حالة مصابة بشلل الأطفال البري و5 حالات مشتقة من اللقاح، لكنها زادت في عام 2018 إلى 33 حالة مصابة بشلل الأطفال البري و103 حالة مشتقة من اللقاح[96][97][98][99]،
يُعد شلل الأطفال واحدًا من مرضين فقط يخضعان حاليًا لبرنامج استئصال عالمي فالمرض الآخر هو داء دودة غينيا[101]، وحتى الآن فإن الأمراض الوحيدة التي تم استئصالها تمامًا من قبل البشر هي: الجدري[102] -الذي تم الإعلان عن استئصاله في عام 1980-، وطاعون البقر[103] -الذي تم الإعلان عن استئصاله في عام 2011-.
وما يثير القلق هو وجود فيروسات شلل الأطفال دوارة مستمدة من اللقاح (cVDPV)، ولا يُعد لقاح شلل الأطفال الفموي لقاحًا مثاليًا؛ فبالرغم من أن الخصائص الجينية متوازنة بعناية لزيادة الفعالية إلى أقصى حد وتقليل حدة الفيروس فمن الممكن أن يتحور الفيروس في لقاح الفم، ونتيجة لذلك فإنه يمكن للأشخاص الذين يتلقون لقاح شلل الأطفال الفموي أن يصابوا بعدوى حادة أو مزمنة، كما يمكن أن ينتقل (ينتشر) الفيروس المتحور الدوَّار إلى أشخاص آخرين، وقد تجاوزت حالات الإصابة بفيروس شلل الأطفال المتداولة في اللقاحات حالات المرض البرية مما يجعل من المرغوب فيه التوقف عن استخدام لقاح شلل الأطفال الفموي في أقرب وقت آمن ممكن.[104]
أفغانستان وباكستان

المنطقة الأخيرة المتبقية بحالات شلل الأطفال البرية هي دول جنوب آسيا أفغانستان وباكستان، يدعم الجانبان الرئيسيان في الحرب الأهلية الأفغانية التطعيم ضد شلل الأطفال[106]، ولكن بعد الانخفاض السريع لعدد مصابي شلل الأطفال حول العالم تتزايد الأعداد في أفغانستان إلى 19 حالة في عام 2015[97][107] و13 في عام 2016 و14 في عام 2017[90] و21 حالة عام 2018 من بين عدد سكان يبلغ حوالي 35 مليون نسمة.
بينما في باكستان كانت هناك 53 حالة في عام 2015 (من بين حوالي 200 مليون نسمة) وهو أعلى رقم بين الدول[97][107] و20 حالة في عام 2016[108] و8 في عام 2017 و12 في عام 2018[91][109]، يعاق التطعيم في باكستان بسبب الصراع والمشاكل التنظيمية، وتقول حركة طالبان الباكستانية الجهادية أن التطعيم مؤامرة غربية لجعل الأطفال المحليين عقيمين[110][111]، ولقد قُتل 66 مُلقِّحًا في عامي 2013 و2014[112][113]، انخفضت الحالات بنسبة 97% من عام 2014 إلى 2018[114] وذلك بسبب: تخصيص 440 مليون درهمًا من الإمارات العربية المتحدة كدعم لتطعيم أكثر من عشرة ملايين طفل[110][115] بالإضافة إلى تغييرات في الوضع العسكري واعتقال بعض من هاجموا العاملين بمجال شلل الأطفال.[110][115]
الأمريكتان
أُعلنت الأمريكتان خلوهما من شلل الأطفال في عام 1994[116]، حيث كانت أخر حالة أُبلِغ عنها لفتى في بيرو عام 1991.[117]
غرب المحيط الهادئ
في عام 2000 أُعلن القضاء على شلل الأطفال رسميًا في 37 دولة في غرب المحيط الهادئ بما في ذلك الصين وأستراليا[118][119]، وعلى الرغم من دوام استئصاله مدة عشر سنوات أُكِّد تفشِّي المرض في الصين في سبتمبر 2011 وشموله على سلالة شائعة في باكستان.[120]
أوروبا
أعلنت أوروبا خلوَّها من شلل الأطفال في عام 2002[121]، وفي 1 سبتمبر 2015 أكدت منظمة الصحة العالمية حالتين من فيروس شلل الأطفال النوع الأول المشتق من اللقاح في أوكرانيا.[122]
جنوب شرق آسيا
كانت آخر حالة لشلل الأطفال في منطقة جنوب شرق آسيا في الهند (جزء من منطقة جنوب شرق آسيا التابع لمنظمة الصحة العالمية) في يناير 2011[123]، ومنذ يناير 2011 لم يتم الإبلاغ عن حالات عدوى شلل الأطفال البري في الهند، وفي فبراير 2012 حُذِفَ البلد من قائمة منظمة الصحة العالمية للبلدان التي يتوطن فيها شلل الأطفال، فقد أُعلن أنه إذا لم تكن هناك حالات لشلل الأطفال البري في البلاد لمدة عامين آخرين فسيُعلن أنها دولة خالية من شلل الأطفال.[124][125]
في 27 مارس 2014 أعلنت منظمة الصحة العالمية أنه تم استئصال شلل الأطفال في منطقة جنوب شرق آسيا والتي تشمل 11 دولة: بنغلاديش وبوتان وكوريا الشمالية والهند وإندونيسيا وجزر المالديف وميانمار ونيبال وسريلانكا وتايلاند وتيمور الشرقية[96]، وبالإضافة لهذه المنطقة كان هناك 80% من سكان العالم يعيشون في مناطق خالية من شلل الأطفال.[96]
في ديسمبر 2019 تم تأكيد إصابة طفل رضيع يبلغ من العمر 3 أشهر بشلل الأطفال الحاد في بلدة توران في ولاية صباح في بورنيو بماليزيا[126][127]، وكانت هذه أول حالة مؤكدة في ماليزيا منذ عام 1992 وأُعلنت ماليزيا خالية من شلل الأطفال في عام 2000، وبحسب ما ورد كان الطفل يعاني من حُمى وضعف عضلات، وعلى الرغم من استقرار حالته فقد احتاج إلى مساعدة للتنفس، وقد أشار اختبار الفيروس إلى أنه مرتبط بالسلالة التي ظهرت في الفلبين، وقال مسؤولون محليون إن السلالة نشأت من فيروس ضعيف مستخدَم في لقاح فموي أُفرز بعد ذلك في البراز وانتشر في السكان غير المُلقَّحين في ظروف غير صحية[126]، وقد أُعلِنَ أن 23 من أصل 199 طفلاً في المجتمع المحلي لم يتلقوا لقاح شلل الأطفال.[126]
تفشي شلل الأطفال في الفلبين 2019-20
أُبلِغَ عن تفشي شلل الأطفال في الفلبين في 19 سبتمبر 2019، فحصت السلطات عدة أماكن من بينها مترو مانيلا ومدينة دافاو بعد الإبلاغ عن حالتين لشلل الأطفال، تم تأكيد احتواء العينات المأخوذة من عدة أماكن في مانيلا على فيروس شلل الأطفال المشتق من اللقاح النوع الثاني (VDPV2) على غرار مُسبِّب المرض الموجود في الحالتين المؤكدتين الأوليين[128]، لذلك قررت الحكومة تطعيم جميع الأطفال بغض النظر عمَّا إذا كانوا قد أصيبوا بشلل الأطفال أم لا، وقد عملت المبادرة العالمية للقضاء على شلل الأطفال (GPEI) مع حكومة الفلبين في حملة تطعيم ضخمة ضد شلل الأطفال، كما شاركت منظمات غير حكومية أخرى مثل الصليب الأحمر في الحملة أيضًا.[129]
تم تأكيد أربع حالات حتى 5 نوفمبر 2019: الأولى كانت فتاة تبلغ من العمر ثلاث سنوات في لاناو ديل سور مع الحالات الأخرى المبلغ عنها في لاغونا وسلطنة ماغوينداناو وسلطان قادرات[130][131]، ويُعتقد أن عدم ثقة العامة في نظام الرعاية الصحية السيئ في البلاد هو سبب تفشي مرض شلل الأطفال.[132]
لا يُعد هذا أول تفشي للأمراض في الفلبين في عام 2019، ففي فبراير 2019 حدث تفشي لمرض الحصبة أيضًا نتيجة لعدم ثقة العامة في نظام الرعاية الصحية السيئ في الفلبين[133]، واعتبارًا من يناير 2019 كانت الفلبين تكافح تفشي حمى الضنك وهو أسوأ تفشي حمى الضنك شهدته الفلبين منذ عام 2012، ومثل تفشي مرض الحصبة كان تفشي حمى الضنك سببه عدم الثقة العامة في حملة التطعيم ضد حمى الضنك في عام 2012.[134]
وقد أثَّر ذلك على المجتمع المحلي بشكل خاص والعالمي بشكل عام:
- فعلى المستوى المحلي: تعمل منظمة الصحة العالمية واليونيسف وغيرها من المجتمعات الطبية الخاصة جنبًا إلى جنب لمساعدة وزارة الصحة الفلبينية في إجراء عمليات تطعيم هائلة في جميع أنحاء مترو مانيلا ومدينة دافاو ومدينة مراوي ومدن رئيسية أخرى في البلاد خلال هذا الوباء[135]، سعت الحملة لإنهاء زيادة الفيروس المميت، ووفقًا للصليب الأحمر الفلبيني فقد استمرت مدة التطعيم الشامل بين 14 و27 أكتوبر 2019، وكان عدد الأطفال الذين كان يُهدَف إلى تطعيمهم هو 65 ألف طفل[135]، قد تعهد الاتحاد الدولي لجمعيات الصليب الأحمر والهلال الأحمر (IFRC) بتقديم 336.700 دولارًا أمريكيًا من أموال الإغاثة في جهود استئصال شلل الأطفال من الفلبين اعتبارًا من 2 أكتوبر 2019.[132]
- وعلى المستوى العالمي: ليس فقط لم يُثبت التفشي وجود خطر على المواطنين الفلبينين فقط لكن الدول المجاورة الأخرى أصبحت تراقب انتشار المرض أيضًا، حيث أصدرت سفارة جمهورية إندونيسيا في الفلبين إرشادات بهدف منع انتشار شلل الأطفال.[136]
الشرق الأوسط
في سوريا أدت الصعوبات في تنفيذ برامج التحصين أثناء الحرب الأهلية الجارية إلى عودة شلل الأطفال على الأرجح في عام 2012[137]، اعترفت به منظمة الصحة العالمية عام 2013[138]، أُكِّدت 15 حالة إصابة بين الأطفال في سوريا بين أكتوبر ونوفمبر 2013 في دير الزور، فيما بعد تم التعرف على حالتين أخريين: واحدة في ريف دمشق والأخرى في حلب، كان هذا أول تفشي في سوريا منذ عام 1999، أبلغ الأطباء ووكالات الصحة العامة الدولية عن أكثر من 90 حالة إصابة بشلل الأطفال في سوريا مع مخاوف من العدوى في مناطق المتمردين بسبب نقص الصرف الصحي وخدمات المياه الآمنة[139](1)، في مايو 2014 أعلنت منظمة الصحة العالمية تجدُّد انتشار شلل الأطفال في حالة الطوارئ الصحية العالمية.[140][141]
كانت حملة التطعيم في سوريا تعمل حرفيًا تحت النيران وأدت إلى وفاة العديد من الملقِّحين[142] لكنها أعادت تغطية التطعيم إلى مستويات ما قبل الحرب.[143] تم تأكيد وباء آخر لشلل الأطفال في عام 2017 في شرق سوريا، وهو على الأرجح نتج عن شكل متحور للفيروس انتشر عبر المياه الملوثة.[144]
أفريقيا
في عام 2003 في شمال نيجيريا -وهي دولة كانت تعتبر في ذلك الوقت خالية من شلل الأطفال مؤقتًا- أعلن القادة السياسيون والدينيون أن لقاح شلل الأطفال مُصمَّم لجعل الأطفال عقيمين[145]، في وقت لاحق ظهر شلل الأطفال في نيجيريا وانتشر من هناك إلى العديد من البلدان الأخرى، في عام 2013 استُهدِف تسعة من العاملين الصحيين الذين يعملون على لقاح شلل الأطفال وقتلوا على يد مسلحين على درجات نارية في كانو لكن كان هذا الهجوم الوحيد[146][147]، عمل الزعماء التقليديون والدينيون المحليون والناجون من شلل الأطفال لإحياء الحملة[107]، وتمت إزالة نيجيريا من قائمة الدول المتوطنة لشلل الأطفال في سبتمبر 2015 بعد أكثر من عام دون أي حالات[148]، ولكن أُعيدت إلى القائمة عام 2016 عندما تم اكتشاف حالتين.[149]
في عام 2013 تلقى مركز السيطرة على الأمراض تقارير عن 183 حالة إصابة بشلل الأطفال في الصومال و 14 حالة في كينيا و8 حالات في المنطقة الصومالية في إثيوبيا[150]، لا يوجد حالات مؤكدة من فيروس شلل الأطفال البري (WPV) في أفريقيا منذ عام 2016[151]، تستمر حالات انتشار فيروس شلل الأطفال المشتق من اللقاح النوع الثاني في الظهور في العديد من البلدان.[152][153]
في 25 أغسطس 2020 أعلنت اللجنة الإقليمية الأفريقية للإشهاد (ARCC) أنَّ أفريقيا خاليةٌ من شلل الأطفال.[154]
التاريخ

آثار شلل الأطفال معروفة منذ عصور ما قبل التاريخ، تُصوِّر اللوحات والمنحوتات المصرية الأشخاص الأصحاء الذين يعانون من أطراف ذابلة والأطفال الذين يمشون بالعصي في سن مبكرة[155]، تم تقديم الوصف السريري الأول من قبل الطبيب الإنجليزي مايكل أندروود في عام 1789، حيث يشير إلى شلل الأطفال على أنه «ضعف في الأطراف السفلية»[156]، أدى عمل الطبيبان جاكوب هاين في عام 1840 وكارل أوسكار ميدين في عام 1890 إلى أن يُعرف بمرض هاين-ميدين[157]، لكن أطلق على المرض فيما بعد شلل الأطفال بناءً على ميله للتأثير على الأطفال.
قبل القرن العشرين نادرًا ما شوهدت عدوى شلل الأطفال عند الرضع قبل ستة أشهر من العمر حيث تحدث معظم الحالات في الأطفال من سن ستة أشهر إلى أربع سنوات، أدى سوء الصرف الصحي في ذلك الوقت إلى التعرض المستمر للفيروس مما عزز المناعة الطبيعية بين السكان، بينما في البلدان المتقدمة خلال أواخر القرن التاسع عشر وأوائل القرن العشرين أُجرِيَت تحسينات في الصرف الصحي المجتمعي بما في ذلك التخلص من مياه الصرف الصحي بشكل أفضل والحرص على إمدادات المياه النظيفة، أدت هذه التغيرات إلى زيادة كبيرة في نسبة الأطفال والبالغين المعرضين لخطر الإصابة بشلل الأطفال عن طريق الحد من تعرض وحصانة الأطفال ضد المرض.[158]
بدأ ظهور أوبئة شلل الأطفال المحلية الصغيرة في أوروبا والولايات المتحدة حوالي عام 1900[159]، بينما تفشى المرض إلى مستويات وبائية في أوروبا وأمريكا الشمالية وأستراليا ونيوزيلندا خلال النصف الأول من القرن العشرين، وبحلول عام 1950 تحولت الذروة العمرية لالتهاب سنجابية النخاع الشللي في الولايات المتحدة من الرُّضَّع إلى الأطفال الذين تتراوح أعمارهم بين خمس إلى تسع سنوات وعندها أصبح خطر الشلل أكبر حيث أن حوالي ثلث الحالات التي أُبلغ عنها كانوا أشخاصًا تزيد أعمارهم عن 15 سنة[160]، وبناء على ذلك ازداد معدل الشلل والوفاة بسبب عدوى شلل الأطفال خلال هذه الفترة[159]، في الولايات المتحدة أصبح وباء شلل الأطفال عام 1952 أسوأ تفشي في تاريخ البلاد، ومن حوالي 58 ألف حالة أُبلِغَ عنها في ذلك العام توفيت 3145 حالة واستمرت 21269 حالة تعاني من شلل خفيف إلى مُعيق.[161]
يعود أصل طب العناية المركزة إلى مكافحة شلل الأطفال[162]، فقد كانت معظم المستشفيات في الخمسينات من القرن الماضي محدودة الوصول إلى رئتين حديديتين للمرضى غير القادرين على التنفس دون مساعدة ميكانيكية، فصُمِّمَّت مراكز الجهاز التنفسي لمساعدة الحالات المريضة بشدة بشلل الأطفال، وتأسست لأول مرة في عام 1952 في مستشفى بليجدام في كوبنهاغن من قبل طبيب التخدير الدنماركي بيورن إيبسن، والتي كانت طليعة وحدات العناية المركزة الحديثة (ICU)، وبعد ذلك بعام قام إيبسن بإنشاء أول وحدة عناية مركزة متخصصة في العالم.[163]
لم يغير وباء شلل الأطفال من حياة أولئك الذين بقوا على قيد الحياة فحسب بل أحدث أيضًا تغيرات ثقافية عميقة وحفز الحركات الشعبية على حملات جمع الأموال التي من شأنها أن تُحدِث ثورة في العمل الخيري الطبي وتزيد من مجالات العلاج الفيزيائي، وبصفتهم أحد أكبر مجموعات المعاقين في العالم ساعد الناجون من شلل الأطفال أيضًا على تقدُّم حركة حقوق الإعاقة الحديثة من خلال حملات الحقوق الاجتماعية والمدنية للمعاقين، وتقدِّر منظمة الصحة العالمية أن هناك ما بين 10 إلى 20 مليون ناجٍ من شلل الأطفال في جميع أنحاء العالم[164]، ففي عام 1977 كان هناك 254 ألف شخص يعيشون في الولايات المتحدة مصابون بالشلل بسبب شلل الأطفال[165]، ووفقًا للأطباء ومجموعات دعم شلل الأطفال المحلية يعيش حوالي 40 ألفًا من الناجين من شلل الأطفال بدرجات متفاوتة من الشلل في ألمانيا، و30 ألفًا في اليابان و24 ألفًا في فرنسا و16 ألفًا في أستراليا، و12 ألفًا في كندا و12 ألفًا في المملكة المتحدة[164]، ومن الجدير بالملاحظة أنه نجا العديد من الأفراد من شلل الأطفال الذين غالبًا ما ينسبون التوقف المطوَّل والشلل المتبقي المرتبط بشلل الأطفال كقوة دافعة في حياتهم ومهنهم.[166] تم عمل ترويج إعلامي للمرض بشكل جيد للغاية خلال أوبئة شلل الأطفال في الخمسينات مع تغطية إعلامية واسعة لأي تطورات علمية قد تؤدي إلى الشفاء، وهكذا أصبح العلماء الذين يعملون على شلل الأطفال من أشهر العلماء في القرن، فتم تكريم خمسة عشر عالمًا واثنين من عامة الشعب الذين قدموا مساهمات مهمة في معرفة وعلاج شلل الأطفال من قبل صالة مشاهير شلل الأطفال التي تم تخصيصها في عام 1957 في معهد روزفلت وورم سبرينغز للتأهيل في وورم سبرينغز في جورجيا بالولايات المتحدة، وفي عام 2008 أضيفت أربع منظمات: منظمة الروتاري الدولية ومنظمة الصحة العالمية والمراكز الأمريكية لمكافحة الأمراض واليونيسيف إلى صالة مشاهير شلل الأطفال[167][168]، أدى استخدام لقاح فيروس شلل الأطفال المعطل والاستخدام واسع النطاق لاحقًا للقاح فيروس شلل الأطفال الفموي الذي طوره ألبرت سابين إلى إنشاء المبادرة العالمية للقضاء على شلل الأطفال (GPEI) في عام 1988، ومننذ ذلك الحين خفَّضَت المبادرة العالمية لحماية البيئة شلل الأطفال من جميع أنحاء العالم بنسبة 99%.[169]
اليوم العالمي لشلل الأطفال
جُعل اليوم العالمي لشلل الأطفال في الرابع والعشرين من أكتوبر من قبل منظمة الروتاري الدولية لإحياء ذكرى ولادة جوناس سولك الذي قاد الفريق الأول لتطوير لقاح ضد شلل الأطفال.[57]
علم الاشتقاق
المصطلح "polio" مشتق من كلمة "poliós" اليونانية القديمة والتي تعني «رمادي»، وكلمة "myelós" والتي تعني «نخاع» إشارةً إلى المادة الرمادية في الحبل الشوكي، واللاحقة -itis تُشير إلى الاتهاب[13]، بمعنى آخر: فإن مصطلح "Poliomyelitis" يعني التهاب المادة الرمادية في الحبل الشوكي بالرغم من أن العدوى الشديدة يمكن أن تمتد إلى جذع الدماغ وحتى الهياكل الأعلى مما يؤدي إلى التهاب شلل الأطفال.
الأبحاث
انطلقت مبادرة مضادات فيروسية للشلل الأطفال عام 2007 بهدف تطوير أدوية مضادة لفيروسات شلل الأطفال، ولكن في حين تم تحديد المرشحين الواعدين لم يتم إحراز أي تقدم بعد المرحلة الثانية من التجارب السريرية.[170][171] يمكن لبوكافير (مثبط القفيصة) وف-7404 (مثبط البروتياز) أن يُسرعا من عملية التخلص من الفيروس ولهذا فهما يخضعان للدراسة حاليًا.[172]
الهوامش
- «1» «قد يبدو أن تسعين طفلًا مصابًا -أو ما يقارب ذلك- عدد قليل، لكنهم ليسوا سوى مظهر ضئيل لمشكلة هائلة، حيث أن كل طفل يُصاب بالشلل يُمكن أن يتسبب في عدوى صامتة لما يصل إلى ألف آخرين. فشلل الأطفال معدي لدرجة أن حالة واحدة تعتبر حالة طوارئ صحية عامة. تسعون حالة يمكن أن تعني إصابة حوالي 90.000 شخص، فكل ناقل ينقل المرض بشكل غير مرئي للآخرين لأسابيع متتالية.»
المراجع
باللغة الإنجليزية
- مُعرِّف أنطولوجيا مرض: http://www.disease-ontology.org/?id=DOID:4953 — تاريخ الاطلاع: 15 مايو 2019 — الرخصة: CC0
- "Poliomyelitis"، Epidemiology and Prevention of Vaccine-Preventable Diseases (The Pink Book) (ط. 13th)، Washington DC: Public Health Foundation، 2015، (chap. 18)، مؤرشف من الأصل في 30 ديسمبر 2016.
- "Poliomyelitis Fact sheet N°114"، who.int، أكتوبر 2014، مؤرشف من الأصل في 18 أبريل 2017، اطلع عليه بتاريخ 3 نوفمبر 2014.
- "This page allows you to request a table with AFP/polio data"، WHO، مؤرشف من الأصل في 19 يونيو 2020، اطلع عليه بتاريخ 8 مارس 2019.
- "Post-Polio Syndrome Fact Sheet"، NIH، 16 أبريل 2014، مؤرشف من الأصل في 29 يوليو 2011، اطلع عليه بتاريخ 4 نوفمبر 2014.
- "Guidance to US Clinicians Regarding New WHO Polio Vaccination Requirements for Travel by Residents of and Long-term Visitors to Countries with Active Polio Transmission"، CDC، 2 يونيو 2014، مؤرشف من الأصل في 04 يونيو 2014، اطلع عليه بتاريخ 4 يونيو 2014.
- "GPEI-This Week"، مؤرشف من الأصل في 2 يوليو 2020، اطلع عليه بتاريخ 22 ديسمبر 2019.
- Daniel, Thomas M.؛ Robbins, Frederick C., المحررون (1999)، Polio (ط. 1st)، Rochester, N.Y.: University of Rochester Press، ص. 11، ISBN 9781580460668، مؤرشف من الأصل في 17 يونيو 2016.
- Wheeler, Derek S.؛ Wong, Hector R.؛ Shanley, Thomas P., المحررون (2009)، Science and practice of pediatric critical care medicine، London: Springer، ص. 10–11، ISBN 9781848009219، مؤرشف من الأصل في 17 يونيو 2016.
- Aylward R (2006)، "Eradicating polio: today's challenges and tomorrow's legacy"، Annals of Tropical Medicine and Parasitology، 100 (5–6): 401–13، doi:10.1179/136485906X97354، PMID 16899145.
- Alfred (06 أكتوبر 2011)، "Oct. 6, 1956: Sabin Polio Vaccine Ready to Test"، Wired، مؤرشف من الأصل في 22 ديسمبر 2016، اطلع عليه بتاريخ 21 مايو 2020.
- "Late functional loss in nonparalytic polio"، American Journal of Physical Medicine & Rehabilitation، 79 (1): 19–23، 2000، doi:10.1097/00002060-200001000-00006، PMID 10678598.
- The Gale Encyclopedia of Neurological Disorders، Detroit: Thomson Gale، 2005، ص. 1859–70، ISBN 978-0-7876-9150-9، مؤرشف من الأصل في 9 يوليو 2020.
- Leboeuf C (1992)، The late effects of Polio: Information For Health Care Providers. (PDF)، Commonwealth Department of Community Services and Health، ISBN 978-1-875412-05-1، مؤرشف من الأصل (PDF) في 25 يونيو 2008، اطلع عليه بتاريخ 23 أغسطس 2008.
- Manual of infantile paralysis, with modern methods of treatment.، Philadelphia Davis، 1914، ص. 79–101، OCLC 2078290، مؤرشف من الأصل في 9 يوليو 2020.
- Wood, Lawrence D. H.؛ Hall, Jesse B.؛ Schmidt, Gregory D. (2005)، Principles of Critical Care (ط. 3rd)، McGraw-Hill Professional، ص. 870، ISBN 978-0-07-141640-5، مؤرشف من الأصل في 6 أغسطس 2020.
- Cohen JI (2004)، "Chapter 175: Enteroviruses and Reoviruses"، في Kasper DL؛ Braunwald E؛ Fauci AS؛ وآخرون (المحررون)، Harrison's Principles of Internal Medicine (ط. 16th)، McGraw-Hill Professional، ص. 1144، ISBN 978-0-07-140235-4.
- "Enteroviruses"، Sherris Medical Microbiology (ط. 4th)، McGraw Hill، 2004، ص. 535–7، ISBN 978-0-8385-8529-0، مؤرشف من الأصل في 27 يوليو 2020.
- Katz, Samuel L.؛ Gershon, Anne A.؛ Krugman, Saul؛ Hotez, Peter J. (2004)، Krugman's infectious diseases of children، St. Louis: Mosby، ص. 81–97، ISBN 978-0-323-01756-5، مؤرشف من الأصل في 6 أغسطس 2020.
- "Member Sign In"، web.archive.org، 04 فبراير 2004، مؤرشف من الأصل في 18 أغسطس 2020، اطلع عليه بتاريخ 18 أغسطس 2020.
- "Vaccine-derived polioviruses and the endgame strategy for global polio eradication"، Annual Review of Microbiology، 59: 587–635، 2005، doi:10.1146/annurev.micro.58.030603.123625، PMID 16153180، مؤرشف من الأصل في 9 يوليو 2020.
- "Nonpoliovirus poliomyelitis simulating Guillain–Barré syndrome"، Archives of Neurology، 58 (9): 1460–64، سبتمبر 2001، doi:10.1001/archneur.58.9.1460، PMID 11559319.
- Parker SP, المحرر (1998)، McGraw-Hill Concise Encyclopedia of Science & Technology، New York: McGraw-Hill، ص. 67، ISBN 978-0-07-052659-4، مؤرشف من الأصل في 6 أغسطس 2020.
- Racaniello V (2006)، "One hundred years of poliovirus pathogenesis"، Virology، 344 (1): 9–16، doi:10.1016/j.virol.2005.09.015، PMID 16364730.
- "Chronic progressive poliomyelitis secondary to vaccination of an immunodeficient child"، نيو إنغلاند جورنال أوف ميديسين، 297 (5): 241–45، 1977، doi:10.1056/NEJM197708042970503، PMID 195206.
- Chandra R (14 يونيو 1975)، "Reduced secretory antibody response to live attenuated measles and poliovirus vaccines in malnourished children"، المجلة الطبية البريطانية، 2 (5971): 583–85، doi:10.1136/bmj.2.5971.583، PMC 1673535، PMID 1131622.
- Horstmann D (1950)، "Acute poliomyelitis relation of physical activity at the time of onset to the course of the disease"، دورية الجمعية الطبية الأمريكية، 142 (4): 236–41، doi:10.1001/jama.1950.02910220016004، PMID 15400610.
- "Mechanism of Injury-Provoked Poliomyelitis"، Journal of Virology، 72 (6): 5056–60، 1998، doi:10.1128/JVI.72.6.5056-5060.1998، PMC 110068، PMID 9573275.
- Evans C (1960)، "Factors influencing the occurrence of illness during naturally acquired poliomyelitis virus infections" (PDF)، Bacteriological Reviews، 24 (4): 341–52، doi:10.1128/MMBR.24.4.341-352.1960، PMC 441061، PMID 13697553، مؤرشف من الأصل (PDF) في 21 يونيو 2007.
- Chapter 26:Poliomyelitis. in: Immunisation Against Infectious Disease, 2006 (PDF)، Edinburgh: Stationery Office [الإنجليزية]، 2006، ص. 313–29، ISBN 978-0-11-322528-6، مؤرشف من الأصل في 26 مارس 2009، اطلع عليه بتاريخ 09 مارس 2007.
- "Antibodies against vaccine-preventable diseases in pregnant women and their offspring in the eastern part of Germany"، Medical Microbiology and Immunology، 190 (4): 167–72، 2002، doi:10.1007/s00430-001-0100-3، PMID 12005329، مؤرشف من الأصل في 11 يوليو 2020.
- "Complexes of Poliovirus Serotypes with Their Common Cellular Receptor, CD155"، Journal of Virology، 77 (8): 4827–35، 2003، doi:10.1128/JVI.77.8.4827-4835.2003، PMC 152153، PMID 12663789.
- Baron S؛ وآخرون, المحررون (1996)، "Picornaviruses: The Enteroviruses: Polioviruses"، Baron's Medical Microbiology (ط. 4th)، Univ of Texas Medical Branch، ISBN 978-0-9631172-1-2، مؤرشف من الأصل في 07 ديسمبر 2008.
- "Al-Qamoos القاموس | English Arabic dictionary / قاموس إنجليزي عربي"، www.alqamoos.org، مؤرشف من الأصل في 9 يوليو 2020، اطلع عليه بتاريخ 08 يوليو 2020.
- Todar K (2006)، "Polio"، Ken Todar's Microbial World، University of Wisconsin – Madison، مؤرشف من الأصل في 27 أبريل 2010، اطلع عليه بتاريخ 23 أبريل 2007.
- Sabin A (1956)، "Pathogenesis of poliomyelitis; reappraisal in the light of new data"، ساينس، 123 (3209): 1151–57، Bibcode:1956Sci...123.1151S، doi:10.1126/science.123.3209.1151، PMID 13337331.
- "Poliovirus and poliomyelitis: a tale of guts, brains, and an accidental event"، Virus Research، 111 (2): 175–93، 2005، doi:10.1016/j.virusres.2005.04.008، PMID 15885840.
- Polio، Diseases and People، Berkeley Heights, NJ: Enslow Publishers، 2001، ص. 12، ISBN 978-0-7660-1592-0، مؤرشف من الأصل في 9 يوليو 2020.
- "Post-polio syndrome: pathophysiology and clinical management"، Critical Review in Physical Medicine and Rehabilitation، 7 (2): 147–88، 1995، doi:10.1615/CritRevPhysRehabilMed.v7.i2.40، مؤرشف من الأصل في 30 يونيو 2016، اطلع عليه بتاريخ 30 يونيو 2016. Reproduced online with permission by Lincolnshire Post-Polio Library; retrieved on 10 November 2007.
- Young GR (1989)، "Occupational therapy and the postpolio syndrome"، The American Journal of Occupational Therapy، 43 (2): 97–103، doi:10.5014/ajot.43.2.97، PMID 2522741، مؤرشف من الأصل في 11 أغسطس 2007.
- "The epidemiology of poliomyelitis: enigmas surrounding its appearance, epidemicity, and disappearance"، American Journal of Epidemiology، 110 (6): 672–92، 1979، doi:10.1093/oxfordjournals.aje.a112848، PMID 400274.
- Karp, Dr. (18 مارس 2005)، "A photomicrograph of the thoracic spinal cord depicting degenerative changes due to Polio Type III."، Public Health Image Library (PHIL)، Centers for Disease Control and Prevention، مؤرشف من الأصل في 2 فبراير 2014، اطلع عليه بتاريخ 24 يناير 2014.
- Wallace, Gregory S؛ Oberste (13 أبريل 2013)، "Chapter 12: Poliomyelitis"، Manual for the Surveillance of Vaccine-Preventable Diseases (5th Edition, 2012)، Centers for Disease Control and Prevention، مؤرشف من الأصل في 28 يناير 2014، اطلع عليه بتاريخ 24 يناير 2014.
- Professional Guide to Diseases (Professional Guide Series)، Hagerstown, MD: Lippincott Williams & Wilkins، 2005، ص. 243–45، ISBN 978-1-58255-370-2، مؤرشف من الأصل في 9 يوليو 2020.
- Hoyt, William Graves؛ Miller, Neil؛ Walsh, Frank (2005)، Walsh and Hoyt's clinical neuro-ophthalmology، Hagerstown, MD: Lippincott Williams & Wilkins، ص. 3264–65، ISBN 978-0-7817-4814-8.
- "Case definitions for infectious conditions under public health surveillance. Centers for Disease Control and Prevention" (PDF)، Morbidity and Mortality Weekly Report، 46 (RR–10): 26–27، 1997، PMID 9148133، مؤرشف من الأصل (PDF) في 10 أغسطس 2009، اطلع عليه بتاريخ 11 نوفمبر 2007.
- Chezzi C (يوليو 1996)، "Rapid diagnosis of poliovirus infection by PCR amplification"، Journal of Clinical Microbiology، 34 (7): 1722–25، doi:10.1128/JCM.34.7.1722-1725.1996، PMC 229102، PMID 8784577.
- Gawande A (12 يناير 2004)، "The mop-up: eradicating polio from the planet, one child at a time"، النيويوركر: 34–40، ISSN 0028-792X.
- Rinaldo, Charles R. (2005-05)، "Passive Immunization Against Poliomyelitis"، American Journal of Public Health، 95 (5): 790–799، ISSN 0090-0036، مؤرشف من الأصل في 5 يناير 2019، اطلع عليه بتاريخ https://ajph.aphapublications.org/doi/10.2105/AJPH.2004.040790.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ الوصول=و|تاريخ=(مساعدة)، روابط خارجية في|تاريخ الوصول= - "Evaluation of Red Cross gamma globulin as a prophylactic agent for poliomyelitis. 5. Reanalysis of results based on laboratory-confirmed cases"، Journal of the American Medical Association، 156 (1): 21–27، 1954، doi:10.1001/jama.1954.02950010023009، PMID 13183798.
- Rinaldo, Charles R. (2005-05)، "Passive Immunization Against Poliomyelitis: The Hammon Gamma Globulin Field Trials, 1951–1953"، American Journal of Public Health (باللغة الإنجليزية)، 95 (5): 790–799، doi:10.2105/AJPH.2004.040790، ISSN 0090-0036، مؤرشف من الأصل في 9 يوليو 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Fine, Paul E. M.؛ Carneiro (15 نوفمبر 1999)، "Transmissibility and Persistence of Oral Polio Vaccine Viruses: Implications for the Global Poliomyelitis Eradication Initiative"، American Journal of Epidemiology (باللغة الإنجليزية)، 150 (10): 1001–1021، doi:10.1093/oxfordjournals.aje.a009924، ISSN 0002-9262، مؤرشف من الأصل في 7 يوليو 2020.
- "Arquivo.pt"، arquivo.pt، مؤرشف من الأصل في 11 أكتوبر 2017، اطلع عليه بتاريخ 07 يوليو 2020.
- "Vaccination, vaccines against poliomyelitis: injectable vaccine Jonas Salk oral vaccine Albert Sabin"، web.archive.org، 07 أكتوبر 2007، مؤرشف من الأصل في 3 أبريل 2020، اطلع عليه بتاريخ 07 يوليو 2020.
- Spice B (4 أبريل 2005)، "Tireless polio research effort bears fruit and indignation"، The Salk vaccine: 50 years later/ second of two parts، Pittsburgh Post-Gazette، مؤرشف من الأصل في 05 سبتمبر 2008، اطلع عليه بتاريخ 23 أغسطس 2008.
- Kew, Olen M.؛ Sutter؛ de Gourville؛ Dowdle؛ Pallansch (01 أكتوبر 2005)، "Vaccine-Derived Polioviruses and the Endgame Strategy for Global Polio Eradication *"، doi:10.1146/annurev.micro.58.030603.123625، مؤرشف من الأصل في 20 أبريل 2020.
{{استشهاد بدورية محكمة}}: Cite journal requires|journal=(مساعدة) - "Pinkbook | Home | Epidemiology of Vaccine Preventable Diseases | CDC"، www.cdc.gov (باللغة الإنجليزية)، 25 سبتمبر 2019، مؤرشف من الأصل في 19 يونيو 2020، اطلع عليه بتاريخ 07 يوليو 2020.
- Sabin, A. B.؛ Boulger (01 يناير 1973)، "History of Sabin attenuated poliovirus oral live vaccine strains"، Journal of Biological Standardization (باللغة الإنجليزية)، 1 (2): 115–118، doi:10.1016/0092-1157(73)90048-6، ISSN 0092-1157، مؤرشف من الأصل في 13 مارس 2013.
- Sabin, Albert B.؛ Ramos-Alvarez؛ Alvarez-Amezquita؛ Pelon؛ Michaels؛ Spigland؛ Koch؛ Barnes؛ Rhim (06 أغسطس 1960)، "LIVE, ORALLY GIVEN POLIOVIRUS VACCINE: EFFECTS OF RAPID MASS IMMUNIZATION ON POPULATION UNDER CONDITIONS OF MASSIVE ENTERIC INFECTION WITH OTHER VIRUSES"، JAMA (باللغة الإنجليزية)، 173 (14): 1521–1526، doi:10.1001/jama.1960.03020320001001، ISSN 0098-7484، مؤرشف من الأصل في 2 مايو 2020.
- "Pinkbook | Home | Epidemiology of Vaccine Preventable Diseases | CDC"، web.archive.org، 30 ديسمبر 2016، مؤرشف من الأصل في 2 أبريل 2020، اطلع عليه بتاريخ 07 يوليو 2020.
- "A Science Odyssey: People and Discoveries: Salk produces polio vaccine"، www.pbs.org، مؤرشف من الأصل في 1 يوليو 2020، اطلع عليه بتاريخ 07 يوليو 2020.
- "Poliomyelitis prevention: recommendations for use of inactivated poliovirus vaccine and live oral poliovirus vaccine. American Academy of Pediatrics Committee on Infectious Diseases"، Pediatrics، 99 (2): 300–305، 1997-02، doi:10.1542/peds.99.2.300، ISSN 1098-4275، PMID 9024465، مؤرشف من الأصل في 7 يوليو 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Racaniello, Vincent R. (05 يناير 2006)، "One hundred years of poliovirus pathogenesis"، Virology، Virology 50th Anniversary Issue (باللغة الإنجليزية)، 344 (1): 9–16، doi:10.1016/j.virol.2005.09.015، ISSN 0042-6822، مؤرشف من الأصل في 8 يناير 2019.
- "Eradication of polio – Is Syria being left behind? / School of Public Health and Community Medicine"، مؤرشف من الأصل في 8 يناير 2020، اطلع عليه بتاريخ 15 أغسطس 2020.
- "WHO | Vaccines for routine use"، web.archive.org، 06 يونيو 2008، مؤرشف من الأصل في 18 أغسطس 2020، اطلع عليه بتاريخ 18 أغسطس 2020.
- Daniel, Thomas M.؛ Robbins, Frederick C. (1997)، Polio، Rochester, NY: University of Rochester Press، ص. 8–10، ISBN 978-1-58046-066-8.
- Goldberg A (2002)، "Noninvasive mechanical ventilation at home: building upon the tradition"، Chest، 121 (2): 321–4، doi:10.1378/chest.121.2.321، PMID 11834636.
- Neumann, Donald A. (2004-08)، "Polio: its impact on the people of the United States and the emerging profession of physical therapy"، The Journal of Orthopaedic and Sports Physical Therapy، 34 (8): 479–492، doi:10.2519/jospt.2004.0301، ISSN 0190-6011، PMID 15373011، مؤرشف من الأصل في 7 يوليو 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Neumann D (2004)، "Polio: its impact on the people of the United States and the emerging profession of physical therapy" (PDF)، The Journal of Orthopaedic and Sports Physical Therapy، 34 (8): 479–92، doi:10.2519/jospt.2004.0301، PMID 15373011، مؤرشف من الأصل (PDF) في 10 سبتمبر 2008، اطلع عليه بتاريخ 10 يوليو 2020. Reproduced online with permission by Post-Polio Health International; retrieved on 10 November 2007.
- "Motor Neuron Disease: ALS, Polio, Postpoliomyelitis"، web.archive.org، 12 أكتوبر 2007، مؤرشف من الأصل في 10 يوليو 2020، اطلع عليه بتاريخ 07 يوليو 2020.
- Mueller, Steffen؛ Wimmer؛ Cello (01 أغسطس 2005)، "Poliovirus and poliomyelitis: A tale of guts, brains, and an accidental event"، Virus Research، Replication strategies of neurotropic viruses and influence on cellular functions (باللغة الإنجليزية)، 111 (2): 175–193، doi:10.1016/j.virusres.2005.04.008، ISSN 0168-1702، مؤرشف من الأصل في 8 يوليو 2020.
- Alvin؛ Silverstein؛ Nunn (2001)، Polio، Berkeley Heights, NJ, USA : Enslow Publishers، مؤرشف من الأصل في 10 يوليو 2020.
- Goldberg, Allen I. (2002-02)، "Noninvasive mechanical ventilation at home: building upon the tradition"، Chest، 121 (2): 321–324، doi:10.1378/chest.121.2.321، ISSN 0012-3692، PMID 11834636، مؤرشف من الأصل في 10 يوليو 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - "Pinkbook | Polio | Epidemiology of Vaccine Preventable Diseases | CDC"، www.cdc.gov (باللغة الإنجليزية)، 25 سبتمبر 2019، مؤرشف من الأصل في 17 يونيو 2020، اطلع عليه بتاريخ 07 يوليو 2020.
- Miller, A. H.؛ Buck (1950-01)، "Tracheotomy in bulbar poliomyelitis"، California Medicine، 72 (1): 34–36، ISSN 0008-1264، PMID 15398892، مؤرشف من الأصل في 8 يوليو 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - "Constructivist Medicine"، مؤرشف من الأصل في 7 فبراير 2012، اطلع عليه بتاريخ 15 أغسطس 2020.
- Manual of infantile paralysis, with modern methods of treatment.، Philadelphia Davis، 1914، ص. 79–101، OCLC 2078290، مؤرشف من الأصل في 17 أغسطس 2020.
- "Comparison between concentric needle EMG and macro EMG in patients with a history of polio"، Clinical Neurophysiology، 110 (11): 1900–08، 1999، doi:10.1016/S1388-2457(99)00150-9، PMID 10576485، مؤرشف من الأصل في 20 أغسطس 2020.
- Neumann, Donald A. (01 أغسطس 2004)، "Historical Perspective—Polio: Its Impact on the People of the United States and the Emerging Profession of Physical Therapy"، Journal of Orthopaedic & Sports Physical Therapy، 34 (8): 479–492، doi:10.2519/jospt.2004.0301، ISSN 0190-6011، مؤرشف من الأصل في 1 يونيو 2018.
- Cashman, Neil R.؛ Covault؛ Wollman؛ Sanes (1987)، "Neural cell adhesion molecule in normal, denervated, and myopathic human muscle"، Annals of Neurology (باللغة الإنجليزية)، 21 (5): 481–489، doi:10.1002/ana.410210512، ISSN 1531-8249، مؤرشف من الأصل في 8 يوليو 2020.
- Agre, James C.؛ Rodriquez؛ Tafel (1991-10)، "Late effects of polio: Critical review of the literature on neuromuscular function"، Archives of Physical Medicine and Rehabilitation، 72 (11): 923–931، doi:10.1016/0003-9993(91)90013-9، ISSN 0003-9993، مؤرشف من الأصل في 8 يوليو 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Trojan, Daria A.؛ Cashman (2005)، "Post-poliomyelitis syndrome"، Muscle & Nerve (باللغة الإنجليزية)، 31 (1): 6–19، doi:10.1002/mus.20259، ISSN 1097-4598، مؤرشف من الأصل في 8 يونيو 2018.
- Gawne, Anne Carrington؛ Halstead (1995)، "Post-Polio Syndrome: Pathophysiology and Clinical Management"، Critical Reviews™ in Physical and Rehabilitation Medicine (باللغة الإنجليزية)، 7 (2)، doi:10.1615/CritRevPhysRehabilMed.v7.i2.40، ISSN 0896-2960، مؤرشف من الأصل في 7 يوليو 2020.
- "Poliomyelitis virus (picornavirus, enterovirus), after-effects of the polio, paralysis, deformations"، web.archive.org، 07 أكتوبر 2007، مؤرشف من الأصل في 10 يوليو 2020، اطلع عليه بتاريخ 18 أغسطس 2020.
- "Poliomyelitis virus (picornavirus, enterovirus), after-effects of the polio, paralysis, deformations"، web.archive.org، 07 أكتوبر 2007، مؤرشف من الأصل في 10 يوليو 2020، اطلع عليه بتاريخ 07 يوليو 2020.
- "Polio - Symptoms and causes"، Mayo Clinic (باللغة الإنجليزية)، مؤرشف من الأصل في 5 مايو 2020، اطلع عليه بتاريخ 07 يوليو 2020.
- "Post-Polio Syndrome Fact Sheet: National Institute of Neurological Disorders and Stroke (NINDS)"، مؤرشف من الأصل في 29 يوليو 2011، اطلع عليه بتاريخ 2 أغسطس 2011.
- Ramlow, J.؛ Alexander؛ LaPorte؛ Kaufmann؛ Kuller (01 أكتوبر 1992)، "Epidemiology of the post-polio syndrome"، American Journal of Epidemiology، 136 (7): 769–786، doi:10.1093/aje/136.7.769، ISSN 0002-9262، PMID 1442743، مؤرشف من الأصل في 7 يوليو 2020.
- Lin, K. H.؛ Lim (2005-08)، "Post-poliomyelitis syndrome: case report and review of the literature"، Annals of the Academy of Medicine, Singapore، 34 (7): 447–449، ISSN 0304-4602، PMID 16123820، مؤرشف من الأصل في 8 يوليو 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - "Polio Case Count"، منظمة الصحة العالمية، 27 ديسمبر 2017، مؤرشف من الأصل في 16 أغسطس 2014، اطلع عليه بتاريخ 27 ديسمبر 2017.
- "Polio This Week"، Global Polio Eradication Initiative، مؤرشف من الأصل في 8 يوليو 2020، اطلع عليه بتاريخ 16 مايو 2019.
- Vaught (10 أبريل 2015)، "Polio Vaccine Celebrates 60th Anniversary"، Rotary International، مؤرشف من الأصل في 17 نوفمبر 2015، اطلع عليه بتاريخ 11 نوفمبر 2015.
- Centers for Disease Control and Prevention (CDC) (2006)، "Update on vaccine-derived polioviruses"، MMWR. Morbidity and Mortality Weekly Report، 55 (40): 1093–97، PMID 17035927.
- Centers for Disease Control and Prevention (CDC) (مايو 2008)، "Progress toward interruption of wild poliovirus transmission – worldwide, January 2007 – April 2008"، MMWR. Morbidity and Mortality Weekly Report، 57 (18): 489–94، PMID 18463607، مؤرشف من الأصل في 19 يونيو 2017.
- World Health Assembly (2012)، Poliomyelitis: intensification of the global eradication initiative. Agenda item A65/20 (PDF)، Geneva, Switzerland: World Health Organization، مؤرشف من الأصل (PDF) في 09 نوفمبر 2013، اطلع عليه بتاريخ 7 ديسمبر 2013.
- "WHO South-East Asia Region certified polio-free"، WHO، 27 مارس 2014، مؤرشف من الأصل في 27 مارس 2014، اطلع عليه بتاريخ 27 مارس 2014.
- "Wild poliovirus type 1 and Circulating vaccine-derived poliovirus cases"، Global Polio Eradication Initiative، 23 ديسمبر 2015، مؤرشف من الأصل في 24 ديسمبر 2015، اطلع عليه بتاريخ 26 ديسمبر 2015.
- "Progress Toward Poliomyelitis Eradication – Afghanistan and Pakistan, January 2011 – August 2012"، CDC، Centers for Disease Control and Prevention، 19 أكتوبر 2012، مؤرشف من الأصل في 12 ديسمبر 2013، اطلع عليه بتاريخ 7 ديسمبر 2013.
- Fine PEM (2009)، "Polio: Measuring the protection that matters most"، Journal of Infectious Diseases، 200 (5): 673–675، doi:10.1086/605331، PMID 19624277.
- Wild Poliovirus case list 2000-2010; data in WHO/HQ as of 9 November 2010 "Emergency appeal for Congo polio outbreak"، مؤرشف من الأصل في 22 ديسمبر 2010، اطلع عليه بتاريخ 17 نوفمبر 2010.
- Akst (1 يوليو 2015)، "Driven to Extinction"، The Scientist، مؤرشف من الأصل في 18 نوفمبر 2015، اطلع عليه بتاريخ 11 نوفمبر 2015.
- "Smallpox"، WHO Factsheet، مؤرشف من الأصل في 21 سبتمبر 2007، اطلع عليه بتاريخ 23 أغسطس 2008.
- "No more deaths from rinderpest"، OIE، 25 مايو 2011، مؤرشف من الأصل في 24 سبتمبر 2015، اطلع عليه بتاريخ 11 نوفمبر 2015.
- Olen M. Kew؛ Peter F. Wright؛ Vadim I. Agol؛ Francis Delpeyroux؛ Hiroyuki Shimizu؛ Neal Nathanson؛ Mark A. Pallansch (2004)، "Circulating vaccine-derived polioviruses: current state of knowledge"، Bulletin of the World Health Organization، 82 (1): 16–23، PMC 2585883، PMID 15106296، مؤرشف من الأصل في 1 يناير 2020.
- "The decade of the last recorded case of paralytic polio by country"، Our World in Data، مؤرشف من الأصل في 13 مايو 2020، اطلع عليه بتاريخ 4 مارس 2020.
- "Afghanistan polio: First case in Kabul since 2001"، BBC News، 11 فبراير 2014، مؤرشف من الأصل في 09 أبريل 2015.
- "Nigeria marks polio-free year, raising global eradication hopes"، Reuters، 23 يوليو 2015، مؤرشف من الأصل في 19 نوفمبر 2015.
- Polio in Afghanistan: 'Americans bomb our children daily, why would they care?' | Global health | The Guardian نسخة محفوظة 18 مارس 2020 على موقع واي باك مشين.
- "Nine polio cases confirmed in 2018"، Dawn، مؤرشف من الأصل في 7 يوليو 2020.
- "Pakistan could beat polio in months, says WHO"، BBC News، 16 مايو 2016، مؤرشف من الأصل في 16 مايو 2016، اطلع عليه بتاريخ 16 مايو 2016.
- Taimur Khan، "Pakistan's fight against polio clashes with battle against Taliban – The National"، مؤرشف من الأصل في 28 سبتمبر 2015.
- "Nationwide polio campaign starts today"، Dawn، 10 ديسمبر 2018، مؤرشف من الأصل في 6 يوليو 2020،
It shows that the number of annual polio cases has decreased by 97 per cent from 306 reported in 2014.
- The National staff (18 أبريل 2015)، "UAE polio campaign vaccinates millions of Pakistani children"، مؤرشف من الأصل في 10 سبتمبر 2015.
- The National staff، "17 million children to be vaccinated against polio in Pakistan"، مؤرشف من الأصل في 10 سبتمبر 2015.
- "Polio in Pakistan: Drop of 70% recorded this year"، BBC News، 03 يونيو 2015، مؤرشف من الأصل في 04 يونيو 2015.
- Centers for Disease Control and Prevention (CDC) (1994)، "International Notes Certification of Poliomyelitis Eradication – the Americas, 1994"، MMWR. Morbidity and Mortality Weekly Report، 43 (39): 720–22، PMID 7522302، مؤرشف من الأصل في 21 مايو 2017.
- Polio Declared Eliminated from the Americas | History of Vaccines نسخة محفوظة 9 يوليو 2020 على موقع واي باك مشين.
- "General News. Major Milestone reached in Global Polio Eradication: Western Pacific Region is certified Polio-Free"، Health Education Research، 16 (1): 109–114، 2001، Bibcode:2001PDiff..16..110Y، doi:10.1093/her/16.1.109.
- "Australia declared polio free"، Communicable Diseases Intelligence، 26 (2): 253–60، 2002، PMID 12206379.
- "New polio outbreak hits China - CNN.com"، CNN، 21 سبتمبر 2011، مؤرشف من الأصل في 01 يناير 2012.
- "Europe achieves historic milestone as Region is declared polio-free" (Press release)، European Region of the World Health Organization، 21 يونيو 2002، مؤرشف من الأصل في 16 سبتمبر 2008، اطلع عليه بتاريخ 23 أغسطس 2008.
- "Circulating vaccine-derived poliovirus – Ukraine"، World Health Organization، 1 سبتمبر 2015، مؤرشف من الأصل في 08 سبتمبر 2015، اطلع عليه بتاريخ 9 سبتمبر 2015.
- "Polio-free certification: WHO South-East Asia"، WHO، 27 مارس 2014، مؤرشف من الأصل في 27 مارس 2014، اطلع عليه بتاريخ 27 مارس 2014.
- Ray, Kalyan (26 فبراير 2012)، "India wins battle against dreaded polio"، Deccan Herald.
- "India polio-free for a year: 'First time in history we're able to put up such a map'"، The Telegraph، Calcutta, India، 26 فبراير 2012، مؤرشف من الأصل في 27 فبراير 2012، اطلع عليه بتاريخ 26 فبراير 2012.
- "Malaysia Reports First Case of Polio in 27 Years"، صوت أمريكا، أسوشيتد برس، 09 ديسمبر 2019، مؤرشف من الأصل في 8 يناير 2020، اطلع عليه بتاريخ 10 ديسمبر 2019.
- "Malaysia reports first case of polio since 1992"، رويترز، 8 ديسمبر 2019، مؤرشف من الأصل في 2 يناير 2020، اطلع عليه بتاريخ 10 ديسمبر 2019.
- "WHO | Polio outbreak– The Philippines"، WHO، مؤرشف من الأصل في 3 يوليو 2020، اطلع عليه بتاريخ 18 نوفمبر 2019.
- "Massive vaccine campaign underway in the Philippines after polio's return"، Public Radio International (باللغة الإنجليزية)، مؤرشف من الأصل في 12 يونيو 2020، اطلع عليه بتاريخ 19 نوفمبر 2019.
- Crisostomo (06 نوفمبر 2019)، "DOH confirms Philippine's 4th polio case"، The Philippine Star، مؤرشف من الأصل في 12 ديسمبر 2019، اطلع عليه بتاريخ 20 نوفمبر 2019.
- Arguilas (29 أكتوبر 2019)، "2 of 3 confirmed polio cases are from BARMM; 3rd is from Datu Piang"، MindaNews، مؤرشف من الأصل في 30 أكتوبر 2019، اطلع عليه بتاريخ 20 نوفمبر 2019.
- "Red Cross alarm over polio outbreak in Philippines after 19 years"، www.aljazeera.com، مؤرشف من الأصل في 9 فبراير 2020، اطلع عليه بتاريخ 21 نوفمبر 2019.
- "Philippines: Vaccine scare blamed for deadly measles outbreak"، www.aljazeera.com، مؤرشف من الأصل في 9 يونيو 2020، اطلع عليه بتاريخ 21 نوفمبر 2019.
- "Philippines: Worst dengue outbreak in years kills over a thousand"، www.aljazeera.com، مؤرشف من الأصل في 9 يونيو 2020، اطلع عليه بتاريخ 21 نوفمبر 2019.
- "WHO and UNICEF back the Department of Health in vaccinating 1.8 million children against polio"، www.unicef.org (باللغة الإنجليزية)، مؤرشف من الأصل في 11 يوليو 2020، اطلع عليه بتاريخ 18 نوفمبر 2019.
- "Embassy of the Republic of Indonesia in Manila, Accredited to the Republic of Marshall Islands and the Republic of Palau the Republic of the Philippines"، Kementerian Luar Negeri Repulik Indonesia (باللغة الإندونيسية)، مؤرشف من الأصل في 15 أغسطس 2019، اطلع عليه بتاريخ 19 نوفمبر 2019.
- Whewell (26 مارس 2014)، "Polio in Syria: An outbreak that threatens the Middle East"، BBC News، مؤرشف من الأصل في 03 يوليو 2015.
- "Syria polio cases spread to Damascus and Aleppo – WHO"، DNA، 26 نوفمبر 2013، مؤرشف من الأصل في 28 نوفمبر 2013، اطلع عليه بتاريخ 26 نوفمبر 2013.
- Sparrow, Annie (20 فبراير 2014)، "Syria's Polio Epidemic: The Suppressed Truth"، New York Review، مؤرشف من الأصل في 25 يناير 2014، اطلع عليه بتاريخ 23 يناير 2014.
- Debora MacKenzie، "Global emergency declared as polio cases surge"، New Scientist، مؤرشف من الأصل في 26 أبريل 2015.
- "World facing polio health emergency"، BBC، 05 مايو 2014، مؤرشف من الأصل في 06 مايو 2014، اطلع عليه بتاريخ 5 مايو 2014.
- Photographs Hosam Katan, Reuters (5 مارس 2015)، "Fighting Polio Amid the Chaos of Syria's Civil War"، مؤرشف من الأصل في 05 يناير 2016.
- Westall, Sylvia (28 يناير 2015)، "Polio immunisation rate in Syria close to pre-war level -WHO"، Reuters، مؤرشف من الأصل في 24 سبتمبر 2015.
- Gladstone, Rick (20 يونيو 2017)، "Polio Paralyzes 17 Children in Syria, W.H.O. Says"، New York Times، مؤرشف من الأصل في 6 يوليو 2020.
- "What Led to the Nigerian Boycott of the Polio Vaccination Campaign?"، NCBI، مؤرشف من الأصل في 31 أغسطس 2020، اطلع عليه بتاريخ 31 أغسطس 2020.
- "Nigeria polio vaccinators shot dead in Kano"، BBC News، 08 فبراير 2013، مؤرشف من الأصل في 28 ديسمبر 2014.
- "Nigeria marks one year without recorded polio case"، BBC News، 24 يوليو 2015، مؤرشف من الأصل في 24 يوليو 2015.
- "WHO Removes Nigeria from Polio-Endemic List"، منظمة الصحة العالمية، 26 سبتمبر 2015، مؤرشف من الأصل في 19 يناير 2016، اطلع عليه بتاريخ 8 يناير 2016.
- "Government of Nigeria reports 2 wild polio cases, first since July 2014"، WHO، 11 أغسطس 2016، مؤرشف من الأصل في 15 أغسطس 2016، اطلع عليه بتاريخ 15 أغسطس 2016.
- "Polio in Somalia, Kenya, Ethiopia"، 22 January 2014، Centers for Disease Control and Prevention، مؤرشف من الأصل في 02 فبراير 2014، اطلع عليه بتاريخ 23 يناير 2014.
- "Where We Work - Nigeria"، The Global Polio Eradication Initiative، 20 ديسمبر 2015، مؤرشف من الأصل في 5 يناير 2020، اطلع عليه بتاريخ 20 ديسمبر 2019.
- "Circulating vaccine-derived poliovirus in Mali"، The Global Polio Eradication Initiative، 09 سبتمبر 2015، مؤرشف من الأصل في 14 سبتمبر 2015، اطلع عليه بتاريخ 9 سبتمبر 2015.
- Herriman, Robert (25 مايو 2017)، "Polio update: Two circulating vaccine-derived poliovirus type 2 outbreaks reported in Democratic Republic of the Congo"، Outbreak News Today، مؤرشف من الأصل في 25 مايو 2017، اطلع عليه بتاريخ 25 مايو 2017.
- Scherbel-Ball, Naomi (25 أغسطس 2020)، "Africa declared free of polio"، BBC News (باللغة الإنجليزية)، مؤرشف من الأصل في 26 أغسطس 2020، اطلع عليه بتاريخ 25 أغسطس 2020.
- Paul JR (1971)، A History of Poliomyelitis، Yale studies in the history of science and medicine، New Haven, Conn: Yale University Press، ص. 16–18، ISBN 978-0-300-01324-5.
- Underwood, Michael (1789)، "Debility of the lower extremities"، A treatise on the diseases of children, with general directions for the management of infants from the birth (1789)، London: J. Mathews، ج. 2، ص. 88–91.
- Pearce J (2005)، "Poliomyelitis (Heine-Medin disease)"، Journal of Neurology, Neurosurgery, and Psychiatry، 76 (1): 128، doi:10.1136/jnnp.2003.028548، PMC 1739337، PMID 15608013.
- Robertson S (1993)، "Module 6: Poliomyelitis" (PDF)، The Immunological Basis for Immunization Series، World Health Organization. Geneva, Switzerland.، مؤرشف من الأصل (PDF) في 02 فبراير 2014، اطلع عليه بتاريخ 23 أغسطس 2008.
- "The Spatial Dynamics of Poliomyelitis in the United States: From Epidemic Emergence to Vaccine-Induced Retreat, 1910–1971"، Annals of the Association of American Geographers، 95 (2): 269–93، 2005، doi:10.1111/j.1467-8306.2005.00460.x، PMC 1473032، PMID 16741562.
- Melnick JL (1990)، Poliomyelitis. In: Tropical and Geographical Medicine (ط. 2nd)، McGraw-Hill، ص. 558–76، ISBN 978-0-07-068328-0.
- Zamula E (1991)، "A New Challenge for Former Polio Patients"، FDA Consumer، 25 (5): 21–25، مؤرشف من الأصل في 20 فبراير 2014.
- "Louise Reisner-Sénélar (2009) The Danish anaesthesiologist Björn Ibsen a pioneer of long-term ventilation on the upper airways"، مؤرشف من الأصل في 30 يناير 2012.
- Pincock S (2007)، Elsevier (المحرر)، "Bjørn Aage Ibsen"، The Lancet، 370 (9598): 1538، doi:10.1016/S0140-6736(07)61650-X، مؤرشف من الأصل في 17 أبريل 2014.
- "After Effects of Polio Can Harm Survivors 40 Years Later"، March of Dimes، 1 يونيو 2001، مؤرشف من الأصل في 25 ديسمبر 2014، اطلع عليه بتاريخ 14 نوفمبر 2014.
- "Post-polio sequelae: physiological and psychological overview"، Rehabilitation Literature، 47 (5–6): 106–11، 1986، PMID 3749588.
- Richard L. Bruno (2002)، The Polio Paradox: Understanding and Treating "Post-Polio Syndrome" and Chronic Fatigue، New York: Warner Books، ص. 105–06، ISBN 978-0-446-69069-0.
- Skinner, Winston (15 نوفمبر 2008)، "Four added to Polio Hall of Fame at Warm Springs"، The Times-Herald (Newnan, GA)، مؤرشف من الأصل في 28 مارس 2010، اطلع عليه بتاريخ 29 مايو 2009.
- "CDC Inducted into Polio Hall of Fame"، CDC in the News، 23 يناير 2009، مؤرشف من الأصل في 24 سبتمبر 2015، اطلع عليه بتاريخ أكتوبر 2020.
{{استشهاد بخبر}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - "Announcement: World Polio Day – 24 October 2012"، CDC، Centers for Disease Control and Prevention، 19 أكتوبر 2012، مؤرشف من الأصل في 12 ديسمبر 2013، اطلع عليه بتاريخ 7 ديسمبر 2013.
- Thibaut؛ De Palma؛ Neyts (15 يناير 2012)، "Combating enterovirus replication: state-of-the-art on antiviral research."، Biochemical Pharmacology، 83 (2): 185–92، doi:10.1016/j.bcp.2011.08.016، PMID 21889497.
- McKinlay؛ Collett؛ Hincks؛ Oberste؛ Pallansch؛ Okayasu؛ Sutter؛ Modlin؛ Dowdle (01 نوفمبر 2014)، "Progress in the development of poliovirus antiviral agents and their essential role in reducing risks that threaten eradication."، Journal of Infectious Diseases، 210 Suppl 1: S447–53، doi:10.1093/infdis/jiu043، PMID 25316866.
- "GPEI-Antivirals" (باللغة الإنجليزية)، مؤرشف من الأصل في 14 مارس 2019، اطلع عليه بتاريخ 14 مارس 2019.
باللغة العربية
- "ترجمة (Poliomyelitis) في القاموس."، موقع القاموس، 18 أغسطس 2020، مؤرشف من الأصل في 18 أغسطس 2020، اطلع عليه بتاريخ 18 أغسطس 2020.
- "منظمة الصحة العالمية | شلل الأطفال"، WHO، مؤرشف من الأصل في 20 أبريل 2020، اطلع عليه بتاريخ 10 يوليو 2020.
- "شلل الأطفال"، منظمة الصحة العالمية، مؤرشف من الأصل في 20 أبريل 2020، اطلع عليه بتاريخ 10 يوليو 2020.
- "شلل الأطفال وكيفية الوقاية منه"، Webteb، مؤرشف من الأصل في 24 مايو 2020، اطلع عليه بتاريخ 10 يوليو 2020.
- "أعراض وأسباب شلل الأطفال"، Mayo Clinic (مايو كلينك)، مؤرشف من الأصل في 13 مايو 2020، اطلع عليه بتاريخ 10 يوليو 2020.
وصلات خارجية
- بوابة تمريض
- بوابة طب
- بوابة علم الفيروسات
