فروسيانيد الصوديوم
فروسيانيد الصوديوم مركب تساندي له الصيغة Na4Fe(CN)6 ، ويكون على شكل بلورات عديمة اللون. ويوجد منه شكل مائي مرتبط مع عشر جزيئات ماء، بلوراته لها لون أصفر. فروسيانيد الصوديوم يعد ملح الصوديوم للمعقد الناتج عن تساند شوارد السيانيد السالبة (أنيونات) حول ذرة الحديد المركزية الموجبة.
| فروسيانيد الصوديوم | |
|---|---|
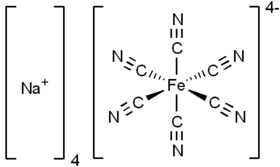 فروسيانيد الصوديوم | |
| الاسم النظامي (IUPAC) | |
سداسي سيانوفرّات رباعي صوديوم | |
| أسماء أخرى | |
فروسيانيد صوديوم | |
| المعرفات | |
| رقم CAS | 13601-19-9? 14434-22-1 (عشاري هيدرات) |
| بوب كيم | 26129 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| الخواص | |
| الصيغة الجزيئية | Na4Fe(CN)6 |
| الكتلة المولية | 303.91 غ/مول |
| المظهر | بلورات صفراء |
| الكثافة | 1.458 غ/سم3 |
| نقطة الانصهار | 435 °س يتفكك |
| الذوبانية في الماء | 31.8 غ/100 مل ماء |
| الذوبانية | منحل في الأسيتون غير منحل في الإيثانول والإيثر |
| المخاطر | |
| ترميز المخاطر |  Xn Xn |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
الخواص
- ينحل مركب فروسيانيد الصوديوم بشكل جيد في الماء، ينحل في الأسيتون لكنه غير منحل في الإيثانول وثنائي إيثيل الإيثر.
- يوجد على شكل عشاري هيدرات Na4Fe(CN)6 . 10H2O والذي يفقد ماءه البلوري بالتسخين فوق 81.5 °س، حيث يصبح عديم اللون.
التحضير
يحضر مركب فروسيانيد الصوديوم من تفاعل محلول فروسيانيد الكالسيوم مع كربونات الصوديوم، حيث يترسب لدينا كربونات الكالسيوم ويبقى فروسيانيد الصوديوم في المحلول الناتج حسب المعادلة:
Ca2[Fe(CN)6] + 2 Na2CO3 → Na4[Fe(CN)6] + 2 CaCO3
كما يحضر من تفاعل كلوريد الحديد الثنائي مع سيانيد الصوديوم حسب المعادلة:
6 NaCN + FeCl2 → Na4[Fe(CN)6] + 2 NaCl
الاستخدامات
- يضاف إلى ملح الطعام بتراكيز منخفضة من أجل منع التكتل. رقم الإي الخاص به E535 .
- يستعمل كاشفاً في الكيمياء التحليلية بالإضافة إلى أملاح الفروسيانيد الأخرى من أجل الكشف عن أيون الحديد الثلاثي Fe +3، حيث يتشكل معقد أزرق بروسيا.
مصادر
- موسوعة رومب الكيميائية Römpp Lexikon Chemie, Georg Thieme Verlag
مراجع
- العنوان : sodium hexacyanoferrate(4-) — الناشر: معهد المعلوماتية الحيوية الأوروبي — مُعرِّف الكيانات الكيميائيَّة ذات الأهمية الحيوية (ChEBI): https://www.ebi.ac.uk/chebi/searchId.do?chebiId=CHEBI:30061 — تاريخ الاطلاع: 5 أكتوبر 2016 — الرخصة: رخصة المشاع الإبداعي الملزمة بالنسب لمؤلف العمل غير القابلة للإلغاء 3.0
- العنوان : SODIUM FERROCYANIDE — مُعرِّف "بَب كِيم" (PubChem CID): https://pubchem.ncbi.nlm.nih.gov/compound/26129 — تاريخ الاطلاع: 14 أكتوبر 2016 — الرخصة: محتوى حر
- http://www.alfa-chemcat.com/daten_msds/D/39660_-_D.pdf%5Bوصلة+مكسورة%5D
- بوابة الكيمياء
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.