Adiponitrilo
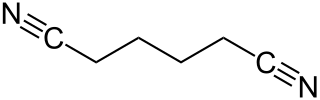
El adiponitrilo, llamado también hexanodinitrilo, 1,4-dicianobutano o 1,4-butanodicarbonitrilo,[2] es un compuesto orgánico de fórmula molecular C6H8N2, cuya estructura química corresponde a un dinitrilo lineal de seis átomos de carbono. Es un importante precursor del polímero nylon-6,6, alcanzando la producción mundial anual de adiponitrilo en 2005 los mil millones de kg.[3]
| Adiponitrilo | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| hexanodinitrilo | ||
| General | ||
| Otros nombres |
1,4-dicianobutano adipildinitrilo adipodinitrilo 1,4-butanodicarbonitrilo | |
| Fórmula semidesarrollada | N≡C-(CH2)4-C≡N | |
| Fórmula molecular | C6H8N2 | |
| Identificadores | ||
| Número CAS | 111-69-3[1] | |
| Número RTECS | AV2625000 | |
| ChEMBL | CHEMBL2132938 | |
| ChemSpider | 13876621 | |
| PubChem | 8128 | |
| UNII | SYT33B891I | |
|
C(CCC#N)CC#N
| ||
| Propiedades físicas | ||
| Apariencia | Líquido incoloro y aceitoso | |
| Olor | Inodoro | |
| Densidad | 951 kg/m³; 0,951 g/cm³ | |
| Masa molar | 10 814 g/mol | |
| Punto de fusión | 1 °C (274 K) | |
| Punto de ebullición | 295 °C (568 K) | |
| Presión de vapor | 0,002 mmHg | |
| Viscosidad | 9,1 cP | |
| Índice de refracción (nD) | 1,438 | |
| Propiedades químicas | ||
| Solubilidad en agua | 80 g/L | |
| log P | -0,32 | |
| Familia | Nitrilo | |
| Peligrosidad | ||
| Punto de inflamabilidad | 436,15 K (163 °C) | |
| NFPA 704 |
2
4
0
| |
| Temperatura de autoignición | 823 K (550 °C) | |
| Compuestos relacionados | ||
| nitrilos | hexanonitrilo | |
| dinitrilos |
glutaronitrilo heptanodinitrilo | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Propiedades físicas y químicas
A temperatura ambiente, el adiponitrilo es un líquido incoloro y prácticamente inodoro de aspecto aceitoso, cuya densidad es ligeramente menor que la del agua (0,951 g/cm³).[2] Su punto de ebullición es 295 °C mientras que su punto de fusión es de 1-2 °C.[4] En estado gaseoso, su densidad es 3,75 veces mayor que la del aire.[2]
Es un líquido soluble en metanol, etanol, cloroalcanos y compuestos aromáticos pero es poco soluble en disulfuro de carbono, éter etílico e hidrocarburos alifáticos. En agua, su solubilidad es de 80 g/L. El valor del logaritmo de su coeficiente de reparto, logP = -0,32, indica una solubilidad algo más elevada en disolventes polares como el agua que en octanol.[5] Su carácter aceitoso se pone de manifiesto en su viscosidad, 9,1 cP a 20 °C, nueve veces mayor que la del agua.[2]
En cuanto a su reactividad, el adiponitrilo es incompatible con oxidantes fuertes, ácidos fuertes, bases fuertes y agentes reductores fuertes.[6]
Síntesis
Rutas de síntesis antiguas
Debido al valor industrial del adiponitrilo, se han desarrollado muchas rutas para su síntesis. Las primeras rutas tenían como precursor al furfural pero más tarde se desarrolló la cloración del butadieno para obtener 1,4-dicloro-2-buteno, el cual con cianuro sódico se convierte en 3-hexenodinitrilo; la hidrogenación de este último forma el adiponitrilo:[3]
- ClCH2CH=CHCH2Cl + 2 NaCN → NCCH2CH=CHCH2CN + 2 NaCl
- NCCH2CH=CHCH2CN + H2 → NC(CH2)4CN
El adiponitrilo también se ha producido a partir de ácido adípico, por deshidratación de la diamida, pero esta vía es rara vez utilizada.
Rutas de síntesis modernas
En la actualidad, la mayor parte del adiponitrilo se obtiene por la hidrocianación del butadieno catalizada por níquel. William C. Drinkard en DuPont fue el primero en empezar a servirse de esta reacción:
- CH2=CHCH=CH2 + 2 HCN → NCCH2CH2CH2CH2CN

El proceso comprende varias etapas, siendo la primera de ellas la monohidrocianación —adición de una molécula de HCN—, riendiendo isómeros de pentenonitrilos así como 2- y 3-metilbutenonitrilo. Estos nitrilos insaturados con convertidos a 3- y 4-pentenonitrilo, los cuales, en la etapa final, son sometidos a una segunda hidrocianación, en sentido anti-Markovnikov, para producir adiponitrilo.[3]
Otra vía de síntesis industrial importante, descubierta en la Monsanto Company, implica electrosíntesis. En dicho proceso tiene lugar la dimerización del acrilonitrilo:
- 2 CH2=CHCN + 2 e− + 2 H+ → NCCH2CH2CH2CH2CN
Usos
La práctica totalidad de adiponitrilo producido es hidrogenado para conseguir 1,6-hexanodiamina, diamina empleada en la elaboración de nylon, de acuerdo a la reacción:[7]
- NC(CH2)4CN + 4 H2 → H2N(CH2)6NH2
Al igual que otros nitrilos, el adiponitrilo es susceptible de ser hidrolizado. No obstante, el ácido adípico resultante puede ser preparado de forma más barata por otras vías.
Precauciones
El adiponitrilo es un compuesto combustible que tiene su punto de inflamabilidad a 163 °C y su temperatura de autoignición a 550 °C. Al arder puede desprender cianuro de hidrógeno, compuesto sumamente tóxico. Asimismo, en un área cerrada su vapor puede explotar al entrar en contacto con fuego. Igualmente, cuando se calienta hasta su descomposición, emite humos extremadamente tóxicos.[2]
Este dinitrilo es tóxico tanto por ingestión como por inhalación, provocando trastornos en la respiración y en la circulación, irritación del estómago e intestino, así como pérdida de peso. Es también irritante en piel y ojos.[2][4]
Véase también
Los compuestos siguientes son también dinitrilos con seis átomos de carbono:
- 3-hexenodinitrilo
- 2-metilenglutaronitrilo
- 1-metil-1H-pirrol-2-carbonitrilo
- 3,3'-tiodipropionitrilo
Referencias
- Número CAS
- Adiponitrile (PubChem)
- M. T. Musser, "Adipic Acid" en Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. doi 269 10.1002/14356007.a01 269
- Hexanedinitrile (EPA)
- Adiponitrile (ChemSpider)
- 1,4-Dicyanobutane (Chemical Book)
- Robert A. Smiley "Hexamethylenediamine" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. doi 629 10.1002/14356007.a12 629
