Amikacina
La amikacina es un antibiótico del grupo de los aminoglucósidos que se usa para el tratamiento de diferentes infecciones bacterianas.[2] Esto incluye infecciones de las articulaciones, infecciones intraabdominales, meningitis, neumonía, sepsis e infecciones del tracto urinario.[3] También se utiliza para el tratamiento de la tuberculosis multirresistente.[4] La amikacina se inyecta por medio intravenoso (en la vena) o intramuscular (en el músculo).[3]
| Amikacina | ||
|---|---|---|
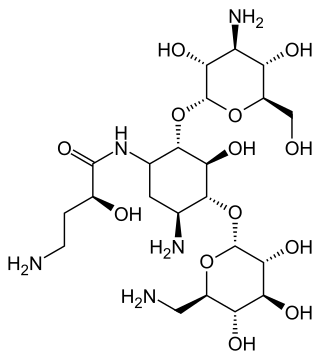 | ||
 | ||
| Nombre (IUPAC) sistemático | ||
|
(2S)-4-amino-N-[(2S,3S,4R,5S)-5-amino-2- [(2S,3R,4S,5S,6R)-4-amino-3,5-dihydroxy- 6-(hydroxymethyl)oxan-2-yl]oxy-4-[(2R,3R, 4S,5R,6R)-6-(aminomethyl)-3,4,5-trihydroxy- oxan-2-yl]oxy-3-hydroxy-cyclohexyl]-2-hydroxy- butanamide | ||
| Identificadores | ||
| Número CAS | 37517-28-5 | |
| Código ATC | D06AX12 J01GB06, S01AA21 | |
| PubChem | 37768 | |
| DrugBank | DB00479 | |
| ChemSpider | 34635 | |
| UNII | 84319SGC3C | |
| KEGG | D02543 | |
| ChEBI | 2637 | |
| ChEMBL | 177 | |
| Datos químicos | ||
| Fórmula | C22H43N5O13 | |
| Peso mol. | 585,6 g/mol | |
|
O=C(N[C@H]3[C@H](O[C@H]1O[C@@H]([C@@H](O)[C@H](N)[C@H]1O)CO)[C@@H](O)[C@H](O[C@H]2O[C@H](CN)[C@@H](O)[C@H](O)[C@H]2O)[C@@H](N)C3)[C@@H](O)CCN
| ||
|
InChI=1S/C22H43N5O13/c23-2-1-8(29)20(36)27-7-3-6(25)18(39-22-16(34)15(33)13(31)9(4-24)37-22)17(35)19(7)40-21-14(32)11(26)12(30)10(5-28)38-21/h6-19,21-22,28-35H,1-5,23-26H2,(H,27,36)/t6-,7+,8-,9+,10+,11-,12+,13+,14+,15-,16+,17-,18+,19-,21+,22+/m0/s1
Key: LKCWBDHBTVXHDL-RMDFUYIESA-N | ||
| Farmacocinética | ||
| Biodisponibilidad | >90%[1] | |
| Unión proteica | 0-11% | |
| Metabolismo | Por mayor parte no metabolizado | |
| Vida media | 2-3 horas | |
| Excreción | renal | |
| Datos clínicos | ||
| Nombre comercial | Amikin, Amiglyde-V, otros | |
| Cat. embarazo | D (AU) Evidencia de riesgo para el feto, aunque el beneficio potencial de su uso en embarazadas puede ser aceptable a pesar del riesgo probable solo en algunas situaciones. Queda a criterio del médico tratante. (EUA) | |
| Estado legal | POM (UK) ℞-only (EUA) | |
| Vías de adm. | Inyección intramuscular o intravenosa | |
La amikacina, al igual que los demás antibióticos aminoglucósidos, puede causar pérdida de audición, problemas de equilibrio y problemas de riñón. Otros efectos secundarios incluyen la parálisis, que puede llevar a la incapacidad para respirar. Si se utiliza durante el embarazo puede causar sordera permanente en el bebé. La amikacina produce el bloqueo de la función de la subunidad menor del ribosoma procariótico, que incapacita a la bacteria para producir proteínas.[3]
La amikacina fue patentada en 1971 y entró en el mercado en 1976.[5][6] Está en la lista de medicamentos esenciales de la Organización Mundial de la Salud.[7] El coste mayorista en el mundo en desarrollo es 11 a 106 € (258 a 2,436 MXN) al mes.[8]
Farmacocinética
La Amikacina no se absorbe oralmente, por lo que su vía de administración es parenteral. Su concentración máxima en suero se logra en 0.5-2 horas cuando se administra intramuscularmente. Menos del 11% de amikacina se une a proteínas de plasma. Está distribuido al corazón, la vesícula biliar, los pulmones y los huesos, así como en bilis, esputo, líquido intersticial, líquido pleural y líquido sinovial. Está en concentraciones bajas en el líquido cefalorraquídeo, excepto cuando se administra de manera intraventricular.[3] En los infantes, la amikacina está en 10-20% de niveles del suero en el líquido cefalorraquídeo, pero aumenta a 50% en casos de meningitis.[11] No cruza fácilmente la barrera hematoencefálica en el cerebro o entra en el tejido ocular.[1]
Mientras la vida media de la amikacina es normalmente de 2 horas, para personas con enfermedad renal terminal puede llegar hasta 50 horas.[11]
La mayoría (95%) de la amikacina introducida de manera IM o IV se excreta sin cambios por filtración glomerular y sale en la orina dentro 24 horas.[3][12] Los factores que causan la excreción de amikacina por vía urinaria incluyen su relativamente bajo peso molecular, alta solubilidad en agua y por no ser metabolizada.[13]
Farmacodinámica
Mecanismo de acción
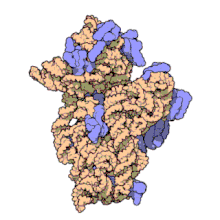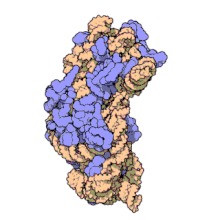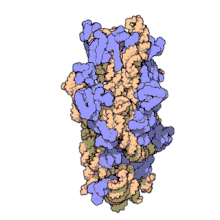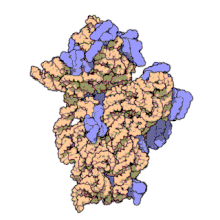
La amikacina se adhiere de manera irreversible al ARNr 16S y la proteína S12 de la subunidad 30S en el ribosoma procariótico. Inhibe la síntesis de proteínas al cambiar la conformación del ribosoma hasta que no puede leer los codones de ARNm correctamente.[14] También interfiere con la región que interacciona con el par base inestable del anticodón de ARNt .[15] Trabaja de manera que depende en la concentración y tiene una mejor acción en un ambiente alcalino.[1]
Con dosis normales, las bacterias sensibles a amikacina responden en 24-48 horas.[11]
Resistencia
La amikacina evade ataques por todas las enzimas que desactivan antibióticos, y da resistencia a antibióticos y a las bacterias, excepto a la aminoacetiltransferasa y nucleotidiltransferasa.[16] La Amikacina tiene una parte de L-HABA adherido a N-1, donde la kanamicina sólo tiene un hidrógeno, el cual bloquea el acceso y disminuye la afinidad de enzimas desactivadores.[17][18] Así, la amikacina tiene sólo uno sitio donde estas enzimas pueden atacar, mientras que los aminoglucósidos gentamicina y tobramicina tienen seis.[12]
Las bacterias que son resistente a estreptomicina y capreomicina son todavía susceptibles a amikacina; las que son resistentes a kanamicina tiene susceptibilidad variable a amikacina. Resistencia a amikacina también confiere resistencia a kanamicina y capreomicina.[19]
La resistencia a la amikacina y a la kanamicina en Mycobacterium, el agente causativo de la tuberculosis, se debe a una mutación en el gen rrs, el cual codifica la subunidad 16S de ARNr. Mutaciones como estas reducen la afinidad de la amikacina al ribosoma de las bacterias.[20] Variaciones de la acetiltransferasa aminoglucósida (AAC) y a la adenililtransferasa aminoglucósida (AAD) también confieren resistencia: resistencia en 'Pseudomonas aeruginosa está causado por AAC(6')-IV, el cual también confiere resistencia a kanamicina, gentamicina y tobramicina, y resistencia en Staphylococcus aureus y S. epidermidis está causada por AAD(4',4), el cual también confiere resistencia a la kanamicina, a la tobramicina y a la apramicina.[17] Algunas capas de S. aureus pueden también desactivar la amikacina por fosforilarlo.[21]
Interacciones
Aunque los betalactámicos pueden inactivar la amikacina, pero no tanto como otros aminoglucósidos, se les usa a menudo con penicilinas (un tipo de betalactámico) para crear un efecto aditivo contra ciertas bacterias, y con carbapenemas, con que se puede tener un efecto sinérgico contra algunas bacterias grampositivas. Otro grupo de betalactámicos, los cefalosporinas, pueden aumentar la nefrotoxicidad de aminoglucósidos y elevar aleatoriamente los niveles de creatinina. Los antibióticos cloranfenicol, clindamicina y tetraciclina inactivan los aminoglucósidos con el antagonismo farmacológico.[3]
El efecto de la amikacina aumenta cuando se utiliza con los fármacos derivados de la toxina botulínica,[22] los anestésicos, bloqueadores neuromusculares o dosis grandes de sangre que contiene ácido cítrico como un anticoagulante.[3]
Los diuréticos potentes no sólo causan la ototoxicidad sino también pueden aumentar la concentración de amikacina en el suero y tejido, haciendo que la ototoxicidad sea aún más probablemente.[3] La quinidina también aumenta los niveles de amikacina en el cuerpo.[22] El AINE indometacina puede auentar los niveles de aminoglucósidos en el suero de infantes prematuros.[3] Medios de contraste como ioversol aumentan la nefrotoxicidad y ototoxicidad causados por la amikacina.[22]
La amikacina puede disminuir el efecto de ciertas vacunas, como la vacuna BCG viva (para tuberculosis), la vacuna contra cólera y la vacuna vivo contra la fiebre tifoidea por actuar como una antagonista farmacolgógica.[22]
Uso clínico
Indicaciones
La amikacina se usa para tratar infecciones severas con bacterias multiresistentes, aeróbicas y gramnegativas, especialmente Pseudomonas, Acinetobacter, Enterobacter, E. coli, Proteus, Klebsiella y Serratia.[11] Las únicas bacterias grampositivas contra las que se puede usar la amikacina son Staphylococcus y Nocardia.[23] También se suele usar para tratar infecciones mycobacteriales tanto las que no son tuberculosis como las que son tuberculosis causado por cepas susceptibles cuándo los fármacos de primera línea han fallado. Es raro utilizarla sola.[12]
Se usa a menudo en las situaciones siguientes:
- Bronquiectasia[22]
- Infecciones del hueso y de la articulación
- Granulocitopenia, combinado con la ticarcilina, en personas con cáncer[21]
- En infecciones abdominales (como peritonitis), como un complemento de otros fármacos (clindamicina, metronidazol, piperacillin con tazobactam o ampicilina con sulbactam)
- Meningitis:
- De E. coli, como un complemento de imipenem
- De Pseudomonas, como un complemento a meropenem
- De Acetobacter, como un complemento de imipenem o colistina
- Meningitis neonatal de Streptococcus agalactiae o Listeria monocytogenes, como un complemento de ampicilina
- Meningitis neonatal de bacterias gramnegativas como E. coli, como un complemento de una cefalosporina de tercera generación
- Mycobacterium, como fármaco de segunda línea para la tuberculosis activa[24] Es también utilizada para infecciones por Mycobacterium avium, M. abscessus, M. chelonae y M. fortuitum.
- Rhodococcus equi, que causa una infección que se parece a tuberculosis
- Infecciones de vía respiratoria, incluyendo como un complemento de betalactámicos o carbapenem para la neumonia nosocomial (adquirida en un hospital)
- Sepsis, incluyendo que para neonates,[11] como un complemento de betalactámicos o carbapenem
- Infecciones de piel y de sitios con suturas[11]
- Infecciones urinarias de las bacterias que ya son resistentes a fármacos menos tóxicos (a menudo de Enterobacteriaceae o P. aeruginosa)
La amikacina se puede combinar con un betalactámicos para la terapia empírica en ellos con neutropenia y fiebre.[3]
La amikacina liposomal para la inhalación está actualmente en investigaciones clínicas para el tratamiento de enfermedades respiratorias, como fibrosis quística,[25] Pseudomonas aeruginosa,[26] bronchiectasis[27][28] e infecciones de Mycobacterium que no son de tuberculosis.[29]
Efectos secundario
Los efectos secundarios de la amikacina son similares a aquellos de otro aminoglucósidos. Los efectos más importantes son la Nefrotoxicidad (daño al riñón) y la ototoxicidad (que pueden dirigir a la pérdida de audición), con una incidencia de 1-10% de usuarios.[22] Se piensan que la tendencia de la amikacina a acumularse en el riñón y en el oído interno sea la causa de estas toxicidades.[1]
La amikacina puede causar la neurotoxicidad, si se usa en una dosis más alta o en un tiempo más largo de lo recomendable. Los efectos resultantes de neurotoxicidad incluyen vértigo, entumecimiento, hormigueo de la piel (parestesia), sacudidos de los músculos, y convulsiones.[3] Su efecto tóxico en el 8º nervio craneal causa ototoxicidad, resultando en pérdida de equilibrio y de audición.[1] El daño a la cóclea es causado por el forzado apoptosis de las células ciliadas, que dirige a la pérdida de oír frecuencias altas, que pasa antes de que se puede detectar cualquier otra pérdida de audición.[11][30] Hay daño a los vestíbulos, probablemente por crear radicales libres oxidativos. Esto no depende en la dosis sino en el tiempo de la duración de la administración.[31]
La amikacina causa nefrotoxicidad por actuar en los túbulos renales proximales, ioniza a un catión fácilmente y se adhiere a los sitios aniónicos de las células epiteliales en el túbulo proximal como parte de pinocitosis mediado por receptores. La concentración de amikacina en la corteza renal se hace diez veces más que su concentración en el plasma;[13] entonces, probablemente interfiere con el metabolismo de fosfolípidos en los lisosomas, el cual causa enzimas líticos para filtrar al citoplasma.[1] La nefrotoxicidad resulta en la concentración aumentada de creatinina, nitrógeno ureico en sangre, células de sangre roja y células de sangre blanca en el suero, así como albuminuria (producción aumentada de albúmina en la orina), glucosuria (excreción de glucosa a la orina), una disminución de gravedad específica de la orina y oliguria (disminución en producción de orina global).[11][30] También pueda causar la apariencia de cilindros urinarios.[1] Los cambios en la función de los túbulos renales también cambian los niveles de electrólitos y el equilibrio entre ácidos y bases en el cuerpo, los cuales pueden dirigir a hipopotasemia y acidosis o alcalosis.[31] La nefrotoxicidad es más común en aquellos con ciertas condiciones preexistentes: hipopotasemia, hipocalcemia, hipomagnesemia, acidosis, tasa de filtración glomerular baja, diabetes mellitus, deshidtratación, fiebre y sepsis, y aquellos quien están tomando antiprostaglandinas.[3][1][31][13] La toxicidad normalmente revierte cuando el curso de antibiótico ha sido completado,[1] y puede ser evitado por una dosis a menor frecuencia (como una vez cada 24 horas en lugar de cada 8 horas).[13]
La amikacina puede causar bloqueo neuromuscular (incluyendo la parálisis muscular aguda) y parálisis respiratoria (incluyendo la apnea).[3]
Efectos secundarios raros (ocurriendo en menos de 1% de usuarios) incluyen reacciones alérgicas, sarpullidos en la piel, fiebre, dolor de cabeza, temblor, náusea y vomitando, eosinofilia, artralgia, anemia, hipotensión e hipomagnesemia. En inyecciones intravítreos (dónde se inyecta la amikacina en el ojo), el infarto macular puede causar pérdida de visión permanente.[11][22]
Contraindicaciones
Se debe evitar la amikacina en aquellos que son sensibles a cualquier aminoglucósido, porque al ser alérgico a un aminoglucósido se confiere la hipersensibilidad a los otros por hipersensibilidad cruzada. También tienen que evitar su uso aquellos sensibles a sulfito (común en personas asmáticas),[11] porque la amikacina normalmente viene con disulfito de sodio, que puede causar una reacción alérgica.[3]
En general, no se debe usar amikacina con otro fármaco que puede causar neurotoxicidad, ototoxicidad o nefrotoxicidad. Tales fármacos incluyen otros aminoglucósidos; el antiviral aciclovir; el antifúngico anfotericina B; los antibióticos bacitracina, capreomicina, colistina, polimixina B y vancomicina; y cisplatino, el cual se usa para quimioterapia.[3]
También, no tendría que ser utilizado con fármacos que son bloqueadores neuromusculares, porque pueden aumentar debilidad de músculo y parálisis.[3]
Poblaciones especiales
Se tiene que usar una dosis más baja de amikacina en los ancianos, que a menudo tienen problemas renales a causa de la edad, y los niños, cuyos riñones todavía no están desarrollados completamente. Se considera como categoría de embarazo D en ambos los Estados Unidos y Australia, significando que tiene una probabilidad de hacer daño el feto.[3] Alrededor de 16% de amikacina cruce la placenta, y mientras la vida media de amikacina en la madre es 2 horas, es de 3.7 horas en el feto.[11] Una mujer embarazada que toma amikacina con otro aminoglucósidos puede causar sordera congénita en su niño. Aunque cruce la placenta, la amikacina es sólo parcialmente secretado en la leche materna.[3]
En general, el tratamiento con amikacina tiene que ser evitado en niños.[13] Los niños también suelen tener un volumen de distribución más grande debido a su concentración más alta de fluido extracelular, donde los aminoglucósidos se concentran.[1]
Los ancianos suelen mantener la amikacina en su sistema por más tiempo, ya que la depuración de amikacina en un anciano de 80 años es de solo 3 litros por hora, mientras que en una persona de 20 años la media de depuración es de 6 litros por hora.—.[32]
La depuración es más alta en personas con fibrosis quística.[33]
En personas con desórdenes musculares como miastenia gravis o la enfermedad de Parkinson, el efecto paralítico de amikacina en los cruces neuromusculares puede empeorar la debilidad muscular.[3]
Presentaciones
Se puede administrar la amikacina una vez o dos veces al día. Normalmente se da por vía intravenosa o intramuscular, aunque se puede dar por nebulización. No hay una forma oral, porque la amikacina no se absorbe por esta vía. En personas con insuficiencia renal, la dosis tiene que ser ajustada según la depuración de creatinina, por lo que normalmente se reduce la frecuencia de aplicación—.[11] En personas con una infección del sistema nervioso central—como meningitis—la amikacina puede ser dada por inyección directa en la espina o en los ventrículos cerebrales.
Uso veterinario
Aunque la amikacina es sólo aprobado por el FDA para uso en perros y para infecciones intrauterinas en caballos, es uno de los aminoglucósidos más utilizado en la medicina veterinaria,[34] y se lo ha usado en perros, gatos, cuyes, chinchillas, hámsteres, ratas, ratones, perritos de las praderas, ganado, pájaros, serpientes, tortugas y testudínidos, crocodilios, rana toros y pez.[1][35][36] Se usa a menudo para infecciones respiratorias en serpientes, enfermedades bacterianas de concha en tortugas y sinusitis en guaras. Es generalmente contraindicada en conejos y liebres (aunque todavía se utiliza) porque hace daño al equilibrio de la flora intestinal.[1]
En perros y gatos, se generalmente utiliza la amikacina como un antibiótico tópico para infecciones de oreja y para úlceras de la córnea, especialmente ellas de Pseudomonas aeruginosa. A menudo, se limpia las orejas antes de administrar la medicación porque el pus y los escombros celulares menoscaban la actividad de amikacina.[34] Se la administra al ojo cuando está en forma de ungüento o solución oftálmico o cuando se inyecta subconjuntivalmente.[37] Amikacina en el ojo puede ser acompañado por cefazolina. A pesar de su uso allí, amikacina—y todos los aminoglucósidos—es tóxica a las estructuras intraoculares.[38]
En caballos, la amikacina es aprobado por el FDA para infecciones del útero—como endometriosis y piometra—de bacterias susceptibles.[39] También se da como medicación tópica para los ojos y el lavado artroscópico; cuándo se combina con una cefalosporina, se usa para tratar infecciones subcutáneas de Staphylococcus. Para infecciones en las extremidades o las articulaciones, se administra con una cefalosporina como una perfusión de extremidades o una inyección en las articulaciones.[34][40] También se puede inyectar la amikacina en las articulaciones con la medicación antiartrítica Adequan para impedir la infección.[41]
Los efectos secundarios en animales incluyen la nefrotoxicidad, ototoxicidad y reacciones alérgicas en los sitios de inyección intramuscular. Los gatos suelen ser más sensibles al daño vestibular causado por la ototoxicidad. Los efectos menos frecuentes incluyen el bloqueo neuromuscular, el edema de rostro y neuropatía periférica.[34][1]
La vida media en la mayoría de animales es 1-2 horas.[42]
Para tratar la sobredosis de amikacina, se requiere hemodiálisis o diálisos peritoneal, los cuales reducen concentraciones la amikacina en el suero, y/o penicilinas, algunos de los cuales pueden formar complejos con amikacina que la desactivan.[1]
Referencias
- Plumb, Donald C. (2011). «Amikacin Sulfate». Plumb's Veterinary Drug Handbook (en inglés) (7º edición). Stockholm, Wisconsin; Ames, Iowa: Wiley. pp. 39-43. ISBN 978-0-470-95964-0.
- Thomson PLM (2008). «Amikacina». En José Antonio Solís Sánchez, ed. Vademécum de genéricos intercambiables. México, D.F. Consultado el 15 de octubre de 2011.
- «Amikacin Sulfate» (en inglés). The American Society of Health-System Pharmacists. Consultado el 8 de diciembre de 2016.
- WHO Model Formulary 2008 (en inglés). World Health Organization. 2009. p. 137. ISBN 9789241547659. Archivado desde el original el 13 de diciembre de 2016. Consultado el 8 de diciembre de 2016.
- Fischer, Janos; Ganellin, C. Robin (2006). Analogue-based Drug Discovery (en inglés). John Wiley & Sons. p. 507. ISBN 9783527607495. Archivado desde el original el 20 de diciembre de 2016.
- Oxford Handbook of Infectious Diseases and Microbiology (en inglés). OUP Oxford. 2009. p. 56. ISBN 9780191039621. Archivado desde el original el 24 de noviembre de 2015.
- «WHO Model List of Essential Medicines (19th List)». World Health Organization (en inglés). abril de 2015. Archivado desde el original el 13 de diciembre de 2016. Consultado el 8 de diciembre de 2016.
- «Amikacin Sulfate». International Drug Price Indicator Guide (en inglés). Archivado desde el original el 22 de julio de 2018. Consultado el 8 de diciembre de 2016.
- Kawaguchi, H.; Naito, T.; Nakagawa, S.; Fujisawa, K. I. (diciembre de 1972). «BB-K 8, a new semisynthetic aminoglycoside antibiotic». The Journal of Antibiotics (en inglés) 25 (12): 695-708. ISSN 0021-8820. PMID 4568692. doi:10.7164/antibiotics.25.695. Archivado desde el original el 16 de agosto de 2017.
- Monteleone, Peter M.; Muhammad, Naseem; Brown, Robert D.; McGrory, John P.; Hanna, Samir A. (1 de enero de 1983). «Amikacin Sulfate». Analytical Profiles of Drug Substances. Analytical Profiles of Drug Substances (en inglés) 12: 37-71. ISBN 9780122608124. ISSN 0099-5428. doi:10.1016/S0099-5428(08)60163-X.
- Biblioteca Nacional de Medicina de los Estados Unidos (17 de agosto de 2016). «AMIKACIN SULFATE- amikacin sulfate injection». DailyMed (en inglés). Consultado el 8 de agosto de 2017.
- Cunha, Burke A. (1 de noviembre de 2006). «New Uses for Older Antibiotics: Nitrofurantoin, Amikacin, Colistin, Polymyxin B, Doxycycline, and Minocycline Revisited». Medical Clinics of North America. Antimicrobial Therapy (en inglés) 90 (6): 1089-1107. ISSN 0025-7125. doi:10.1016/j.mcna.2006.07.006.
- Ettinger, Stephen J.; Feldman, Edward C. (24 de diciembre de 2009). Textbook of Veterinary Internal Medicine (en inglés). Elsevier Health Sciences. pp. 1976, 523. ISBN 978-1-4377-0282-8.
- Microbiology: With Diseases by Body System (4th edición). Boston: Pearson. 2015. ISBN 978-0-321-91855-0.
- «Amikacin». DrugBank. 2 de agosto de 2017. Archivado desde el original el 16 de agosto de 2017. Consultado el 10 de agosto de 2017.
- Mudd, Efrain (7 de agosto de 2017). «O Aminoglycosides». Pharmacological Sciences. Archivado desde el original el 16 de agosto de 2017. Consultado el 14 de agosto de 2017.
- Kondo, Shinichi; Hotta, Kunimoto (1 de enero de 1999). «Semisynthetic aminoglycoside antibiotics: Development and enzymatic modifications». Journal of Infection and Chemotherapy 5 (1): 1-9. ISSN 1341-321X. PMID 11810483. doi:10.1007/s101560050001.
- Park, Je Won; Ban, Yeon Hee; Nam, Sang-Jip; Cha, Sun-Shin; Yoon, Yeo Joon (1 de diciembre de 2017). «Biosynthetic pathways of aminoglycosides and their engineering». Current Opinion in Biotechnology 48: 33-41. ISSN 0958-1669. PMID 28365471. doi:10.1016/j.copbio.2017.03.019.
- Caminero, José A; Sotgiu, Giovanni; Zumla, Alimuddin; Migliori, Giovanni Battista (1 de septiembre de 2010). «Best drug treatment for multidrug-resistant and extensively drug-resistant tuberculosis». The Lancet Infectious Diseases 10 (9): 621-629. ISSN 1473-3099. doi:10.1016/S1473-3099(10)70139-0.
- Ahmad, Suhail; Mokaddas, Eiman (1 de marzo de 2014). «Current status and future trends in the diagnosis and treatment of drug-susceptible and multidrug-resistant tuberculosis». Journal of Infection and Public Health 7 (2): 75-91. ISSN 1876-0341. PMID 24216518. doi:10.1016/j.jiph.2013.09.001.
- Aronson J. K., ed. (2016). «Amikacin». Meyler's Side Effects of Drugs (en inglés) (16º edición). Oxford: Elsevier. pp. 207-209. ISBN 978-0-444-53716-4.
- «amikacin (Rx)». Medscape (en inglés). WebMD. Consultado el 9 de agosto de 2017.
- Scholar, Eric M.; Pratt, William B. (22 de mayo de 2000). The Antimicrobial Drugs (en inglés) (2º edición). Oxford University Press, USA. pp. 15-19. ISBN 978-0-19-975971-2. Archivado desde el original el 10 de septiembre de 2017.
- Vardanyan, Ruben; Hruby, Victor (2016). «Chapter 32: Antimicobacterial Drugs». Synthesis of Best-Seller Drugs (en inglés). Boston: Academic Press. pp. 669-675. ISBN 978-0-12-411492-0.
- «Randomized, open-label, active-controlled, multicenter study to assess the efficacy, safety and tolerability of Arikace™ in Cystic Fibrosis patients with chronic infection due to Pseudomonas aeruginosa». EU Clinical Trials Register (en inglés).
- «Study to Evaluate Arikayce™ in CF Patients With Chronic Pseudomonas Aeruginosa Infections». ClinicalTrials.gov (en inglés).
- «A Study to Determine the Safety and Tolerability of Arikace™ Versus Placebo in Patients Who Have Bronchiectasis». ClinicalTrials.gov (en inglés).
- «A Study to Determine the Safety and Tolerability of Arikace™ Versus Placebo in Patients Who Have Bronchiectasis». UK Clinical Trials Gateway (en inglés).
- «Arikayce for Nontuberculous Mycobacteria». ClinicalTrials.gov (en inglés).
- Morris, Daniel O.; Kennis, Robert A. (11 de octubre de 2012). Clinical Dermatology, An Issue of Veterinary Clinics: Small Animal Practice, E-Book (en inglés). Elsevier Health Sciences. p. 29. ISBN 978-1-4557-7377-0. Archivado desde el original el 10 de septiembre de 2017.
- Corti, Natascia; Taegtmeyer, Anne; Imhof, Alexander (1 de enero de 2011). «Miscellaneous antibacterial drugs». Side Effects of Drugs Annual. A worldwide yearly survey of new data in adverse drug reactions (en inglés) 33: 509-540. ISBN 9780444537416. ISSN 0378-6080. doi:10.1016/B978-0-444-53741-6.00026-X.
- Maire, P.; Bourguignon, L.; Goutelle, S.; Ducher, M.; Jelliffe, R. (2017). «Chapter 20 - Individualizing Drug Therapy in the Elderly». Individualized Drug Therapy for Patients (en inglés). Boston: Academic Press. pp. 373-382. ISBN 978-0-12-803348-7.
- Eghianruwa, Kingsley (2014). Essential Drug Data for Rational Therapy in Veterinary Practice (en inglés). Author House. p. 16. ISBN 978-1-4918-0000-3. Archivado desde el original el 10 de septiembre de 2017.
- Forney, Barbara. «Amikacin for Veterinary Use». Wedgewood Pharmacy (en inglés). Consultado el 9 de agosto de 2017.
- Riviere, Jim E.; Papich, Mark G. (13 de mayo de 2013). Veterinary Pharmacology and Therapeutics (en inglés). John Wiley & Sons. p. 931. ISBN 978-1-118-68590-7.
- Mader, Douglas R.; Divers, Stephen J. (12 de diciembre de 2013). Current Therapy in Reptile Medicine and Surgery - E-Book (en inglés). Elsevier Health Sciences. p. 382. ISBN 978-0-323-24293-6.
- Maggs, David; Miller, Paul; Ofri, Ron (7 de agosto de 2013). Slatter's Fundamentals of Veterinary Ophthalmology - E-Book (en inglés). Elsevier Health Sciences. p. 37. ISBN 978-0-323-24196-0.
- Hsu, Walter H. (25 de abril de 2013). Handbook of Veterinary Pharmacology (en inglés). John Wiley & Sons. p. 486. ISBN 978-1-118-71416-4.
- Biblioteca Nacional de Medicina de los Estados Unidos (9 de marzo de 2017). «AMIGLYDE-V- amikacin sulfate injection». DailyMed (en inglés). Consultado el 8 de agosto de 2017.
- Orsini, James A. (1 de agosto de 2017). «Update on Managing Serious Wound Infections in Horses: Wounds Involving Joints and Other Synovial Structures». Journal of Equine Veterinary Science (en inglés) 55: 115-122. ISSN 0737-0806. doi:10.1016/j.jevs.2017.01.016.
- Wanamaker, Boyce P.; Massey, Kathy (25 de marzo de 2014). Applied Pharmacology for Veterinary Technicians - E-Book (en inglés). Elsevier Health Sciences. p. 392. ISBN 978-0-323-29170-5.
- Papich, Mark G. (octubre de 2015). «Amikacin». Saunders Handbook of Veterinary Drugs: Small and Large Animal (en inglés) (4º edición). Elsevier Health Sciences. pp. 25-27. ISBN 978-0-323-24485-5.
- S.S.A. Catálogo de Medicamentos Genéricos Intercambiables para farmacias y público en general al 3 de agosto de 2007.
Con el objeto de demostrar la intercambiabilidad a que se refiere el artículo 75 del reglamento de Insumos para la Salud, los medicamentos que integran el Catálogo de Medicamentos Genéricos Intercambiables han sido comparados, siguiendo los lineamientos indicados por la NOM-177SSA1-1998, contra los productos innovadores o de referencia enlistados en las págs. 11 a 22 donde usted lo podrá consultar
