Butironitrilo
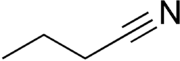
El butironitrilo, también llamado butanonitrilo, propilcianuro y 1-cianopropano, es un compuesto orgánico de fórmula molecular C4H7N.[2][3][4] Es un nitrilo lineal de cuatro átomos de carbono con un grupo funcional C≡N en su extremo.
| Butironitrilo | ||
|---|---|---|
 | ||
 | ||
| Nombre IUPAC | ||
| butanonitrilo | ||
| General | ||
| Otros nombres |
propilcianuro 1-cianopropano n-butironitrilo | |
| Fórmula semidesarrollada | CH3-(CH2)2-C≡N | |
| Fórmula molecular | C4H7N | |
| Identificadores | ||
| Número CAS | 109-74-0[1] | |
| Número RTECS | ET8750000 | |
| ChEBI | 51937 | |
| ChemSpider | 7717 | |
| PubChem | 8008 | |
| UNII | O3V36V0W0M | |
|
CCCC#N
| ||
| Propiedades físicas | ||
| Apariencia | Líquido incoloro | |
| Olor | Intenso y sofocante | |
| Densidad | 792 kg/m³; 0,792 g/cm³ | |
| Masa molar | 6911 g/mol | |
| Punto de fusión | −112 °C (161 K) | |
| Punto de ebullición | 117 °C (390 K) | |
| Presión de vapor | 18,5 mmHg | |
| Viscosidad | 0,6 cP | |
| Índice de refracción (nD) | 1,384 | |
| Propiedades químicas | ||
| Solubilidad en agua | 33 g/L | |
| log P | 0,62 | |
| Familia | Nitrilo | |
| Peligrosidad | ||
| Punto de inflamabilidad | 291,15 K (18 °C) | |
| NFPA 704 |
3
3
1
| |
| Temperatura de autoignición | 774,15 K (501 °C) | |
| Compuestos relacionados | ||
| nitrilos |
dimetilaminoacetonitrilo valeronitrilo pivalonitrilo | |
| dinitrilos |
succinonitrilo glutaronitrilo | |
| polinitrilos | cianoformo | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
Propiedades físicas y químicas
A temperatura ambiente, el butironitrilo es un líquido incoloro con un olor intenso y sofocante. Tiene su punto de ebullición a 117 °C mientras que su punto de fusión es de -112 °C. Con una densidad inferior a la del agua (ρ = 0,792 g/cm³), es menos viscosa que ésta (0,6 cP a 20 °C). Posee una solubilidad en agua de 33 g/L, siendo también miscible en éter, dimetilformamida y benceno. El valor del logaritmo de su coeficiente de reparto, logP = 0,62, indica que es más soluble en disolventes apolares —como el 1-octanol— que en disolventes polares.[5][3] En forma de vapor, su densidad es 2,4 veces mayor que la del aire.[2]
En cuanto a su reactividad, el butironitrilo es incompatible con agentes oxidantes.[6]
Presencia en el entorno
El butironitrilo ha sido estudiado en relación con una nueva cepa bacteriana, denominada ANL-iso2(T), obtenida a partir de un cultivo inoculado con sedimentos de un lago de sosa. Dicha bacteria utiliza distintos nitrilos como único sustrato de crecimiento, siendo dicho desarrollo bifásico, empezando con una rápida hidrólisis de nitrilo a amida, ácido carboxílico y amoníaco, para luego continuar con una pausada utilización de dichos productos, observándose el crecimiento de la biomasa.[7] En este sentido, la degradación microbiana de nitrilos reviste interés medioambiental; la bacteria Rhodococcus sp. RHA1 presente en suelos utiliza una serie de nitrilos, incluyendo el butironitrilo, como sustratos de crecimiento, habiéndose purificado y caracterizado una enzima nitrilo hidratasa recién descubierta en este organismo.[8]
Por otra parte, el butironitrilo ha sido detectado en el espacio exterior, dentro de la Gran Molécula Heimat,[9] densa nube de gas localizada en la nube molecular Sagittarius B2.[10]
Síntesis
A nivel industrial, el butironitrilo se prepara por amoxidación del 1-butanol, de acuerdo a la reacción:
- C3H7CH2OH + NH3 + O2 → C3H7CN + 3 H2O
Otro método para la síntesis de este nitrilo parte del butanal, el cual se trata con NH2OH·HCl/Al2O3 seco/MeSO2Cl, sin necesidad de disolvente.[11] Otra forma de obtener butironitrilo es por deshidratación de butiraldoxima, reacción que puede ser catalizada por distintos sistemas tales como Pd(OAc)2/Ph3P, [(CH3CH2CN)2]PtCl4, O3Re(OH), porfirina de hierro o níquel Raney; si esta transformación se lleva a cabo en acetonitrilo utilizando cloruro de níquel como catalizador, el rendimiento alcanza el 99%.[12]
Un procedimiento alternativo para sintetizar este nitrilo se basa en la electrólisis a corriente constante de butanamida y trifenilfosfina en diclorometano; el rendimiento es del 95% aproximadamente.[13] Asimismo, los nitrilos pueden sintetizarse por oxidación de la correspondiente amina (1-butanamina en este caso), siendo los oxidantes más utilizados níquel de Sabatier, pentafluoruro de iodo, peróxido de níquel y tetraacetato de plomo; la utilización del sistema [Cu(I)Cl/O2/piridina] permite alcanzar un rendimiento del 93%.[14]
Usos
El butironitrilo es profusamente empleado en cromatografía normal y de fase inversa. También se ha usado en investigaciones de actividad genotóxica, sirviendo para comparar el análisis de cometas frente al test de Ames.[15] Otro uso de este nitrilo es como disolvente dentro de composiciones electrolíticas utilizadas en células solares sensibilizadas con colorantes.[16]
Precauciones
El butironitrilo es un compuesto fácilmente inflamable que tiene su punto de inflamabilidad a 18 °C. Al arder puede desprender humos tóxicos conteniendo óxidos de nitrógeno, monóxido de carbono y cianuro de hidrógeno. Es una sustancia tóxica si se ingiere o inhala, y puede provocar irritación en piel y ojos.[6]
Véase también
Los siguientes compuestos son nitrilos con cuatro átomos de carbono:
- Isobutironitrilo
- Metacrilonitrilo
- Crotononitrilo
- Cianuro de alilo
- Cianopropino
Referencias
- Número CAS
- Butyronitrile (PubChem)
- Butyronitrile (ChemSpider)
- Butyronitrile (Chemical Book)
- Butanenitrile (EPA)
- Butironitrilo. MSDS (AlfaAesar)
- Sorokin D.Y.; van Pelt S.; Tourova T.P.; Evtushenko L,I. (2009). «Nitriliruptor alkaliphilus gen. nov., sp. nov., a deep-lineage haloalkaliphilic actinobacterium from soda lakes capable of growth on aliphatic nitriles, and proposal of Nitriliruptoraceae fam. nov. and Nitriliruptorales ord. nov.». Int J Syst Evol Microbiol. 59 Feb (Pt2): 248-253. Consultado el 6 de marzo de 2017.
- Okamoto S.; Eltis LD. (2007). «Purification and characterization of a novel nitrile hydratase from Rhodococcus sp. RHA1». Mol. Microbiol. 65 (3): 828-838. Consultado el 17 de marzo de 2017.
- «Two highly complex organic molecules detected in space». Royal Astronomical Society. 21 de abril de 2009. Consultado el 29 de septiembre de 2015.
- «New organic molecules in space». Max Planck Society. 26 de marzo de 2008. Consultado el 28 de septiembre de 2015.
- Hashem Sharghi; Mona Hosseini Sarvari (2002). «A direct synthesis of nitriles and amides from aldehydes using dry or wet alumina in solvent free conditions». Tetrahedron 58 (52): 10323-10328.
- Li, Yen-Ting; Liao, Bei-Sih; Chen, Hsin-Pei; Liu, Shiuh-Tzung (2011). «Ligand-Free Nickel-Catalyzed Conversion of Aldoximes into Nitriles». Synthesis 16: 2639-2643.
- Ohmori, Hidenobu; Sakai, Kiyoshi; Nagai, Noriko; Mizuki, Yasuyuki; Masui, Masaichiro (1985). «Reaction of Electrochemically Generated Triphenylphosphine Radical Cation with Amides and Ureas». Chemical and Pharmaceutical Bulletin 33 (1): 373-376.
- Patrice Capdevielle; André Lavigne; Michel Maumy (2009). «Improved and Extended One-Step Conversion of Primary Amines into Nitriles by Copper-Catalyzed Oxidation». Synthesis 89 (6): 453-454. Consultado el 17 de marzo de 2017.
- Wu, J.C.; Hseu, Y.C.; Chen, C.H.; Wang, S.H.; Chen, S.C. (2009). «Comparative investigations of genotoxic activity of five nitriles in the comet assay and the Ames test». J. Hazard Mater. 169 (1-3): 492-497. Consultado el 17 de marzo de 2017.
- Sauvage, F.; Chhor, S.; Marchioro, A.; Moser, J.E.; Graetzel, M. (2011). «Nitriliruptor alkaliphilus gen. nov., sp. nov., a deep-lineage haloalkaliphilic actinobacterium from soda lakes capable of growth on aliphatic nitriles, and proposal of Nitriliruptoraceae fam. nov. and Nitriliruptorales ord. nov.». J. Am. Chem. Soc. 133 (33): 13103-13109. Consultado el 17 de marzo de 2017.
