wikiHow est un wiki, ce qui veut dire que de nombreux articles sont rédigés par plusieurs auteurs(es). Pour créer cet article, 19 personnes, certaines anonymes, ont participé à son édition et à son amélioration au fil du temps.
Il y a 7 références citées dans cet article, elles se trouvent au bas de la page.
Cet article a été consulté 13 625 fois.
La chimie organique a une très mauvaise réputation. En fait, avant de passer l’examen, les étudiants entendent très souvent des histoires horribles sur les difficultés de cette matière. Bien que cette matière soit un peu complexe, au fond, la chimie organique n’est pas un cauchemar comme ça en a l’air. Il y a très peu de concepts à mémoriser, mais beaucoup de mécanismes à assimiler. Par conséquent, si vous tenez à réussir votre prochain examen de chimie organique, vous devez comprendre les règles de base et créer une méthode de travail efficace.
Étapes
Partie 1
Partie 1 sur 3:Connaitre les règles élémentaires de la chimie organique
-
1Apprenez la définition de la chimie organique. De manière générale, cette matière porte sur l’étude des composés chimiques contenant des atomes de carbone [1] . Le carbone est le sixième élément du tableau périodique et l’un des éléments essentiels à la vie sur Terre. Les êtres vivants sont constitués de molécules, qui sont composées principalement de carbone. En d’autres termes, la chimie organique traite des processus chimiques qui se déroulent au sein de votre corps tous les jours. Cela implique également tous les processus chimiques qui se produisent dans les plantes, les animaux et les écosystèmes.
- Cependant, la chimie organique ne se limite pas qu’aux êtres vivants. Par exemple, les réactions chimiques qui se produisent pendant la combustion des combustibles fossiles relèvent directement de la chimie organique, car ces réactions font intervenir des composés à base de carbone.
-
2Apprenez à représenter les molécules. La chimie organique est un sujet d’étude beaucoup plus visuel que la chimie générale. Vous allez devoir vous appuyer sur des dessins schématiques de molécules et de composés, plus souvent qu’au second cycle. Comprendre comment interpréter ces représentations est l’une des compétences de base les plus importantes à avoir pour étudier la chimie organique.
- Avant de commencer, vous devez vous familiariser avec les structures de Lewis. Cette notion de base est souvent enseignée en chimie générale. Selon cette représentation graphique, les atomes d’une molécule sont représentés par leur symbole chimique (les lettres sur le tableau périodique). Les lignes représentent les liaisons et les points représentent les électrons de valence. Pour vous rafraichir la mémoire, consultez cet article.
- Le concept des formules topologiques, qui peut vous sembler nouveau, constitue un autre moyen de représenter les molécules. Dans une formule topologique, les atomes de carbone ne sont pas représentés. On utilise plutôt des segments pour représenter les liaisons. Puisque les atomes de carbone sont l’élément fondamental en chimie organique, la formule topologique permet de dessiner les molécules beaucoup plus rapidement. Tous les atomes non carbonés sont représentés par leur symbole chimique. Vous trouverez ici une explication plus détaillée sur les représentations topologiques [2] .
-
3Apprenez à représenter les liaisons. Les liaisons covalentes sont de loin les liaisons les plus courantes que vous rencontrerez en chimie organique (même si le fait d’avoir une bonne compréhension des liaisons ioniques et d’autres types de liaisons est toujours important). Dans une liaison covalente, deux atomes partagent des électrons célibataires et forment une liaison. S’il y a plus d’électrons non appariés, ils forment une liaison double ou triple.
- Tant dans les formules topologiques que dans les structures de Lewis, une liaison simple est représentée par une ligne, une double liaison par deux lignes et une triple liaison par trois lignes.
- Dans les formules topologiques, les liaisons entre le carbone (C) et l’hydrogène (H) ne sont pas représentées, car ces atomes sont très utilisés.
- Sauf circonstances particulières, les atomes ne peuvent qu’avoir huit électrons de valence (couches électroniques). Cela signifie que dans la plupart des cas, un atome peut se lier au maximum à quatre autres atomes.
-
4Apprenez à représenter les structures moléculaires en 3D. En chimie organique, les étudiants doivent apprendre à visualiser la forme réelle des molécules et ne pas se contenter de les dessiner sur une feuille. Les molécules possèdent une structure en trois dimensions. La nature des liaisons entre les atomes est le facteur le plus important qui détermine la forme tridimensionnelle de la molécule, bien que ce ne soit pas le seul. Voici une liste d’éléments à retenir lorsque vous étudiez les formes en trois dimensions des molécules à base de carbone.
- Un atome de carbone relié à quatre autres atomes avec des liaisons simples prend la forme d’un tétraèdre (une pyramide à quatre sommets). Un bon exemple de cette structure est le méthane (CH4).
- Lorsqu’un carbone est lié à un autre atome avec une double liaison et à deux autres atomes avec des liaisons simples, on dit qu’il a une géométrie moléculaire trigonale plan (un triangle plat). L’ion CO3-2 en est un exemple.
- Un carbone qui est lié à deux atomes avec de doubles liaisons ou à un atome avec une triple liaison a une géométrie linéaire (une ligne rigide). Le dioxyde de carbone (CO2) en est un exemple.
-
5Apprenez à déchiffrer l’hybridation des orbitales atomiques. Ça peut sembler intimidant comme terme, mais ce concept n’est pas si difficile à comprendre. Fondamentalement, le modèle des orbitales hybrides est simplement la méthode par laquelle les chimistes représentent les électrons de valence d’un atome en fonction de son comportement (et non de sa représentation). Si un atome a un certain nombre d’électrons célibataires pour engager des liaisons, mais qu’il a tendance à former un nombre différent de liaisons, on dit que cet atome possède des orbitales hybrides pour décrire cette différence.
- Le carbone en est un exemple parfait. Il possède 4 électrons de valence, dont deux occupent l’orbitale 2s et deux électrons libres qui occupent l’orbitale 2p. Puisqu’il y a deux électrons libres, on pourrait penser que le carbone forme deux liaisons. Cependant, des expériences ont démontré que les électrons groupés dans l’orbitale 2s forment des liens, même s’ils ne sont pas libres. Par conséquent, un atome de carbone possède quatre électrons non appariés contenus dans une orbitale hybride sp.
-
6Apprenez les bases de l’électronégativité. En chimie organique, il existe de nombreux facteurs qui déterminent la façon dont deux molécules réagissent les unes avec les autres. Cependant, l’électronégativité est souvent l’un de ces facteurs les plus importants. L’électronégativité est une grandeur qui caractérise la façon dont un atome conserve ses électrons. Les atomes ayant une électronégativité élevée ont tendance à bien conserver leurs électrons (et vice versa pour les atomes ayant une électronégativité faible). Pour plus de détails à ce sujet, consultez cet article.
- L’électronégativité d’un atome augmente de la gauche vers la droite et du bas vers le haut du tableau périodique (l’hélium et l’hydrogène n’en font pas partie). Le fluor, l’élément dans la partie supérieure droite, a la plus forte électronégativité.
- Étant donné que les atomes électronégatifs ont tendance à attirer d’autres électrons, ils accaparent les électrons libres que possèdent d’autres molécules. Par exemple, les atomes tels que le chlore et le fluor prennent souvent la forme d’ions négatifs après avoir volé des électrons d’autres atomes [3] .
Publicité
Partie 2
Partie 2 sur 3:Suivre quelques conseils utiles pour ses études
-
1Ne vous laissez pas intimider. La chimie organique présente un grand nombre de concepts et vous oblige à réfléchir sur les problèmes de chimie sous de nouvelles formes. Aussi, vous devrez apprendre le vocabulaire des termes généraux de la chimie. Détendez-vous, tous vos camarades de classe sont confrontés au même problème. Étudiez avec assiduité, demandez de l’aide en cas de besoin et vous verrez que tout ira bien.
- Certains candidats qui ont réussi l’examen avant vous pourraient raconter des tas d’histoires horribles sur cette matière. Ne les écoutez pas ! Les gens ont l’habitude d’exagérer un peu sur leurs expériences. Passer votre premier examen en étant terrifié et convaincu de faire face à un défi impossible rendra juste les choses plus difficiles [4] . Au contraire, vous devez prendre confiance en vous en étudiant beaucoup et en vous reposant correctement la nuit avant l’examen.
-
2Comprenez les concepts au lieu de les mémoriser. En classe, vous allez certainement étudier des centaines de réactions différentes. Il est pratiquement impossible de les apprendre par cœur, alors ne perdez pas votre temps et limitez-vous juste aux plus importantes. Au lieu de cela, concentrez-vous sur les principes élémentaires qui régissent les réactions chimiques les plus courantes. La plupart des réactions suivent très rarement les mêmes modèles. Ainsi, si vous voulez résoudre correctement les problèmes en chimie organique, il va falloir les connaitre et savoir comment les appliquer.
- Toutefois, si vous êtes doué pour retenir les choses, vous pouvez utiliser cette compétence à votre avantage. Essayez d’écrire les mécanismes des réactions élémentaires sur de petites fiches et servez-vous-en pour les mémoriser. Vous aurez toujours besoin d’ajuster vos connaissances lorsque vous rencontrez de nouvelles réactions chimiques dans les exercices, mais vous pouvez utiliser les mêmes principes de base pour pouvoir écrire correctement un mécanisme.
-
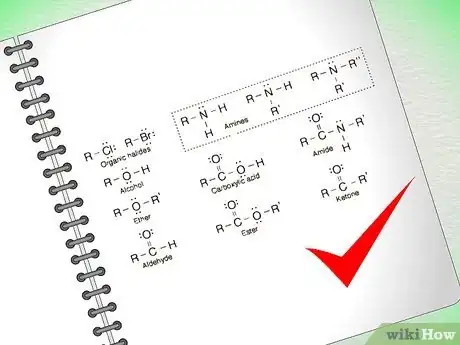
3Apprenez les groupes fonctionnels. La chimie organique de base utilise le même ensemble de structures dans pratiquement toutes les molécules. On parle de groupes fonctionnels pour décrire ces structures. Savoir identifier ces groupes et comprendre la façon dont ils ont tendance à réagir est une étape cruciale pour résoudre les problèmes en chimie organique. Étant donné que les groupes fonctionnels réagissent constamment de la même manière, connaitre leurs caractéristiques vous permettra de résoudre une série de problèmes.
- Les groupes fonctionnels en chimie organique sont trop nombreux pour qu’on puisse les énumérer tous dans cet article. Cependant, vous pouvez facilement trouver des ressources sur Internet qui vous aideront à cet effet. Par exemple, cliquez sur ce lien pour plus d’informations.
-
4Apprenez la signification de nucléophile et d’électrophile. La plupart des réactions organiques sont de trois types : nucléophile ou électrophile, péricyclique et radical, et la plus courante est de loin la réaction nucléophile ou électrophile.
- La réaction nucléophile : elle est observée quand une espèce a des électrons supplémentaires à partager. Attention aux espèces chargées négativement, aux doubles liaisons ou aux espèces neutres avec des paires isolées. On peut citer comme exemples des espèces comme les hydroxydes, la pyridine, les iodures, les alcènes, les énolates et les réactifs de Grignard.
- La réaction électrophile : elle concerne une espèce qui recherche une paire d’électrons. Attention aux espèces partiellement ou totalement chargées positivement. Les carbocations, les haloalcanes et les carbonyles en sont des exemples.
-
5En cas de doute, suivez le flux d’électrons. Au stade le plus élémentaire, la plupart des réactions organiques n’impliquent que deux ou plusieurs molécules capables de s’échanger des électrons. Si vous n’arrivez pas à écrire le mécanisme d’une réaction, commencez à évaluer où vous pouvez raisonnablement déplacer des électrons. Autrement dit, recherchez les atomes qui semblent être des accepteurs d’électrons et ceux qui semblent être des donneurs d’électrons. Procédez au transfert puis posez-vous cette question : que puis-je faire maintenant pour que les molécules soient en état de stabilité ?
- Par exemple, étant donné que l’oxygène (O) est plus électronégatif que le carbone, l’atome d’oxygène qui est fixé par double liaison au carbone dans un groupe cétone a tendance à conserver les électrons de liaison plus près de lui-même. Cela transfère au carbone une légère charge positive et lui permet d’attirer les électrons libres. Si dans la réaction il y a un atome qui a tendance à libérer des électrons, il est logique qu’il se lie au carbone en formant une nouvelle liaison et en déclenchant la réaction.
-
6Formez un groupe d’étude. Ne croyez jamais que vous pouvez faire tout seul un exercice de chimie organique. Faire ses devoirs avec d’ autres camarades est une excellente idée. Non seulement les autres personnes peuvent vous aider à mieux comprendre les concepts qui vous semblent complexes, mais vous pouvez dans le même temps renforcer vos connaissances en leur expliquant ce que vous maitrisez déjà.Publicité
Partie 3
Partie 3 sur 3:Obtenir de l’aide
-
1Apprenez à connaitre davantage votre professeur. La personne qui possède les meilleures connaissances en chimie organique dans votre classe est sans nul doute votre professeur. Profitez de cette ressource très précieuse. Allez dans le bureau de votre professeur pour discuter des concepts que vous ne comprenez pas. Essayez de lui poser quelques questions claires et concises ou des exercices que vous avez du mal traiter. Préparez-vous à lui expliquer le raisonnement qui vous conduit à la mauvaise solution.
- Évitez de contacter votre professeur sans avoir une idée claire de ce que vous voulez lui demander. Dire simplement je ne comprends pas l’exercice ne servira pas à grand-chose.
- C’est non seulement une excellente occasion de trouver des réponses à vos questions, mais c’est aussi un moyen de mieux connaitre votre professeur. N’oubliez pas que si vous voulez faire un 3e cycle, vous aurez également besoin de quelques références académiques. Les professeurs sont prêts à écrire une lettre de recommandation positive sur les étudiants qui ont pris la peine de discuter avec eux.
- Si vous n’arrivez pas à joindre votre professeur, trouvez son laboratoire de recherche et son bureau des étudiants. La plupart des professeurs emploient quelques étudiants diplômés dans leurs laboratoires et ils peuvent vous aider si vous avez des questions.
-
2Utilisez des instruments pour visualiser les problèmes. En chimie organique, la forme des molécules détermine la façon dont elles réagissent. Comme il est difficile de produire une représentation graphique en trois dimensions des molécules complexes, vous pouvez utiliser des synthons (encore appelés building blocks) pour analyser des structures complexes.
- Les modèles moléculaires sont des outils qui vous permettront de représenter les molécules avec des pièces en plastique. Ils peuvent s’avérer un peu chers si vous les achetez dans une librairie universitaire ou dans un magasin de matériel de laboratoire et d’instrumentation scientifique. Cependant, certains enseignants les prêtent aux étudiants qui en font la demande.
- Si vous ne disposez pas d’un modèle moléculaire, utilisez des billes de mousse, des marqueurs et des chevilles en bois. Vous pouvez facilement les trouver dans les magasins d’artisanat et de bricolage.
- Il existe aussi plusieurs programmes informatiques (comme ChemDraw) qui peuvent vous aider à visualiser les molécules en 3D [5] .
-
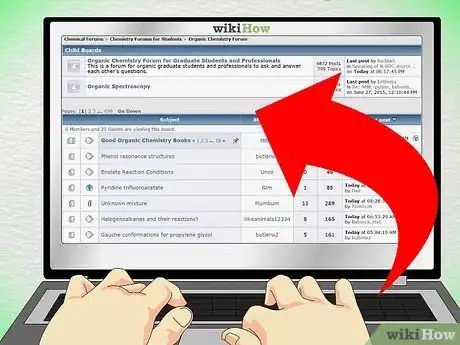
3Rejoignez un forum en ligne. L’un des bons côtés du niveau de difficulté de la chimie organique, c’est que beaucoup d’étudiants cherchent de l’aide en ligne et viennent également en aide à d’autres apprenants. Il existe une multitude de forums composés d’importantes communautés de personnes qui veulent discuter des questions les plus complexes en chimie organique. Essayez de publier un exercice qui vous pose problème sur l’un de ces forums, puis discutez avec les personnes qui vous répondront afin de trouver la solution.
-
4Utilisez des ressources en ligne. Il existe de nombreux sites qui peuvent vous aider à résoudre les sujets les plus complexes de la chimie organique. En voici quelques-uns.
- Techno-science : il s’agit d’une excellente ressource et vous y trouverez des informations et des articles intéressants.
- Éduscol : bien qu’il ne soit plus actualisé depuis 2016, ce site dispose de quelques cours en chimie qui peuvent vous aider à mieux comprendre cette science. Vous y trouverez également des exercices ainsi que des travaux pratiques [7] .
- UNISCIEL : ce site propose un grand nombre de ressources numériques de qualité dans plusieurs disciplines scientifiques, dont la chimie.
Publicité
Conseils
- Si vous consacrez plus de temps à la chimie organique, il vous sera plus facile de comprendre les concepts de base les plus importants. Essayez de consacrer à cette matière au moins une heure ou deux tous les jours. La cohérence est toute aussi importante que la quantité de temps que vous consacrez à vos études.
- Une bonne connaissance de la physique de base peut s’avérer fort utile pour comprendre les nombreux sujets en chimie organique. Si vous le pouvez, suivez également un cours d’introduction à la physique avant de commencer à suivre les cours de chimie organique.
- Si vous voulez obtenir des instructions détaillées pour des activités en chimie organique, consultez les articles de la catégorie Chimie.
Références
- ↑ http://www.acs.org/content/acs/en/careers/college-to-career/areas-of-chemistry/organic-chemistry.html
- ↑ http://www.ivyroses.com/Chemistry/Organic/How-to-draw-skeletal-formulae-of-organic-molecules.php
- ↑ https://www.wyzant.com/resources/lessons/science/chemistry/electronegativity
- ↑ http://www.masterorganicchemistry.com/2011/01/17/how-to-do-well-in-organic-chemistry-one-students-advice/?_ga=1,219393433,1803543740,1435265508
- ↑ http://www.chemeddl.org/resources/models360/models.php
- ↑ http://www.chemicalforums.com/index.php?board=3,0
- ↑ http://eduscol.education.fr/rnchimie/chi_org/dossiers/default.htm