Tableau périodique des éléments
Le tableau périodique des éléments, également appelé tableau ou table de Mendeleïev, classification périodique des éléments ou simplement tableau périodique, représente tous les éléments chimiques, ordonnés par numéro atomique croissant et organisés en fonction de leur configuration électronique, laquelle sous-tend leurs propriétés chimiques.
La conception de ce tableau est généralement attribuée au chimiste russe Dmitri Ivanovitch Mendeleïev, qui, en 1869, construisit une table, différente de celle qu'on utilise aujourd'hui[alpha 1], mais semblable dans son principe, dont le grand intérêt était de proposer une classification systématique des éléments connus à l'époque en vue de souligner la périodicité de leurs propriétés chimiques, d'identifier les éléments qui restaient à découvrir, voire de prédire certaines propriétés d'éléments chimiques alors inconnus.
Le tableau périodique a connu de nombreux réajustements depuis lors jusqu'à prendre la forme que nous lui connaissons aujourd'hui. Il est devenu un référentiel universel auquel peuvent être rapportés tous les types de comportements physiques et chimiques des éléments. Depuis la mise à jour de l'UICPA du 28 novembre 2016, sa forme standard comporte 118 éléments[1], allant de l'hydrogène 1H à l'oganesson 118Og.
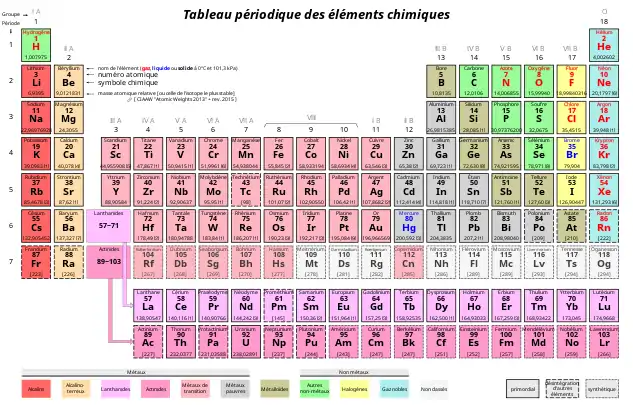 Tableau périodique des éléments au 28 novembre 2016.
Tableau périodique des éléments au 28 novembre 2016..svg.png.webp) Avec davantage de détails par élément.
Avec davantage de détails par élément.
Le tableau périodique standard
Ce tableau est la représentation la plus usuelle de la classification des éléments chimiques. Certains chimistes ont proposé d'autres façons de classer les éléments, mais celles-ci restent bornées au domaine scientifique.
| CAS | I A | II A | III B | IV B | V B | VI B | VII B | VIII B | VIII B | VIII B | I B | II B | III A | IV A | V A | VI A | VII A | VIII A | |
| IUPAC | I A | II A | III A | IV A | V A | VI A | VII A | VIII | VIII | VIII | I B | II B | III B | IV B | V B | VI B | VII B | O | |
| Bloc s | f | Bloc d | Bloc p | ||||||||||||||||
| ↓→ | 1 | 2 | 3[alpha 2] | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | |
| 1 | 1 H |
2 He | |||||||||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | |||||||||||
| 3 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | |||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr | |
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe | |
| 6 | 55 Cs |
56 Ba |
* |
71 Lu |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn |
| 7 | 87 Fr |
88 Ra |
* * |
103 Lr |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og |
| ↓ | |||||||||||||||||||
| Lanthanides | * |
57 La |
58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
||||
| Actinides | * * |
89 Ac |
90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
||||
| Légende | L'abondance naturelle est indiquée par le bord des cases : |
L'état standard à 0 °C et 1 atm | |||||||
| Trait continu | Élément primordial | est indiqué par la couleur du numéro atomique : | |||||||
| 94 Pu |
← Numéro atomique | Tirets épais | Produit de désintégration d'autres éléments | Noir | Bleu | Rouge | Gris | ||
| ← Symbole chimique | Pointillés clairs | Élément synthétique (artificiel) | Solide | Liquide | Gazeux | Inconnu | |||
| Métaux | Non-métaux | ||||||||
| Alcalins | Alcalino- terreux |
Lanthanides | Métaux de transition |
Métaux pauvres |
Métalloïdes | Autres non-métaux |
Halogènes | Gaz nobles |
Éléments non classés |
| Actinides | |||||||||
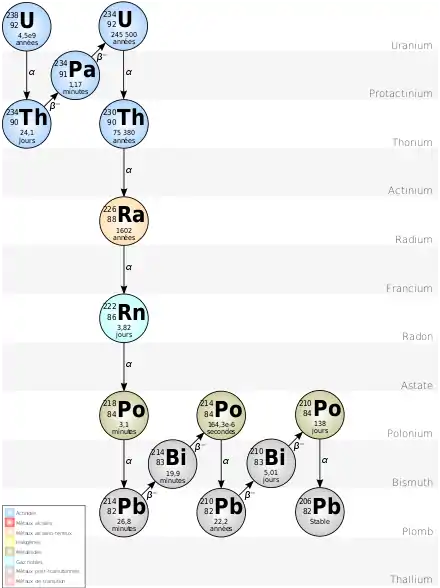
Parmi les 118 éléments chimiques connus, 83 sont dits primordiaux parce qu'ils possèdent au moins un isotope stable ou suffisamment stable pour être plus ancien que la Terre. Parmi eux, trois sont radioactifs : l'uranium 92U, le thorium 90Th et le bismuth 83Bi ; la radioactivité de ce dernier est cependant si faible qu'elle n'a été mise en évidence qu'en 2003[5].
11 éléments existent naturellement dans l'environnement terrestre, mais sont trop radioactifs pour que leurs isotopes présents lors de la formation du Système solaire aient pu subsister jusqu'à nos jours : ils sont formés continuellement par désintégration radioactive d'autres éléments chimiques, principalement de l'uranium et du thorium. C'est par exemple le cas du technétium 43Tc, le plus léger d'entre eux, qui est un produit de fission de l'uranium, ou encore du plutonium 94Pu, le plus lourd d'entre eux, qui est considéré comme un radioisotope naturel présent à l'état de traces dans la pechblende, principal minerai d'uranium. La chaîne de désintégration de l'uranium 238, principal isotope naturel d'uranium, produit ainsi continuellement du protactinium 234Pa, du thorium 234Th et 230Th, du radium 226Ra, du radon 222Rn, du polonium 218Po, 214Po et 210Po, du bismuth 214Bi et 210Bi, et du plomb 214Pb, 210Pb et 206Pb ; ce dernier est stable.
Les 24 derniers éléments sont dits synthétiques, car ils n'existent pas naturellement dans l'environnement terrestre et sont produits artificiellement dans les réacteurs nucléaires ou expérimentalement en laboratoire. On peut cependant trouver certains d'entre eux dans la nature à la suite d'essais nucléaires atmosphériques ou d'accidents nucléaires, comme c'est le cas, dans certaines zones contaminées, pour l'américium 95Am, le curium 96Cm, le berkélium 97Bk et le californium 98Cf. Hors de notre planète, ces éléments, ainsi que l'einsteinium 99Es, sont peut-être produits naturellement par processus r[6] lors d'explosions de supernovae, comme on l'a longtemps pensé de l'isotope 254Cf[7],[8],[9], hypothèse cependant réfutée depuis lors[10] ; ils auraient également été détectés dans le spectre de l'étoile de Przybylski[11].
Parmi les 103 éléments dont l'état standard est connu aux conditions normales de température et de pression (0 °C et 1 atm), 90 sont solides, 11 sont gazeux, et seulement deux sont liquides : le brome 35Br, fondant à −7,2 °C, et le mercure 80Hg, fondant à −38,8 °C ; plusieurs éléments solides ont cependant un point de fusion voisin de la température ambiante, par exemple le francium 87Fr, à 27 °C, le césium 55Cs, à 28,5 °C, le gallium 31Ga, à 29,8 °C, le rubidium 37Rb, à 39,3 °C, ou encore le phosphore blanc 15P, à 44,2 °C.
Construction du tableau
Dans la mesure où les propriétés physico-chimiques des éléments reposent sur leur configuration électronique, cette dernière est sous-jacente à l'agencement du tableau périodique. Ainsi, chaque ligne du tableau, appelée période, correspond à une couche électronique, identifiée par son nombre quantique principal, noté n : il existe sept couches électroniques connues à l'état fondamental, donc sept périodes dans le tableau périodique standard, numérotées de 1 à 7. Chaque période est elle-même scindée en un à quatre blocs, qui correspondent aux sous-couches électroniques, identifiées par leur nombre quantique secondaire, noté ℓ : il existe quatre types de sous-couches électroniques connues à l'état fondamental, notées s, p, d et f (ces lettres viennent d'abréviations utilisées initialement en spectroscopie). Chacune de ces sous-couches contient respectivement 1, 3, 5 et 7 orbitales atomiques, identifiées par leur nombre quantique magnétique, noté mℓ. Enfin, chaque orbitale est occupée par au plus deux électrons, identifiés chacun par leur nombre quantique magnétique de spin, noté ms.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| 1 | H | He | |||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |
| 6 | Cs | Ba | * | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | * * |
Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | |||||||||||||||||||
| * | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | |||||
| * * |
Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | |||||
| Bloc s | Bloc f | Bloc d | Bloc p | ||||||||||||||||
| Blocs du tableau périodique | |||||||||||||||||||
| ℓ=0 | ℓ=3 | ℓ=2 | ℓ=1 | ||||||||||||
| 1s | |||||||||||||||
| 2s | 2p | 2p | 2p | ||||||||||||
| 3s | 3p | 3p | 3p | ||||||||||||
| 4s | 3d | 3d | 3d | 3d | 3d | 4p | 4p | 4p | |||||||
| 5s | 4d | 4d | 4d | 4d | 4d | 5p | 5p | 5p | |||||||
| 6s | 4f | 4f | 4f | 4f | 4f | 4f | 4f | 5d | 5d | 5d | 5d | 5d | 6p | 6p | 6p |
| 7s | 5f | 5f | 5f | 5f | 5f | 5f | 5f | 6d | 6d | 6d | 6d | 6d | 7p | 7p | 7p |
| Orbitales par sous-couches constituant les blocs du tableau périodique. | |||||||||||||||
Chaque électron d'un atome est donc décrit par quatre nombres quantiques, qui vérifient les propriétés suivantes :
- le nombre quantique principal n est un nombre entier naturel non nul : n ≥ 1 ;
- le nombre quantique azimutal ℓ est un nombre entier positif ou nul vérifiant 0 ≤ ℓ ≤ n – 1 ;
- le nombre quantique magnétique mℓ est un nombre entier vérifiant – ℓ ≤ mℓ ≤ ℓ ;
- le nombre quantique magnétique de spin ms vaut – 12 ou + 12, les électrons correspondants étant couramment représentés par les symboles ↓ et ↑.
En vertu du principe d'exclusion de Pauli, selon lequel deux fermions (ici, deux électrons) d'un même système (ici, un même atome) ne peuvent partager le même état quantique, les sous-couches électroniques s, p, d et f ne peuvent contenir chacune qu'au plus 2, 6, 10 et 14 électrons respectivement ; dans le tableau périodique, elles matérialisent ainsi le bloc s, le bloc p, le bloc d et le bloc f, contenant respectivement 2, 6, 10 et 14 éléments par période.
Si l'on respecte la construction du tableau par blocs en fonction des configurations électroniques, l'hélium devrait se trouver au-dessus du béryllium dans la 2e colonne, celle dont les atomes ont une sous-couche externe ns2, et non au-dessus du néon dans la 18e colonne, dont les atomes ont une sous-couche externe np6 ; l'hélium est cependant positionné usuellement dans la 18e colonne, car c'est celle des gaz nobles, dont il fait chimiquement partie.
Règle de Klechkowski
 Ordre indicatif de remplissage des couches et les sous-couches par énergie croissante selon la règle de Klechkowski.
Ordre indicatif de remplissage des couches et les sous-couches par énergie croissante selon la règle de Klechkowski.
Toutes les sous-couches d'une période n'appartiennent pas nécessairement à la même couche électronique : à partir de la 3e période, des sous-couches appartenant à des couches différentes se remplissent sur une même période. En effet, la distribution des électrons sur les différents niveaux d'énergie quantiques autour de l'atome obéit au principe d'Aufbau (« édification » en allemand), selon lequel l'ordre précis des sous-couches électroniques est donné par la règle de Klechkowski : les sous-couches sont remplies afin que les valeurs n + ℓ puis n soient croissantes, avec n le nombre quantique principal et ℓ le nombre quantique azimutal.
Distribution des électrons dans les orbitales atomiques par sous-couche électronique Période Sous-couche Nombres quantiques Nombre quantique magnétique Nombre d'électrons Principal Azimutal -3 -2 -1 0 1 2 3 Sous-couche Période no 1 1s n = 1 ℓ = 0 ↑ ↓ 2 2 no 2 2s n = 2 ℓ = 0 ↑ ↓ 2 8 2p n = 2 ℓ = 1 ↑ ↓ ↑ ↓ ↑ ↓ 6 no 3 3s n = 3 ℓ = 0 ↑ ↓ 2 8 3p n = 3 ℓ = 1 ↑ ↓ ↑ ↓ ↑ ↓ 6 no 4 4s n = 4 ℓ = 0 ↑ ↓ 2 18 3d n = 3 ℓ = 2 ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ 10 4p n = 4 ℓ = 1 ↑ ↓ ↑ ↓ ↑ ↓ 6 no 5 5s n = 5 ℓ = 0 ↑ ↓ 2 18 4d n = 4 ℓ = 2 ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ 10 5p n = 5 ℓ = 1 ↑ ↓ ↑ ↓ ↑ ↓ 6 no 6 6s n = 6 ℓ = 0 ↑ ↓ 2 32 4f n = 4 ℓ = 3 ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ 14 5d n = 5 ℓ = 2 ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ 10 6p n = 6 ℓ = 1 ↑ ↓ ↑ ↓ ↑ ↓ 6 no 7 7s n = 7 ℓ = 0 ↑ ↓ 2 32 5f n = 5 ℓ = 3 ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ 14 6d n = 6 ℓ = 2 ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ ↑ ↓ 10 7p n = 7 ℓ = 1 ↑ ↓ ↑ ↓ ↑ ↓ 6
C'est la succession des sous-couches électroniques de chaque période qui détermine la structure du tableau périodique en blocs, chaque période étant définie par le retour d'une sous-couche s suivant une sous-couche p de la période précédente, avec un nombre quantique principal incrémenté d'une unité.
Exceptions et règle de Hund
La règle de Klechkowski est observée pour plus de 80 % des 103 éléments dont la configuration électronique à l'état fondamental est connue avec précision, mais une vingtaine d'éléments y font exception. L'état fondamental est en effet, par définition, celui dont l'énergie est la plus faible, et le nombre quantique magnétique de spin des électrons entre en jeu pour déterminer cette énergie : plus le spin résultant des électrons d'une orbitale atomique est élevé, plus la configuration de ces électrons sur cette orbitale est stable (règle de Hund). Il s'ensuit que, pour les éléments du bloc d et du bloc f (métaux de transition, lanthanides et actinides), il est énergétiquement moins favorable de suivre la règle de Klechkowski que de favoriser l'occupation impaire des sous-couches les plus externes lorsque la couche d ou f est vide, à moitié remplie ou entièrement remplie, car l'écart d'énergie entre ces sous-couches est inférieur au gain d'énergie induit par la redistribution des électrons de telle sorte que leur nombre quantique magnétique de spin résultant soit le plus élevé — dans le tableau qui suit, les distributions d'électrons irrégulières sont indiquées en gras :
Élément chimique Famille Configuration électronique 24 Cr Chrome Métal de transition [Ar] 4s1 3d5 28 Ni Nickel Métal de transition [Ar] 4s1 3d9 ( * ) 29 Cu Cuivre Métal de transition [Ar] 4s1 3d10 41 Nb Niobium Métal de transition [Kr] 5s1 4d4 42 Mo Molybdène Métal de transition [Kr] 5s1 4d5 44 Ru Ruthénium Métal de transition [Kr] 5s1 4d7 45 Rh Rhodium Métal de transition [Kr] 5s1 4d8 46 Pd Palladium Métal de transition [Kr] 4d10 47 Ag Argent Métal de transition [Kr] 5s1 4d10 57 La Lanthane Lanthanide [Xe] 6s2 5d1 58 Ce Cérium Lanthanide [Xe] 6s2 4f1 5d1 64 Gd Gadolinium Lanthanide [Xe] 6s2 4f7 5d1 78 Pt Platine Métal de transition [Xe] 6s1 4f14 5d9 79 Au Or Métal de transition [Xe] 6s1 4f14 5d10 89 Ac Actinium Actinide [Rn] 7s2 6d1 90 Th Thorium Actinide [Rn] 7s2 6d2 91 Pa Protactinium Actinide [Rn] 7s2 5f2 6d1 92 U Uranium Actinide [Rn] 7s2 5f3 6d1 96 Cm Curium Actinide [Rn] 7s2 5f7 6d1 103 Lr Lawrencium Actinide [Rn] 7s2 5f14 7p1
- ( * ) Le nickel présente en réalité deux configurations électroniques correspondant à des énergies totales qui se recouvrent. Les manuels notent généralement la configuration régulière [Ar] 4s2 3d8, étayée par les données expérimentales, car elle contient le niveau d'énergie le moins élevé. Cependant, c'est la configuration irrégulière [Ar] 4s1 3d9 qui présente l'énergie moyenne la moins élevée des deux, de sorte que cette configuration est souvent retenue dans les calculs.
Périodicité des propriétés chimiques
Le grand intérêt de la classification périodique est d'organiser les éléments chimiques de telle sorte que leurs propriétés physico-chimiques puissent être largement prédites par leur position dans la table. Ces propriétés évoluent différemment selon qu'on se déplace verticalement ou horizontalement dans le tableau.
Périodes et groupes du tableau périodique
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| 1 | H | He | |||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |
| 6 | Cs | Ba | * | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | * * |
Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | |||||||||||||||||||
| * | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | |||||
| * * |
Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | |||||
Tableau périodique des éléments chimiques |
|||||||||||||||||||
Une période désigne une ligne du tableau périodique. Elle se définit par le remplissage progressif des sous-couches électroniques jusqu'à atteindre la sous-couche s de la couche électronique suivante. Les propriétés des éléments varient généralement beaucoup le long d'une période, mais peuvent être localement assez semblables et constituer des familles d'éléments chimiques complètes, notamment dans le bloc d (métaux dits « de transition ») et surtout dans le bloc f (lanthanides sur la 6e période et actinides sur la 7e période).
Un groupe désigne une colonne du tableau périodique. Chacun des 18 groupes du tableau périodique standard constitue souvent un ensemble d'éléments aux propriétés distinctes des groupes voisins, notamment aux extrémités gauche et droite du tableau périodique (c'est-à-dire dans les blocs s et p), où ils se sont vu attribuer des noms d'usage au fil du temps :
- métaux alcalins = groupe 1 (bloc s) excepté l'hydrogène
- métaux alcalino-terreux = groupe 2 (bloc s)
- pnictogènes = groupe 15 (bloc p)
- chalcogènes = groupe 16 (bloc p)
- halogènes = groupe 17 (bloc p)
- gaz nobles = groupe 18 (bloc p) dont l'hélium (bloc s)
Si les termes pnictogène et chalcogène sont aujourd'hui assez désuets, les quatre autres en revanche sont encore très employés car ils se confondent usuellement avec des familles de même nom :
- Groupe 1 : métaux alcalins
- Hormis l'hydrogène, les éléments du premier groupe du tableau périodique constituent la famille des métaux alcalins. Il s'agit de métaux peu denses de couleur argentée et à bas point de fusion, plutôt mous à température ambiante, formant des composés ioniques avec les halogènes et chimiquement très réactifs — ils réagissent violemment avec l'eau pour donner des hydroxydes qui sont des bases fortes — de sorte qu'on ne les trouve jamais sous forme élémentaire dans le milieu naturel.
- Groupe 2 : métaux alcalino-terreux
- Un peu plus durs et plus denses que les métaux alcalins, les métaux alcalino-terreux forment également des composés ioniques avec les halogènes mais ne réagissent pas avec l'eau à température ambiante, seulement avec la vapeur d'eau pour former des hydroxydes très basiques.
- Groupe 17 : halogènes
- Hormis l'astate et le tennesse en bas de la colonne, les éléments du 17e groupe forment la famille des halogènes. Ils existent sous forme élémentaire diatomique et donnent des acides forts avec l'hydrogène. Ils forment des composés ioniques avec les métaux alcalins et les métaux alcalino-terreux. C'est le seul groupe du tableau dont l'état standard des éléments peut être gazeux (fluor, chlore), liquide (brome) ou solide (iode) aux conditions normales de température et de pression (on ignore si le copernicium est gazeux, auquel cas ce serait également vrai pour le 12e groupe).
- Groupe 18 : gaz nobles
- Hormis l'oganesson en bas de la colonne, les éléments du 18e groupe forment la famille des gaz nobles. Aux conditions normales de température et de pression, ce sont des gaz monoatomiques incolores et inodores quasiment dépourvus de réactivité chimique, dont les points de fusion et d'ébullition sont séparés de moins de 10 °C à pression atmosphérique.
Le groupe 3 est un cas particulier dans la mesure où sa composition ne fait pas l'objet d'un consensus parmi les chimistes : si les éléments des périodes 4 et 5 qui le constituent sont toujours le scandium et l'yttrium, ceux des périodes 6 et 7 sont en revanche ou bien le lanthane et l'actinium, ou bien le lutécium et le lawrencium. Cela signifie que la composition des blocs d et f est également variable selon les auteurs, car le groupe 3 fait partie du bloc d. La première option, plaçant le lanthane et l'actinium dans le groupe 3, et donc dans le bloc d, était prépondérante jusqu'au début du siècle, avec, semble-t-il, un renversement de tendance depuis lors ; ce choix relève essentiellement d'une convention : les propriétés chimiques du scandium, de l'yttrium et des 15 lanthanides (lanthane et lutécium compris) sont ainsi suffisamment semblables pour que ces éléments soient collectivement appelés terres rares. De son côté, l'Union internationale de chimie pure et appliquée (IUPAC) a émis en une proposition plaçant le lutécium et le lawrencium dans le groupe 3 comme compromis satisfaisant les principes généraux qui, selon elle, doivent guider la mise en forme du tableau périodique[4].
Variations des propriétés des éléments à travers le tableau
La description quantique de la configuration électronique des atomes permet d'expliquer la similitude des propriétés chimiques au sein d'un groupe par une configuration identique des électrons dans la couche de valence. Le rayon atomique augmente rapidement de haut en bas d'une colonne, car à chaque période s'ajoute une couche électronique. En corollaire, l'énergie d'ionisation et l'électronégativité diminuent, car les électrons périphériques sont moins fortement liés au noyau dans le bas du tableau.
Outre les analyses par lignes et par colonnes, le tableau périodique permet également d'établir des relations diagonales entre certains éléments chimiques des deuxième et troisième périodes qui se trouvent en diagonale les uns par rapport aux autres dans le tableau. Il s'agit toujours de la direction diagonale allant du haut à gauche vers le bas à droite, car parcourir une période vers la droite et descendre le long d'une colonne se traduisent de façon opposée sur la couche de valence des atomes (respectivement, diminution et augmentation du rayon atomique, d'où augmentation et diminution de l'électronégativité). Il s'ensuit certaines similitudes entre éléments diagonaux, qui pourtant ne partagent ni la même période ni le même groupe : la distribution des métalloïdes dans le tableau périodique illustre cet effet.
Rayon atomique
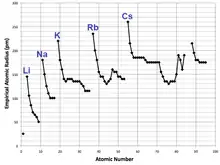
D'une manière générale, le rayon atomique tend à décroître lorsqu'on parcourt une période de gauche à droite, depuis les métaux alcalins jusqu'aux gaz nobles, et à croître lorsqu'on parcourt un groupe de haut en bas. Il croît brutalement lorsqu'on passe d'une période à la suivante, entre le gaz noble d'une période P et le métal alcalin de la période P + 1. Ceci s'explique très bien par les couches électroniques constituant les atomes, et ces observations fournissent des preuves importantes pour l'élaboration et la confirmation des théories de la mécanique quantique.
La décroissance du rayon atomique le long des périodes résulte notamment du fait que la charge électrique du noyau atomique augmente tout au long de chaque période, ce qui accroît l'attraction du noyau sur les électrons et réduit par conséquent le volume des orbitales atomiques. La contraction des lanthanides, observée au cours du remplissage de la sous-couche 4f, illustre très bien ce phénomène : le rayon atomique de l'osmium (élément 76) est quasiment identique à celui du ruthénium (élément 44), qui lui est juste au-dessus dans le tableau. Cette particularité s'observe le long de la 6e période à partir du hafnium (élément 72) jusqu'au platine (élément 78), après lequel elle est masquée par un effet relativiste appelé effet de paire inerte. Un phénomène semblable s'observe également avec le remplissage des sous-couches nd du bloc d, mais est moins marqué que celui observé avec les lanthanides, bien qu'il ait la même origine.
Le tableau ci-dessous présente les rayons de covalence moyens mesurés pour la plupart des atomes, qui illustrent les tendances observées pour les rayons atomiques à travers le tableau périodique :
| H 31 |
He 28 | |||||||||||||||||
| Li 128 |
Be 96 |
B 84 |
C 76 |
N 71 |
O 66 |
F 57 |
Ne 58 | |||||||||||
| Na 166 |
Mg 141 |
Al 121 |
Si 111 |
P 107 |
S 105 |
Cl 102 |
Ar 106 | |||||||||||
| K 203 |
Ca 176 |
Sc 170 |
Ti 160 |
V 153 |
Cr 139 |
Mn 139 |
Fe 132 |
Co 126 |
Ni 124 |
Cu 132 |
Zn 122 |
Ga 122 |
Ge 120 |
As 119 |
Se 120 |
Br 120 |
Kr 116 | |
| Rb 220 |
Sr 195 |
Y 190 |
Zr 175 |
Nb 164 |
Mo 154 |
Tc 147 |
Ru 146 |
Rh 142 |
Pd 139 |
Ag 145 |
Cd 144 |
In 142 |
Sn 139 |
Sb 139 |
Te 138 |
I 139 |
Xe 140 | |
| Cs 244 |
Ba 215 |
* |
Lu 187 |
Hf 175 |
Ta 170 |
W 162 |
Re 151 |
Os 144 |
Ir 141 |
Pt 136 |
Au 136 |
Hg 132 |
Tl 145 |
Pb 146 |
Bi 148 |
Po 140 |
At 150 |
Rn 150 |
| Fr 260 |
Ra 221 |
** |
Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | ||||||||||||||||||
| * |
La 207 |
Ce 204 |
Pr 203 |
Nd 201 |
Pm 199 |
Sm 198 |
Eu 198 |
Gd 196 |
Tb 194 |
Dy 192 |
Ho 192 |
Er 189 |
Tm 190 |
Yb 187 | ||||
| ** |
Ac 215 |
Th 206 |
Pa 200 |
U 196 |
Np 190 |
Pu 187 |
Am 180 |
Cm 169 |
Bk | Cf | Es | Fm | Md | No | ||||
Énergie d'ionisation
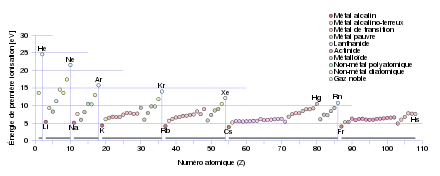
L'énergie d'ionisation, qui correspond implicitement à l'énergie de première ionisation, est l'énergie minimum nécessaire pour retirer un électron à un atome et former un cation. L'électron retiré est le moins lié au noyau atomique et se trouve dans la couche de valence. L'énergie de deuxième ionisation est par conséquent l'énergie nécessaire pour retirer un deuxième électron à l'ion précédemment formé, etc. Pour un atome donné, les énergies d'ionisation successives augmentent avec le degré d'ionisation. Pour le magnésium, par exemple, l'énergie de première ionisation est de 738 kJ·mol-1 pour former le cation Mg+, tandis que l'énergie de deuxième ionisation est de 1 450 kJ·mol-1 pour former le cation Mg2+. Cela s'explique par le fait que les électrons sont d'autant plus liés au noyau qu'ils sont dans des sous-couches intérieures, ce qui explique également que l'énergie de première ionisation croisse quand on se rapproche du haut et de la droite du tableau.
L'énergie d'ionisation fait un bond lorsqu'on tente d'arracher un électron à une configuration électronique de gaz noble, ce qui est par exemple le cas du magnésium ionisé deux fois Mg2+, dont la configuration électronique est très semblable à celle du néon : l'énergie de troisième ionisation passe à 7 730 kJ·mol-1 pour former le cation Mg3+ et correspond à l'arrachement d'un électron de la sous-couche 2p après que les deux électrons de la sous-couche 3s ont été retirés lors des première et deuxième ionisations.
Le tableau ci-dessous représente la première énergie d'ionisation mesurée pour la plupart des éléments, ce qui permet de visualiser les variations de cette grandeur à travers le tableau périodique. On observe en particulier plusieurs minima locaux autour de l'angle inférieur gauche des différents blocs, césium et francium pour le bloc s, actinium pour le bloc f, lawrencium pour le bloc d et thallium pour le bloc p :
| H 13,598 |
He 24,587 | |||||||||||||||||
| Li 5,3917 |
Be 9,3227 |
B 8,298 |
C 11,26 |
N 14,534 |
O 13,618 |
F 17,423 |
Ne 21,565 | |||||||||||
| Na 5,1391 |
Mg 7,6462 |
Al 5,9858 |
Si 8,1517 |
P 10,487 |
S 10,36 |
Cl 12,968 |
Ar 15,76 | |||||||||||
| K 4,3407 |
Ca 6,1132 |
Sc 6,5615 |
Ti 6,8281 |
V 6,7462 |
Cr 6,7665 |
Mn 7,434 |
Fe 7,9024 |
Co 7,881 |
Ni 7,6398 |
Cu 7,7264 |
Zn 9,3942 |
Ga 5,9993 |
Ge 7,8994 |
As 9,7886 |
Se 9,7524 |
Br 11,814 |
Kr 14 | |
| Rb 4,1771 |
Sr 5,6949 |
Y 6,2171 |
Zr 6,6339 |
Nb 6,7588 |
Mo 7,0924 |
Tc 7,28 |
Ru 7,3605 |
Rh 7,4589 |
Pd 8,3369 |
Ag 7,5762 |
Cd 8,9938 |
In 5,7864 |
Sn 7,3439 |
Sb 8,6084 |
Te 9,0096 |
I 10,451 |
Xe 12,13 | |
| Cs 3,8939 |
Ba 5,2117 |
* |
Lu 5,4259 |
Hf 6,825 |
Ta 7,5496 |
W 7,864 |
Re 7,8335 |
Os 8,4382 |
Ir 8,967 |
Pt 8,9587 |
Au 9,2255 |
Hg 10,438 |
Tl 6,1082 |
Pb 7,4167 |
Bi 7,2856 |
Po 8,417 |
At 9,3175 |
Rn 10,749 |
| Fr 4,0727 |
Ra 5,2784 |
** |
Lr 4,9 |
Rf 6 |
Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | ||||||||||||||||||
| * |
La 5,5769 |
Ce 5,5387 |
Pr 5,473 |
Nd 5,525 |
Pm 5,582 |
Sm 5,6436 |
Eu 5,6704 |
Gd 6,1501 |
Tb 5,8638 |
Dy 5,9389 |
Ho 6,0215 |
Er 6,1077 |
Tm 6,1843 |
Yb 6,2542 | ||||
| ** |
Ac 5,17 |
Th 6,3067 |
Pa 5,89 |
U 6,1941 |
Np 6,2657 |
Pu 6,0262 |
Am 5,9738 |
Cm 5,9915 |
Bk 6,1979 |
Cf 6,2817 |
Es 6,42 |
Fm 6,5 |
Md 6,58 |
No 6,65 | ||||
Électronégativité
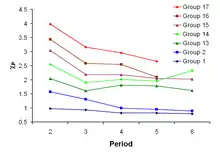
L'électronégativité est une indication de la tendance d'un atome à attirer les électrons. Elle dépend à la fois du numéro atomique et de l'éloignement des électrons de valence par rapport au noyau atomique. Plus l'électronégativité est élevée, plus l'élément attire les électrons. Cette grandeur, déterminée par exemple par l'échelle de Pauling, suit globalement la même tendance que l'énergie d'ionisation : elle croît quand on va vers le haut et vers la droite du tableau, avec un maximum pour le fluor et un minimum pour le francium. Il existe cependant des exceptions à cette règle générale, qui suivent les exceptions à l'évolution du rayon atomique : le gallium et le germanium ont une électronégativité supérieure à celle de l'aluminium et du silicium respectivement en raison de la contraction du bloc d. Les éléments de la 4e période qui viennent immédiatement après les métaux de transition ont des rayons atomiques particulièrement petits, d'où une électronégativité plus élevée. On observe également que les métaux du groupe du platine et les métaux nobles ont une électronégativité particulièrement élevée et croissante vers le bas du tableau, phénomène qu'on observe également le long du groupe no 6.
| H 2,2 |
He | |||||||||||||||||
| Li 0,98 |
Be 1,57 |
B 2,04 |
C 2,55 |
N 3,04 |
O 3,44 |
F 3,98 |
Ne | |||||||||||
| Na 0,93 |
Mg 1,31 |
Al 1,61 |
Si 1,9 |
P 2,19 |
S 2,58 |
Cl 3,16 |
Ar | |||||||||||
| K 0,82 |
Ca 1 |
Sc 1,36 |
Ti 1,54 |
V 1,63 |
Cr 1,66 |
Mn 1,55 |
Fe 1,83 |
Co 1,88 |
Ni 1,91 |
Cu 1,9 |
Zn 1,65 |
Ga 1,81 |
Ge 2,01 |
As 2,18 |
Se 2,55 |
Br 2,96 |
Kr 3 | |
| Rb 0,82 |
Sr 0,95 |
Y 1,22 |
Zr 1,33 |
Nb 1,6 |
Mo 2,16 |
Tc 1,9 |
Ru 2,2 |
Rh 2,28 |
Pd 2,2 |
Ag 1,93 |
Cd 1,69 |
In 1,78 |
Sn 1,96 |
Sb 2,05 |
Te 2,1 |
I 2,66 |
Xe 2,6 | |
| Cs 0,79 |
Ba 0,89 |
* |
Lu 1,27 |
Hf 1,3 |
Ta 1,5 |
W 2,36 |
Re 1,9 |
Os 2,2 |
Ir 2,2 |
Pt 2,28 |
Au 2,54 |
Hg 2 |
Tl 1,62 |
Pb 2,33 |
Bi 2,02 |
Po 2 |
At 2,2 |
Rn 2,2 |
| Fr 0,7 |
Ra 0,9 |
** |
Lr 1,3 |
Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | ||||||||||||||||||
| * |
La 1,1 |
Ce 1,12 |
Pr 1,13 |
Nd 1,14 |
Pm 1,13 |
Sm 1,17 |
Eu 1,2 |
Gd 1,2 |
Tb 1,1 |
Dy 1,22 |
Ho 1,23 |
Er 1,24 |
Tm 1,25 |
Yb 1,1 | ||||
| ** |
Ac 1,1 |
Th 1,3 |
Pa 1,5 |
U 1,38 |
Np 1,26 |
Pu 1,28 |
Am 1,13 |
Cm 1,28 |
Bk 1,3 |
Cf 1,3 |
Es 1,3 |
Fm 1,3 |
Md 1,3 |
No 1,3 | ||||
Affinité électronique
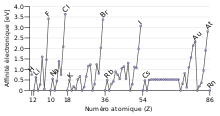
L'affinité électronique d'un atome est la quantité d'énergie libérée lorsqu'un électron est ajouté à un atome neutre pour former un anion. Cette grandeur varie beaucoup d'un élément à un autre, mais des tendances sont perceptibles à travers le tableau périodique, présentant certaines similitudes avec l'électronégativité. Les halogènes présentent la plus forte affinité électronique, très supérieure à celle de tous les autres éléments ; elle est maximum pour le chlore, et non le fluor, à la différence de l'électronégativité.
D'une manière générale, les non-métaux ont une affinité électronique plus positive que celle des métaux, tandis que celle des gaz nobles, réagissant trop peu, n'a pas été mesurée. L'affinité électronique croît généralement le long d'une période, mais il est plus difficile de dégager une tendance le long des groupes : elle devrait décroître en descendant le long d'un groupe puisque les couches de valence sont de moins en moins liées au noyau, mais on observe expérimentalement qu'environ un tiers des éléments échappent à cette tendance, et présentent une affinité électronique supérieure à celle de l'élément situé au-dessus d'eux dans le tableau périodique ; seul le 1er groupe, celui des métaux alcalins, est caractérisé par une décroissance régulière de l'affinité électronique.
Caractère métallique
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| 1 | H | He | |||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |
| 6 | Cs | Ba | * |
Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | * * |
Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | |||||||||||||||||||
* |
La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | |||||
* * |
Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | |||||
| Li | Métaux alcalins | ||||||||||||||||||
| Be | Métaux alcalino-terreux | ||||||||||||||||||
| La | Lanthanides | ||||||||||||||||||
| Ac | Actinides | ||||||||||||||||||
| Sc | Métaux de transition | ||||||||||||||||||
| Al | Métaux pauvres | ||||||||||||||||||
| B | Métalloïdes | ||||||||||||||||||
| C | Non-métaux polyatomiques | ||||||||||||||||||
| O | Non-métaux diatomiques | ||||||||||||||||||
| Ne | Non-métaux monoatomiques | ||||||||||||||||||
| Nh | Nature chimique inconnue | ||||||||||||||||||
En fonction de leurs propriétés physiques et chimiques générales, les éléments peuvent être classés en métaux, métalloïdes et non-métaux :
- les métaux sont généralement des solides brillants très conducteurs susceptibles de former des alliages avec d'autres métaux ainsi que des composés ioniques avec des non-métaux ;
- les non-métaux sont des isolants souvent gazeux susceptibles de former des composés covalents avec d'autres non-métaux et des composés ioniques avec des métaux ;
- les métalloïdes présentent des propriétés intermédiaires entre métaux et non-métaux, et sont situés, dans le tableau, entre ces deux catégories d'éléments.
Plus l'énergie d'ionisation, l'électronégativité et l'affinité électronique sont faibles, plus l'élément a un caractère métallique prononcé. Réciproquement, les éléments pour lesquels ces grandeurs sont élevées sont non métalliques. Les non-métaux se regroupent par conséquent autour de l'angle supérieur droit du tableau (typiquement le fluor et le chlore), tandis que la grande majorité des éléments ont un caractère métallique plus ou moins prononcé, les plus métalliques se regroupant autour de l'angle inférieur gauche (typiquement le francium et le césium). Entre ces deux extrêmes, on a coutume de distinguer parmi les métaux :
- les métaux alcalins, les plus réactifs ;
- les métaux alcalino-terreux, réactifs à un degré moindre que les précédents ;
- les lanthanides et les actinides, dont font partie tous les métaux du bloc f ;
- les métaux de transition, comprenant la majeure partie des métaux du bloc d ;
- les métaux pauvres, dont font partie tous les métaux du bloc p.
Parmi les non-métaux, on peut distinguer, outre les familles conventionnelles :
- les non-métaux polyatomiques, rappelant les métalloïdes et susceptibles de présenter un caractère métallique (carbone graphite et sélénium gris, par exemple) ;
- les non-métaux diatomiques, essentiellement non métalliques hormis dans des conditions particulières (hydrogène métallique et phase ζ de l'oxygène par exemple)
- les non-métaux monoatomiques, qui sont les gaz nobles et sont essentiellement inertes chimiquement.
Familles d'éléments chimiques et autres regroupements
Au-delà des lignes, des colonnes et des diagonales, les éléments sont traditionnellement regroupés en familles aux propriétés physico-chimiques homogènes :
- famille des métaux alcalins, égale au groupe 1, moins l'hydrogène.
- famille des métaux alcalino-terreux, confondue avec le groupe 2.
- famille des lanthanides, égale aux éléments du bloc f de la 6e période, plus le lutécium 71Lu.
- famille des actinides, égale aux éléments du bloc f de la 7e période, plus le lawrencium 103Lr.
- famille des métaux de transition, égale aux éléments du bloc d moins le lutécium 71Lu, le lawrencium 103Lr, les éléments du groupe 12 et certains éléments de la 7e période, mais incluant le copernicium 112Cn.
- famille des métaux pauvres, parfois dits « de post-transition », dont l'étendue peut varier selon les auteurs et qui regroupe les métaux du bloc p ainsi que ceux du groupe 12 hormis le copernicium 112Cn. ;
- famille des métalloïdes, intermédiaires entre métaux et non-métaux ;
- famille des non-métaux, regroupant tous les éléments non métalliques n'appartenant pas aux deux dernières colonnes du tableau ;
- famille des halogènes, comprenant les quatre premiers éléments du groupe 17 ;
- famille des gaz nobles, comprenant les six premiers éléments du groupe 18.
Aux extrémités gauche et droite du tableau, ces familles se confondent à peu près avec les groupes, tandis qu'au centre du tableau elles ont plutôt tendance à se confondre avec les blocs, voire avec les périodes. Ces regroupements d'éléments fondés sur leurs propriétés physiques et chimiques sont par essence imparfaits, car ces propriétés varient souvent de manière assez continue à travers le tableau périodique, de sorte qu'il est fréquent d'observer des recouvrements aux limites entre ces regroupements. Ainsi, le béryllium est toujours classé parmi les métaux alcalins bien que ses oxydes soient amphotères et qu'il présente une tendance marquée à former des composés covalents, deux caractéristiques des métaux pauvres comme l'aluminium. De même, le radon est toujours classé comme gaz noble bien qu'il ne soit pas chimiquement inerte et tende à former des composés ioniques, ce qui le rapproche des métaux.
D'autres regroupements sont également en usage, par exemple :
- les terres rares, qui comprennent le scandium 21Sc, l'yttrium 39Y et les lanthanides ;
- le groupe du platine, qui regroupe les éléments des groupes 7 à 10 des périodes 5 et 6 ;
- la classification géochimique des éléments, qui définit les éléments lithophiles, sidérophiles, chalcophiles et atmophiles ;
- etc.
Limites à la périodicité aux confins du tableau
La configuration électronique des éléments est décrite de façon satisfaisante par le modèle des orbitales atomiques jusqu'au milieu de la 7e période. Pour Z >> 100, des effets relativistes deviennent significatifs sur des électrons en interaction avec un noyau très fortement chargé, certaines corrections induites par l'électrodynamique quantique ne peuvent plus être négligées, les approximations considérant les électrons de façon individuelle pour déterminer les orbitales — approximation du champ central — ne sont plus valides, et des effets de couplage spin-orbite redistribuent les niveaux d'énergie, et donc les sous-couches électroniques. Il s'ensuit que la distribution des électrons autour du noyau devient délicate à modéliser pour ces éléments, et qu'on peut s'attendre à ce que leurs propriétés chimiques soient plus difficiles à prévoir.
Si les propriétés physiques et chimiques de tous les éléments jusqu'au hassium 108Hs sont bien connues, seuls deux éléments de numéro atomique supérieur à 108 ont fait l'objet d'études expérimentales : le copernicium 112Cn et le flérovium 114Fl ; on n'a par conséquent que très peu d'informations sur les propriétés physiques et chimiques des autres éléments de numéro atomique supérieur à 108.
Le copernicium 112Cn, dont les propriétés chimiques ont été particulièrement étudiées, s'est révélé être un homologue plus volatil du mercure et prolonge donc bien le groupe 12[16]. Il peut ainsi être rangé parmi les métaux pauvres comme le mercure, mais il semble également répondre à la définition de l'IUPAC pour les éléments de transition, c'est-à-dire « un élément chimique dont les atomes ont une sous-couche électronique d incomplète, ou qui peuvent former des cations dont la sous-couche électronique d est incomplète[17] » en raison d'effets relativistes stabilisant la sous-couche électronique s au détriment de la sous-couche d : le cation Cn2+ aurait ainsi la configuration électronique [Rn]5f14 6d8 7s2. Le copernicium présente par ailleurs certaines propriétés le rapprochant des gaz nobles[18] et pourrait d'ailleurs être gazeux[19].
Le flérovium, quant à lui, présente des propriétés ambiguës : davantage métal que gaz noble, contrairement à ce que laissaient penser les premiers résultats obtenus en 2008[20], il serait lui aussi volatil, mais plus réactif que le copernicium, et pourrait appartenir, tout comme lui, à une nouvelle famille correspondant à des « métaux volatils », intermédiaires entre métaux et gaz nobles du point de vue de leurs propriétés d'adsorption sur l'or[21] ; dans la mesure où il s'avère chimiquement semblable au plomb, il peut être vu comme un métal pauvre, mais ne peut en toute rigueur être rangé dans une famille d'éléments en l'état actuel de nos connaissances.
Les propriétés de l'oganesson 118Og, qui devrait être un gaz noble en vertu de son positionnement en bas de la 18e colonne du tableau, n'ont pas été étudiées expérimentalement ; des modélisations suggèrent qu'il pourrait peut-être s'agir d'un solide semiconducteur ayant des propriétés évoquant les métalloïdes[16].
Isotopes et radioactivité
Isotopes
Les éléments chimiques sont identifiés dans le tableau périodique par leur numéro atomique, qui représente le nombre de protons que contient leur noyau, mais il peut exister plusieurs atomes différents pour un même élément chimique, différant les uns des autres par le nombre de neutrons dans leur noyau. Dans la mesure où ces atomes occupent la même case dans le tableau périodique, ils sont dits isotopes — avec une étymologie issue du grec ancien ἴσος τόπος signifiant « au même endroit ».
Les isotopes d'un élément ont généralement exactement les mêmes propriétés chimiques, car leur configuration électronique est identique. Mais la masse du noyau étant différente, on observe un effet isotopique d'autant plus prononcé que l'atome est léger. C'est notamment le cas pour le lithium 3Li, l'hélium 2He (du point de vue de ses propriétés physiques) et surtout l'hydrogène 1H.
L'isotope 2H (deutérium) de l'hydrogène est suffisamment différent de l'isotope 1H (protium) pour que l'UICPA admette — mais sans le recommander — l'usage d'un symbole chimique spécifique au deutérium (D) distinct de celui de l'hydrogène (H).
Radioactivité
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| 1 | H | He | |||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |
| 6 | Cs | Ba | * |
Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn |
| 7 | Fr | Ra | * * |
Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | |||||||||||||||||||
* |
La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | |||||
* * |
Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | |||||
| Pb | Un isotope au moins de cet élément est stable | ||||||||||||||||||
| Cm | Un isotope a une période d'au moins 4 millions d'années | ||||||||||||||||||
| Cf | Un isotope a une période d'au moins 800 ans | ||||||||||||||||||
| Md | Un isotope a une période d'au moins 1 journée | ||||||||||||||||||
| Bh | Un isotope a une période d'au moins 1 minute | ||||||||||||||||||
| Og | Tous les isotopes connus ont une période inférieure à 1 minute | ||||||||||||||||||
80 des 118 éléments du tableau périodique standard possèdent au moins un isotope stable : ce sont tous les éléments de numéro atomique compris entre 1 (hydrogène) et 82 (plomb) hormis le technétium 43Tc et le prométhium 61Pm, qui sont radioactifs.
Dès le bismuth 83Bi, tous les isotopes des éléments connus sont radioactifs. L'isotope 209Bi a ainsi une période radioactive valant un milliard de fois l'âge de l'univers. Lorsque la période dépasse quatre millions d'années, la radioactivité produite par ces isotopes devient négligeable et présente à court terme un risque sanitaire très faible : c'est par exemple le cas de l'uranium 238, dont la période est de près de 4,5 milliards d'années et dont la toxicité est avant tout chimique[22],[23],[24], à travers notamment des composés solubles tels que UF6, UO2F2, UO2Cl2, UO2(NO3)2, UF4, UCl4, UO3, certains composés peu solubles tels que UO2 et U3O8 étant quant à eux radiotoxiques[25].
Au-delà de Z = 110 (darmstadtium 281Ds), tous les isotopes des éléments ont une période radioactive de moins de 30 secondes, et de moins d'un dixième de seconde à partir de l'élément 115 (moscovium 288Mc).
Le modèle en couches de la structure nucléaire permet de rendre compte de la plus ou moins grande stabilité des noyaux atomiques en fonction de leur composition en nucléons (protons et neutrons). En particulier, des « nombres magiques » de nucléons, conférant une stabilité particulière aux atomes qui en sont composés, ont été observés expérimentalement, et expliqués par ce modèle[26],[27]. Le plomb 208, qui est le plus lourd des noyaux stables existants, est ainsi composé du nombre magique de 82 protons et du nombre magique de 126 neutrons.
Certaines théories[alpha 4] extrapolent ces résultats en prédisant l'existence d'un îlot de stabilité parmi les nucléides superlourds, pour un « nombre magique » de 184 neutrons et — selon les théories et les modèles — 114, 120, 122 ou 126 protons ; une approche plus moderne montre toutefois, par des calculs fondés sur l'effet tunnel, que, si de tels noyaux doublement magiques sont probablement stables du point de vue de la fission spontanée, ils devraient cependant subir des désintégrations α avec une période radioactive de quelques microsecondes[28],[29],[30], tandis qu'un îlot de relative stabilité pourrait exister autour du darmstadtium 293, correspondant aux nucléides définis par Z compris entre 104 et 116 et N compris entre 176 et 186 : ces éléments pourraient avoir des isotopes présentant des périodes radioactives de l'ordre de la minute.
Extension du tableau périodique
Limite du tableau périodique
On ignore jusqu'à combien de protons et d'électrons un même atome peut contenir. La limite d'observabilité pratique est généralement estimée à au plus Z = 130[31], dans la mesure où l'existence des atomes superlourds se heurte à la limite de stabilité des noyaux[32]. Cela place la fin du tableau périodique peu après l'une des valeurs proposées pour le dernier îlot de stabilité, centré dans ce cas autour de Z = 126.
Richard Feynman releva en 1948 qu'une interprétation simple de l'équation de Dirac semi-relativiste aboutit à une impossibilité pour représenter les orbitales atomiques lorsque le numéro atomique vaut Z > 1⁄α ≈ 137, où α est la constante de structure fine : de tels atomes ne pourraient avoir d'orbitale électronique stable pour plus de 137 électrons, ce qui rendrait impossible l'existence d'atomes électriquement neutres au-delà de 137 protons ; l'élément 137 est depuis lors parfois surnommé « feynmanium »[33]. Le modèle de Bohr donne par ailleurs une vitesse supérieure à celle de la lumière pour les électrons de la sous-couche 1s dans le cas où Z > 137. Une étude plus poussée, prenant notamment en compte la taille non nulle du noyau, montre cependant que le nombre critique de protons pour lequel l'énergie de liaison électron-noyau devient supérieure à 2m0c2, où m0 représente la masse au repos d'un électron ou d'un positron, vaut Zcrit ≈ 173 : dans ce cas, si la sous-couche 1s n'est pas pleine, le champ électrostatique du noyau y crée une paire électron-positron[34],[35], d'où l'émission d'un positron[36] ; si ce résultat n'écarte pas complètement la possibilité d'observer un jour des atomes comprenant plus de 173 protons, il met en lumière un facteur supplémentaire d'instabilité les concernant.
Conjectures au-delà de la 7e période
Au-delà des sept périodes standard, une huitième période est envisagée pour classer les atomes — à ce jour inobservés — ayant plus de 118 protons. Cette huitième période serait la première à posséder des éléments du bloc g, caractérisés à l'état fondamental par des électrons sur une orbitale g. Néanmoins, compte tenu des limites à la périodicité aux confins du tableau — effets relativistes sur les électrons des très gros atomes — qui deviennent significatifs dès le dernier tiers de la 7e période, il est peu probable que la configuration électronique de tels atomes obéisse aux règles observées tout au long des six premières périodes. Il est en particulier délicat d'établir le nombre d'éléments contenus dans ce bloc g : la règle de Klechkowski en prédit 18, mais la méthode de Hartree-Fock en prédit 22.
Le tableau périodique étendu à la huitième période avec 22 éléments dans le bloc g pourrait ainsi présenter l'aspect suivant :
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | 143 | 144 | 145 | 146 | 147 | 148 | 149 | 150 | 151 | 152 | 153 | 154 | 155 | 156 | 157 | 158 | 159 | 160 | 161 | 162 | 163 | 164 | 165 | 166 | 167 | 168 | 169 | 170 | 171 | 172 |
| ↓ | |||||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
Une neuvième période est parfois évoquée, mais, compte tenu de l'incertitude réelle quant à la possibilité d'observer à terme plus d'une dizaine d'éléments nouveaux sur la huitième période, tous les éléments de numéro atomique supérieur à 130 relèvent a priori de la pure extrapolation mathématique. À noter qu'une variante de la table ci-dessus, proposée par Fricke et al. en 1971[37] et revue par Pekka Pyykkö en 2011[38], répartit les 172 mêmes éléments sur 9 périodes, et non 8, en les distribuant de manière non périodique : les éléments 139 et 140 sont ainsi placés entre les éléments 164 et 169, dans le bloc p et non plus dans le bloc g, tandis que les éléments 165 à 168 sont placés sur une 9e période dans les blocs s et p.
Historique
De la toute première tentative de classification des éléments chimiques par Antoine Lavoisier en 1789 au tableau périodique de Glenn Seaborg que nous utilisons aujourd'hui, de nombreux hommes de sciences, issus d'horizons — et parfois de disciplines — différents, ont apporté chacun leur contribution, sur une période de près de deux siècles.
Première classification d'Antoine Lavoisier

C'est en 1789 que le chimiste français Antoine Lavoisier a publié à Paris son Traité élémentaire de chimie, présenté dans un ordre nouveau et d'après les découvertes modernes. Cet ouvrage en deux volumes a jeté les bases de la chimie moderne, en faisant le point sur les connaissances de la fin du XVIIIe siècle dans cette discipline. Il y précise notamment le concept d'élément chimique comme une substance simple qui ne peut être décomposée en d'autres substances, avec en corollaire la loi fondamentale de conservation de la masse de chacune de ces substances simples au cours des réactions chimiques. Il mentionna également le fait que de nombreuses substances considérées comme simples par le passé, se sont révélées être en réalité des composés chimiques (par exemple, l'huile et le sel marin), et il précisa s'attendre à ce qu'on considère sous peu les terres (c'est-à-dire certains minerais) comme des substances composées de nouveaux éléments.
Il publia dans cet ouvrage un tableau récapitulatif des « substances » considérées à son époque comme des éléments chimiques, en prenant soin d'établir une équivalence avec le vocabulaire hérité des alchimistes afin d'éliminer toute ambiguïté. Ce tableau, qui se voulait exhaustif et outil de référence, mentionnait ainsi, parmi les éléments chimiques, la lumière et le feu, encore considérés à cette époque comme des principes « chimiques » bien que Lavoisier lui-même ait invalidé la théorie du phlogistique :
| Noms nouveaux | Noms anciens correspondants | |
| Substances simples qui appartiennent aux trois règnes et qu'on peut regarder comme les éléments des corps[alpha 5] |
Lumière | |
| Calorique |
Chaleur
| |
| Oxygène |
Air déphlogistiqué
| |
| Azote |
Gaz phlogistiqué
| |
| Hydrogène |
Gaz inflammable
| |
| Substances simples non-métalliques oxydables et acidifiables |
Soufre | |
| Phosphore | ||
| Carbone | Charbon pur | |
| Radical muriatique[alpha 6] | Inconnu | |
| Radical fluorique[alpha 7] | Inconnu | |
| Radical boracique[alpha 8] | Inconnu | |
| Substances simples métalliques oxydables et acidifiables |
Antimoine | |
| Argent | ||
| Arsenic | ||
| Bismuth | ||
| Cobalt | ||
| Cuivre | ||
| Étain | ||
| Fer | ||
| Manganèse | ||
| Mercure | ||
| Molybdène | ||
| Nickel | ||
| Or | ||
| Platine | ||
| Plomb | ||
| Tungstène | ||
| Zinc | ||
| Substances simples salifiables terreuses[alpha 9] |
Chaux |
Terre calcaire
|
| Magnésie |
Magnésie
| |
| Barite |
Barote
| |
| Alumine |
Argile
| |
| Silice |
Terre siliceuse
| |
| « Tableau des substances simples » publié par Antoine Lavoisier en 1789[39]. | ||
Les éléments chimiques y sont classés en quatre familles :
- Les éléments impondérables (gaz et autres « essences »)
- Les non-métaux
- Les métaux
- Les « terres », à savoir des minerais (oxydes, sulfates) considérés comme corps simples.
Le chlore est désigné comme « radical muriatique », car Lavoisier considérait que tous les acides étaient des oxoacides — le nom oxygène signifie étymologiquement « formant des acides » — et cherchait donc le « radical » que l'oxygène aurait rendu acide — l'acide muriatique désignait l'acide chlorhydrique, qui ne contient cependant pas d'oxygène.
Cette classification a surtout le mérite de clarifier certaines notions fondamentales, mais ne révèle encore aucune périodicité des propriétés des éléments classés : les métaux sont ainsi recensés tout simplement par ordre alphabétique en français.
Triades de Johann Döbereiner
La première tentative de classification moderne des éléments chimiques revient au chimiste allemand Johann Wolfgang Döbereiner qui, en 1817, nota que la masse atomique du strontium (88) était égale à la moyenne arithmétique des masses atomiques du calcium (40) et du baryum (137), qui ont des propriétés chimiques semblables (aujourd'hui, ils sont classés parmi les métaux alcalino-terreux). En 1829, il avait découvert deux autres « triades » de ce type : celle des halogènes (la masse atomique du brome (80) étant égale à la moyenne arithmétique (81) de celles du chlore (35,5) et de l'iode (127)) et celle des métaux alcalins (la masse atomique du sodium (23) étant égale à la moyenne arithmétique de celles du lithium (7) et du potassium (39)).
D'autres chimistes identifièrent d'autres séries d'éléments, et Leopold Gmelin publia en 1843 la première édition de son Handbuch der Chemie, qui mentionnait des triades, ainsi que trois « tétrades » et une « pentade » — azote, phosphore, arsenic, antimoine et bismuth, que nous connaissons aujourd'hui comme les éléments du groupe 15 du tableau périodique.
Tétrades de Jean-Baptiste Dumas
En 1859, le chimiste français Jean-Baptiste Dumas généralisa les triades de Döbereiner en les étendant en tétrades incluant les éléments les plus légers, définies non plus par les moyennes arithmétiques, mais par une progression similaire d'une tétrade à l'autre, par exemple :
- Fluor = 19 (+ 16,5) Chlore = 35,5 (+ 44,5) Brome = 80 (+ 47) Iode = 127
- Magnésium = 24 (+ 16) Calcium = 40 (+ 48) Strontium = 88 (+ 49) Baryum = 137
Bien qu'en apparence similaire à celle de Döbereiner, l'approche de Dumas était potentiellement bien plus féconde, car applicable de façon pertinente à un bien plus grand nombre d'éléments : alors que les progressions arithmétiques sont restreintes à quelques groupes d'éléments, l'incrément constaté par Dumas entre éléments successifs aux propriétés similaires mesure précisément la longueur de la période qui sépare ces deux éléments — incrément d'environ 16 entre les deux premiers éléments d'une tétrade, puis incrément d'environ 48 entre deuxième et troisième éléments, puis entre troisième et quatrième éléments.
Vis tellurique de Chancourtois
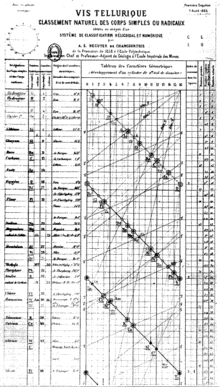
Le premier à remarquer la périodicité des propriétés chimiques des éléments fut le géologue français Alexandre-Émile Béguyer de Chancourtois lorsqu'il classa en 1862 les éléments chimiques alors connus en fonction de leur masse atomique déterminée en 1858 par le chimiste italien Stanislao Cannizzaro. Il normalisa la masse atomique de tous les éléments en prenant celle de l'oxygène égale à 16, et, considérant que « les propriétés des éléments sont les propriétés des nombres » organisa les éléments chimiques en spirale sur un cylindre divisé en seize parties, de telle sorte que les éléments aux propriétés similaires apparaissent l'un au-dessus de l'autre.
Chancourtois remarqua alors que certaines « triades » se retrouvaient précisément alignées dans cette représentation, ainsi que la tétrade oxygène – soufre – sélénium – tellure, qui se trouvait également avoir des masses atomiques à peu près multiples de seize (respectivement 16, 32, 79 et 128). C'est la raison pour laquelle il appela cette représentation « vis tellurique » en référence au tellure. C'était la première ébauche de classification périodique des éléments. Celle-ci ne retint cependant pas l'attention de la communauté scientifique, car Chancourtois n'était pas chimiste et avait employé des termes appartenant plutôt au domaine de la géochimie dans la publication qu'il avait adressée à l'Académie des sciences, laquelle fut éditée de surcroît sans ses schémas explicatifs, ce qui rendit le texte abscons.
D'un point de vue conceptuel, c'était une grande avancée, mais, d'un point de vue pratique, Chancourtois n'avait pas identifié la période correcte pour les éléments les plus lourds, de sorte que, dans sa représentation, une même colonne regroupait le bore, l'aluminium et le nickel, ce qui est correct pour les deux premiers, mais totalement erroné d'un point de vue chimique pour le troisième.
Loi des octaves de John Newlands
Dans la foulée, le chimiste anglais John Alexander Reina Newlands publia en 1863 une classification périodique qui eut, elle, un plus fort retentissement (quoique tardif, et a posteriori), car il avait organisé les premiers éléments alors connus par masse atomique croissante — plus précisément, par masse équivalente croissante — dans un tableau à sept lignes en les arrangeant de telle sorte que leurs propriétés chimiques soient similaires par lignes, sans hésiter à placer deux éléments dans une même case si nécessaire pour éviter de laisser des cases vides par ailleurs.
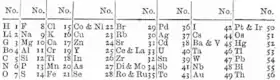
Ce faisant, il avait identifié une nouvelle triade, dont les extrémités étaient le silicium et l'étain, et dont l'élément médian restait à découvrir : il prédit ainsi l'existence du germanium, en lui assignant une masse atomique d'environ 73. Mais la grande faiblesse de son travail était qu'il n'avait pas laissé de case vide dans son tableau pour accueillir notamment le futur germanium : il avait en fait cherché avant tout à classer les éléments connus dans un tableau complet sans chercher de classification plus large tenant compte de possibles éléments à découvrir, qu'il avait pourtant pressentis. De plus, comme Chancourtois, il avait un problème de périodicité, car si les éléments légers connus à l'époque avaient bien une périodicité chimique tous les sept éléments, cela cessait d'être valable au-delà du calcium, et le tableau de Newlands s'avère alors inopérant :
| I. | II. | III. | IV. | V. | VI. | VII. | VIII. | |
|---|---|---|---|---|---|---|---|---|
| 1 | H | F | Cl | Co & Ni | Br | Pd | I | Pt & Ir |
| 2 | Li | Na | K | Cu | Rb | Ag | Cs | Tl |
| 3 | Be | Mg | Ca | Zn | Sr | Cd | Ba & V | Pb |
| 4 | B | Al | Cr | Y | Ce & La | U | Ta | Th |
| 5 | C | Si | Ti | In | Zr | Sn | W | Hg |
| 6 | N | P | Mn | As | Di & Mo | Sb | Nb | Bi |
| 7 | O | S | Fe | Se | Rh & Ru | Te | Au | Os |
| Tableau de John Newlands illustrant la « loi des octaves »[40], 1865. | ||||||||
La mise en évidence d'une périodicité globale jusqu'au calcium était néanmoins une grande avancée, et Newlands présenta cette classification en l'appelant « loi des octaves » par analogie avec les sept notes de musique, mais ce travail fut assez mal accueilli par ses pairs de la Société de chimie de Londres, qui le tournèrent souvent en ridicule et firent obstacle à sa publication ; ce n'est qu'après la publication des travaux de Dmitri Mendeleïev que la qualité de cette analyse a été reconnue.
Notation d'éléments manquants par William Odling
Le chimiste anglais William Odling — secrétaire de la Société de chimie de Londres, et donc rival de Newlands — travaillait également, dans les années 1860, à une table périodique des éléments chimiques remarquablement proche de celle que publierait Mendeleïev en 1869. Elle était organisée en périodes verticales avec des cases vides pour les éléments manquants et plaçait — à la différence du premier tableau de Mendeleïev — le platine, le mercure, le thallium et le plomb dans les bons groupes. Son action négative à l'encontre de Newlands entacha néanmoins définitivement la renommée d'Odling, et sa contribution à l'élaboration du tableau périodique des éléments est aujourd'hui largement méconnue.
Introduction de la valence avec Lothar Meyer
La contribution du chimiste allemand Lothar Meyer est à peine mieux reconnue que celle d'Odling, car ses travaux décisifs ont été publiés après ceux de Mendeleïev alors qu'ils étaient pour la plupart antérieurs. Il publia ainsi une première version de sa classification des éléments en 1864, puis finalisa en 1868 une seconde version plus aboutie qui ne fut intégralement publiée qu'à sa mort, en 1895.
Le premier tableau de Meyer comprenait vingt-huit éléments classés en six familles définies par leur valence : c'était un grand pas en direction de la forme moderne du tableau périodique, organisé en groupes dépendant de la configuration électronique des éléments, elle-même directement en relation avec leur valence ; ce n'était néanmoins pas encore le même tableau qu'aujourd'hui, car les éléments étaient toujours rangés par masse atomique croissante. Le second tableau de Meyer, qui élargissait et corrigeait le premier, fut publié en 1870, quelques mois après celui de Mendeleïev, dont il renforça l'impact sur la communauté scientifique en apportant aux thèses du chimiste russe, encore très contestées, le soutien de travaux indépendants. La grande force de ce travail résidait dans les périodes de longueur variable, avec une disposition des éléments qui permettait d'éviter les regroupements fâcheux de Newlands, tels que le fer, l'or et certains éléments du groupe du platine parmi l'oxygène, le soufre, et les autres éléments du groupe 16 :
| I. | II. | III. | IV. | V. | VI. | VII. | VIII. | IX. |
| B = 11,0 | Al = 27,3 | ? | ?In = 113,4 | Tl = 202,7 | ||||
| ? | ? | ? | ||||||
| C = 11,97 | Si = 28 | ? | Sn = 117,8 | Pb = 206,4 | ||||
| Ti = 48 | Zr = 89,7 | ? | ||||||
| N = 14,01 | P = 30,9 | As = 74,9 | Sb = 122,1 | Bi = 207,9 | ||||
| V = 51,2 | Nb = 93,7 | Ta = 182,2 | ||||||
| O = 15,96 | S = 31,98 | Se = 78 | Te = 128? | ? | ||||
| Cr = 54,4 | Mo = 95,6 | W = 183,5 | ||||||
| ? | F = 19,1 | Cl = 35,38 | Br = 79,75 | I = 126,5 | ? | |||
| Mn = 54,8 | Ru = 103,5 | Os = 198,6 | ||||||
| Fe = 55,9 | Rh = 104,1 | Ir = 196,7 | ||||||
| Co = Ni = 58,6 | Pd = 106,2 | Pt = 196,7 | ||||||
| Li = 7,01 | Na = 22,99 | K = 39,04 | Rb = 85,2 | Cs = 132,7 | ? | |||
| Cu = 63,3 | Ag = 107,66 | Au = 196,2 | ||||||
| ?Be = 9,3 | Mg = 23,9 | Ca = 39,9 | Sr = 87,0 | Ba = 136,8 | ? | |||
| Zn = 64,9 | Cd = 116,6 | Hg = 199,8 | ||||||
| Tableau périodique des éléments chimiques de Julius Lothar Meyer[41], publié en 1870. | ||||||||
Meyer avait également remarqué que si l'on trace une courbe représentant en abscisse la masse atomique et en ordonnée le volume atomique de chaque élément, cette courbe présente une série de maxima et de minima périodiques, les maxima correspondant aux éléments les plus électropositifs.
Classification périodique de Mendeleïev


Malgré la qualité réelle des travaux de ses contemporains, c'est bien au chimiste russe Dmitri Mendeleïev qu'on doit le premier tableau périodique des éléments s'approchant de celui que nous utilisons aujourd'hui, non seulement dans sa forme, mais surtout par la vision qui l'accompagne. À la différence de ses prédécesseurs, Mendeleïev a, en effet, formulé explicitement en quoi son tableau constituait un outil d'analyse théorique des propriétés de la matière :
- Les éléments chimiques, lorsqu'ils sont ordonnés par masse atomique croissante, montrent une périodicité de leurs propriétés chimiques.
- Les éléments qui ont des propriétés chimiques semblables ont soit des masses atomiques semblables (osmium, iridium, platine par exemple), soit des masses atomiques croissantes de façon arithmétique (potassium, rubidium, césium par exemple).
- La disposition des éléments ou des groupes d'éléments dans la table par masse atomique croissante correspond à leur valence et est en rapport, dans une certaine mesure, avec leurs propriétés chimiques.
- Les éléments les plus abondants dans le milieu naturel sont ceux qui ont la plus faible masse atomique.
- La valeur de la masse atomique détermine les propriétés des éléments chimiques.
- La masse atomique de certains éléments devrait parfois être revue, car le tableau est plus cohérent en réarrangeant certains éléments — typiquement, le tellure — sans tenir compte de leur masse atomique expérimentale.
- On doit s'attendre à découvrir des éléments inconnus au moment de la publication de ce tableau, par exemple des éléments analogues à l'aluminium et au silicium, avec une masse atomique comprise entre 65 et 75.
- Il est possible de prédire certaines propriétés des éléments à partir de leur masse atomique.
L'avancée était significative :
- Mendeleïev prédit ainsi l'existence d'une série d'éléments, dont il précisa certaines propriétés, à commencer par leur masse atomique :
- l'eka-bore (44), correspondant au scandium (45), découvert en 1879
- l'eka-aluminium (68), correspondant au gallium (69,7), découvert en 1875 — une réussite particulièrement brillante, car Mendeleïev avait prévu une densité de 6 g/cm3 et un bas point de fusion, les valeurs réelles étant 5,9 g/cm3 et 29,78 °C
- l'eka-silicium (72), correspondant au germanium (72,6), découvert en 1886 — là encore, avec un remarquable accord entre les observations et les propriétés physico-chimiques prédites par Mendeleïev
- l'eka-manganèse (100), correspondant au technétium (99), découvert en 1937
- Il identifia par sa théorie une dizaine d'éléments dont la masse atomique avait été déterminée de façon incorrecte
- Il réorganisa sans le savoir certains éléments en fonction de leur numéro atomique et non de leur masse atomique
Les travaux de Mendeleïev ont été accueillis avec scepticisme par ses pairs, mais la publication subséquente de plusieurs résultats similaires (ceux de John Newlands et de Lothar Meyer en particulier) obtenus de façon indépendante a fait basculer le consensus en faveur de cette nouvelle vision des éléments chimiques.
Découverte de l'argon par William Ramsay et Lord Rayleigh
C'est en voulant mesurer avec précision la masse atomique de l'oxygène et de l'azote par rapport à celle de l'hydrogène que John William Strutt Rayleigh nota une divergence entre la masse atomique de l'azote produit à partir d'ammoniac et celle de l'azote séparé de l'air atmosphérique, légèrement plus lourd. Employant une méthodologie rigoureuse, William Ramsay parvint en 1894 à isoler l'argon à partir de « l'azote » atmosphérique, et expliqua l'anomalie apparente de la masse atomique de l'azote atmosphérique en déterminant la masse atomique de ce nouvel élément, pour lequel rien n'était prévu dans le tableau de Mendeleïev. Sa nature gazeuse et son inertie chimique l'avaient rendu jusqu'alors invisible aux chimistes.
La masse atomique de l'argon (un peu moins de 40) est très voisine de celle du calcium (un peu plus de 40) et donc supérieure à celle du potassium (39,1), ce qui posa quelques problèmes de classification[42], car il semblait y avoir « plus de place » dans le tableau périodique entre le chlore et le potassium qu'entre le potassium et le calcium. Les choses se compliquèrent encore lorsque Ramsay et Morris Travers découvrirent le néon en 1898, matérialisant, avec l'hélium (découvert en 1868 par l'astronome français Jules Janssen et l'Anglais Joseph Norman Lockyer), le groupe nouveau des gaz rares (ou gaz nobles), appelé « groupe 0 » : la masse atomique du néon (20,2) était exactement intermédiaire entre celles du fluor (19) et du sodium (23). Ainsi, les gaz rares semblaient se positionner tantôt entre un métal alcalin et un métal alcalino-terreux, tantôt entre un halogène et un métal alcalin.
Classement par numéro atomique avec Henry Moseley
À la suite de la découverte de l'électron et de celle des isotopes par l'Anglais Joseph John Thomson — qui ont accompagné les débuts de la physique de l'atome avec les travaux de l'Allemand Max Planck, du Néo-Zélandais Ernest Rutherford et du Danois Niels Bohr — les recherches du physicien anglais Henry Moseley sur la corrélation entre la charge du noyau atomique et le spectre aux rayons X des atomes ont abouti en 1913 au classement des éléments chimiques non plus par masse atomique croissante, mais par numéro atomique croissant. C'était une évolution majeure, qui résolvait toutes les incohérences issues du classement en fonction de la masse atomique, lesquelles devenaient gênantes depuis les travaux de systématisation de Dmitri Mendeleïev.
L'argon était ainsi placé entre le chlore et le potassium, et non plus entre le potassium et le calcium, tandis que le cobalt était clairement positionné avant le nickel bien qu'il soit un peu plus lourd. Il confirma que le tellure devait être placé avant l'iode sans nécessiter de revoir sa masse atomique, contrairement à ce qu'avait suggéré Mendeleïev. Il releva également que les éléments de numéro atomique 43 et 61 manquaient à l'appel : l'élément 43 avait déjà été prédit par Mendeleïev comme eka-manganèse (il s'agit du technétium, radioactif, synthétisé en 1937) mais l'élément 61 était nouveau — il s'agit du prométhium, radioactif également, isolé en 1947 :
| O | I | II | III | IV | V | VI | VII | VIII | |||||||||
| A | B | A | B | A | B | A | B | A | B | A | B | A | B | ||||
| 1 H |
|||||||||||||||||
| 2 He |
3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
||||||||||
| 10 Ne |
11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
||||||||||
| 18 Ar |
19 K |
29 Cu |
20 Ca |
30 Zn |
21 Sc |
31 Ga |
22 Ti |
32 Ge |
23 V |
33 As |
24 Cr |
34 Se |
25 Mn |
35 Br |
26 Fe |
27 Co |
28 Ni |
| 36 Kr |
37 Rb |
47 Ag |
38 Sr |
48 Cd |
39 Y |
49 In |
40 Zr |
50 Sn |
41 Nb |
51 Sb |
42 Mo |
52 Te |
(43) |
53 I |
44 Ru |
45 Rh |
46 Pd |
| 54 Xe |
55 Cs |
79 Au |
56 Ba |
80 Hg |
57-71 Ln |
81 Tl |
72 Hf |
82 Pb |
73 Ta |
83 Bi |
74 W |
84 Po |
75 Re |
(85) |
76 Os |
77 Ir |
78 Pt |
| 86 Rn |
(87) |
88 Ra |
89 Ac |
90 Th |
91 Pa |
92 U |
|||||||||||
| 57 La |
58 Ce |
59 Pr |
60 Nd |
(61) |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu | |||
| Structure du tableau périodique des éléments publié en 1913 par Henry Moseley[43]. | |||||||||||||||||
Ce tableau, directement inspiré de celui de John Newlands, constituait l'étape conduisant à la disposition contemporaine. En particulier, la numérotation des groupes avec des chiffres romains de I à VIII, qui remontent à Newlands, et les lettres A et B, introduites par Moseley, étaient encore largement utilisées à la fin du XXe siècle :
| I A | II A | III B | IV B | V B | VI B | VII B | VIII | I B | II B | III A | IV A | V A | VI A | VII A | O | ||
| 1 H |
2 He | ||||||||||||||||
| 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | ||||||||||
| 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | ||||||||||
| 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr |
| 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
(43) |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe |
| 55 Cs |
56 Ba |
57-71 Ln |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
(85) |
86 Rn |
| (87) |
88 Ra |
89 Ac |
90 Th |
91 Pa |
92 U |
(93) |
(94) |
(95) |
(96) |
(97) |
(98) |
(99) |
|||||
| 57 La |
58 Ce |
59 Pr |
60 Nd |
(61) |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu |
|||
| Tableau périodique dans les années 1920-1930, suite aux travaux d'Henry Moseley[44]. | |||||||||||||||||
Il était identique au tableau actuel, hormis pour ce qui avait trait à la septième période.
Concept des actinides de Glenn Seaborg
Le physicien américain Glenn Theodore Seaborg contribua dès 1942 au projet Manhattan dans l'équipe du physicien italien Enrico Fermi. Il était chargé d'isoler le plutonium — que lui-même avait synthétisé et caractérisé en — de la matrice d'uranium au sein de laquelle il se formait. C'est au cours de ce travail qu'il développa une connaissance approfondie de la chimie particulière de ces éléments. Il établit ainsi que leur position dans le tableau périodique (l'uranium était alors placé sous le tungstène et le plutonium sous l'osmium) ne rendait pas compte de leurs propriétés.
En 1944, il parvint à synthétiser et à caractériser l'américium et le curium (éléments 95 et 96), ce qui lui permit de formaliser le concept des actinides, c'est-à-dire d'une nouvelle famille aux propriétés spécifiques et formée des éléments 89 à 103, située sous les lanthanides dans le tableau périodique, qui prit ainsi sa configuration actuelle. Seaborg conjectura également l'existence des superactinides, regroupant les éléments 121 à 153 et situés sous les actinides.
Le tableau périodique utilisé de nos jours est celui remanié en 1944 par Seaborg.
Présentations alternatives
Tableau périodique de Charles Janet
De très nombreuses présentations alternatives du tableau périodique ont été proposées tout au long du XXe siècle, et des présentations graphiques innovantes sont encore régulièrement proposées. L'une des plus anciennes et des plus simples est celle d'un autodidacte français, par ailleurs méconnu, Charles Janet, qui a donné son nom à une disposition du tableau élaborée au début du XXe siècle et récemment redécouverte par les Anglo-saxons, chez lesquels elle est assez bien connue des spécialistes du sujet (sous les noms de Janet Form ou de Left-Step Periodic Table) car elle range les éléments chimiques sur des périodes définies chacune par une valeur de n + ℓ donnée (où n est le nombre quantique principal et ℓ le nombre quantique azimutal) tout en ayant le double mérite de rester familière et de disposer les éléments dans l'ordre naturel des blocs (de droite à gauche), à la différence du tableau usuel :
| f1 | f2 | f3 | f4 | f5 | f6 | f7 | f8 | f9 | f10 | f11 | f12 | f13 | f14 | d1 | d2 | d3 | d4 | d5 | d6 | d7 | d8 | d9 | d10 | p1 | p2 | p3 | p4 | p5 | p6 | s1 | s2 |
| H | He | ||||||||||||||||||||||||||||||
| Li | Be | ||||||||||||||||||||||||||||||
| B | C | N | O | F | Ne | Na | Mg | ||||||||||||||||||||||||
| Al | Si | P | S | Cl | Ar | K | Ca | ||||||||||||||||||||||||
| Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | Rb | Sr | ||||||||||||||
| Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | Cs | Ba | ||||||||||||||
| La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | Fr | Ra |
| Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | 119 | 120 |
| Tableau périodique actuel organisé à la façon de Charles Janet[45]. | |||||||||||||||||||||||||||||||
Autres représentations
Une autre représentation est celle de Theodor Benfey, datée de 1960, dont l'objectif était de remédier aux discontinuités du tableau standard à l'aide d'une représentation en spirale :
 Tableau périodique en spirale de Theodor Benfey.
Tableau périodique en spirale de Theodor Benfey.
De nombreux modèles en trois dimensions ont également été proposés afin d'enrichir la représentation des éléments par diverses informations spécifiques[46].
 Tableau périodique étendu pour définir les propriétés dans le cadre des lanthanides, des actinides, de l'yttrium, le scandium, l'aluminium, le bore, l'hydrogène
Tableau périodique étendu pour définir les propriétés dans le cadre des lanthanides, des actinides, de l'yttrium, le scandium, l'aluminium, le bore, l'hydrogène
Une autre représentation a été proposée par Timmothy Stowe, en losanges par niveaux de remplissage : voir Tableau radial des éléments chimiques.
 Tableau en cupcakes utilisé par Ida Freund en tant qu'outil pédagogique[47].
Tableau en cupcakes utilisé par Ida Freund en tant qu'outil pédagogique[47].
Le tableau de Mendeleïev a été adapté pour représenter d'autres données physiques des éléments, et été appliqué pour visualiser des éléments totalement différents[48].
Usages des éléments de la table dans l'industrie
Jusque dans les années 1970, l'industrie utilisait moins de vingt métaux. Depuis les années 2000, par suite du développement des produits électroniques, des technologies de l'information et de la communication, de l'aéronautique, allié à l'innovation technique dans la recherche de performances et de rendements, la demande en nouveaux métaux « high tech » a explosé, et concerne maintenant environ 60 métaux. Pratiquement tous les éléments de la table sont utilisés jusqu'au no 92 (uranium)[49]. Les réserves de la plupart des métaux au niveau de production 2008 varient de 20 ans à 100 ans[50].
Notes et références
Notes
- Elle était organisée en cinq colonnes (plus l'hydrogène et le lithium) comptant jusqu'à vingt éléments, mais surtout les éléments chimiques y étaient rangés par masse atomique croissante, et non en fonction de leur numéro atomique.
- En fonction des auteurs, le groupe 3 peut également être constitué du lanthane et de l'actinium au lieu du lutécium et du lawrencium représentés ici[2],[3]. En janvier 2021, le groupe de travail de l'IUPAC a proposé la disposition plaçant le lutécium et le lawrencium dans le groupe 3 comme compromis en attendant des conclusions définitives[4].
- La nature d'un élément chimique relève souvent de plusieurs familles d'éléments, dont la répartition représentée ici ne retient que la nature dominante de chaque élément ; la répartition des familles dans le tableau peut varier selon les auteurs, notamment dans la partie droite du tableau.
- Notamment les théories de champ moyen et les théories MM.
- Par cette formule, Lavoisier entendait regrouper les substances « impalpables ».
- Lavoisier désigne ainsi indirectement le chlore.
- Il s'agit du fluor.
- Il s'agit du bore.
- Il s'agissait d'oxydes ou de sulfates d'éléments métalliques pour certains déjà connus de Lavoisier, qui soupçonnait d'ailleurs que certaines de ces « substances simples » fussent en réalité des substances composées de plusieurs éléments différents.
Références
- (en) « IUPAC Periodic Table of the Elements », (consulté le ).
- (en) Eric Scerri, Philip Ball, William Jensen, Laurence Lavelle, Lars R. Ohrström et Guillermo Restrepo, « The constitution of group 3 of the periodic table », (consulté le )
- (en) Eric Scerri avec le groupe de travail de l'IUPAC, « Which Elements Belong in Group 3 of the Periodic Table? », Chemistry International, vol. 38, no 2, , p. 22-23 (DOI 10.1515/ci-2016-0213, lire en ligne)
- (en) Eric Scerri, « Provisional Report on Discussions on Group 3 of The Periodic Table », Chemistry International, vol. 43, no 1, , p. 31-34 (DOI 10.1515/ci-2021-0115, lire en ligne)
- (en) Pierre de Marcillac, Noël Coron, Gérard Dambier, Jacques Leblanc et Jean-Pierre Moalic, « Experimental detection of α-particles from the radioactive decay of natural bismuth », Nature, vol. 422, no 6934, , p. 876-878 (PMID 12712201, DOI 10.1038/nature01541, Bibcode 2003Natur.422..876D, lire en ligne)
- (en) I. V. Panov, I. Yu. Korneev et F.-K. Thielemann, « The r-Process in the region of transuranium elements and the contribution of fission products to the nucleosynthesis of nuclei with A ≤ 130 », Astronomy Letters, vol. 34, no 3, , p. 189-197 (DOI 10.1007/s11443-008-3006-1, Bibcode 2008AstL...34..189P, lire en ligne)
- (en) G. R. Burbidge, F. Hoyle, E. M. Burbidge, R. F. Christy et W. A. Fowler, « Californium-254 and Supernovae », Physical Review, vol. 103, no 5, , p. 1145-1149 (DOI 10.1103/PhysRev.103.1145, Bibcode 1956PhRv..103.1145B, lire en ligne)
- (en) W. Baade, G. R. Burbidge, F. Hoyle, E. M. Burbidge, R. F. Christy et W. A. Fowler, « Supernovae and Californium 254 », Publications of the Astronomical Society of the Pacific, vol. 68, no 403, , p. 296 (DOI 10.1086/126941, JSTOR 40673077, Bibcode 1956PASP...68..296B, lire en ligne)
- (de) St. Temesváry, « Das Element Californium-254 und die Lichtkurven der Supernovae von Typ I. Ein Beitrag zur Frage der Synthese schwerer Elemente im Kosmo », Naturwissenschaften, vol. 44, no 11, , p. 321-323 (DOI 10.1007/BF00630928, Bibcode 1957NW.....44..321T, lire en ligne)
- (en) John G. Conway, E. Kenneth Hulet et Richard J. Morrow, « Emission Spectrum of Californium », Journal of the Optical Society of America, vol. 52, no 2, , p. 222 (DOI 10.1364/JOSA.52.000222, lire en ligne)
- (en) V. F. Gopka, A. V. Yushchenko, V. A. Yushchenko, I. V. Panov et Ch. Kim, « Identification of absorption lines of short half-life actinides in the spectrum of Przybylski’s star (HD 101065) », Kinematics and Physics of Celestial Bodies, vol. 24, no 2, , p. 89-98 (DOI 10.3103/S0884591308020049, Bibcode 2008KPCB...24...89G, lire en ligne)
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, « Covalent radii revisited », Dalton Transactions, no 21, , p. 2832-2838 (DOI 10.1039/B801115J, lire en ligne)
- (en) W. C. Martin et G. W. F. Drake, Wiese, W. L., Atomic, Molecular, & Optical Physics Handbook, Woodbury, American Institute of Physics, , 2e éd. (ISBN 978-1-56396-242-4)
- (en) David R. Lide, section 10 « Atomic, Molecular, and Optical Physics; Ionization Potentials of Atoms and Atomic Ions », CRC Handbook of Chemistry and Physics, 84e édition, CRC Press, Boca Raton, Floride, 2003. (ISBN 0-8493-0484-9)
- (en) S. Rothe, A. N. Andreyev, S. Antalic, A. Borschevsky, L. Capponi, T. E. Cocolios, H. De Witte, E. Eliav, D. V. Fedorov, V. N. Fedosseev, D. A. Fink, S. Fritzsche, L. Ghys, M. Huyse, N. Imai, U. Kaldor, Yuri Kudryavtsev, U. Köster, J. F. W. Lane, J. Lassen, V. Liberati, K. M. Lynch, B. A. Marsh, K. Nishio, D. Pauwels, V. Pershina, L. Popescu, T. J. Procter, D. Radulov, S. Raeder, M. M. Rajabali, E. Rapisarda, R. E. Rossel, K. Sandhu, M. D. Seliverstov, A. M. Sjödin, P. Van den Bergh, P. Van Duppen, M. Venhart, Y. Wakabayashi et K. D. A. Wendt, « Measurement of the first ionization potential of astatine by laser ionization spectroscopy », Nature Communications, vol. 4, , article no 1835 (PMID 23673620, PMCID 3674244, DOI 10.1038/ncomms2819, Bibcode 2013NatCo...4E1835R, lire en ligne)
- (en) Heinz W. Gäggeler et Andreas Türler, « Gas-Phase Chemistry of Superheavy Elements », The Chemistry of Superheavy Elements, , p. 415-483 (DOI 10.1007/978-3-642-37466-1_8, lire en ligne)
- (en) « transition element », IUPAC, Compendium of Chemical Terminology [« Gold Book »], Oxford, Blackwell Scientific Publications, 1997, version corrigée en ligne : (2019-), 2e éd. (ISBN 0-9678550-9-8) :
« Transition element: an element whose atom has an incomplete d sub-shell, or which can give rise to cations with an incomplete d sub-shell. »
- (en) « Chemistry of Hassium », Gesellschaft für Schwerionenforschung mbH, (consulté le )
- (en) « Indication d'un élément 112 gazeux »
- (en) Rapport 2008 du FLNR au JINR : « Chimie des éléments 112 et 114 », p. 87, accédé le 08/07/2009.
- (en) Jens Volker Kratz, « The Impact of Superheavy Elements on the Chemical and Physical Sciences » [PDF], 4th International Conference on the Chemistry and Physics of the Transactinide Elements, (consulté le ).
- (en) Alexandra C. Miller, Michael Stewart, Kia Brooks, Lin Shi et Natalie Page, « Depleted uranium-catalyzed oxidative DNA damage: absence of significant alpha particle decay », Journal of Inorganic Biochemistry, vol. 91, no 1, , p. 246-252 (PMID 12121782, DOI 10.1016/S0162-0134(02)00391-4, lire en ligne)
- (en) Features: Depleted Uranium, sur le site de l'Agence internationale de l'énergie atomique
- (en) Depleted uranium (DU): general information and toxicology, Public Health England, 17 décembre 2007.
- L’uranium, propriétés et toxicité, H. Métivier, L’uranium sous forme appauvrie, SFRP, Paris, 27 novembre 2001.
- (en) W. Groth, « Elementary Theory of Nuclear Shell Structure, von M. Goeppert Mayer und J. H. D. Jensen. John Wiley u. Sons, Inc., New York; Chapman u. Hall, Ltd., London 1955. 1. Aufl. XIV, 269 S., gebd. $ 7.75 », Angewandte Chemie, vol. 68, no 10, , p. 360 (DOI 10.1002/ange.19560681011, lire en ligne)
- (en) Maria Goeppert Mayer & J. Hans D. Jensen, Elementary Theory of Nuclear Shell Structure, John Wiley & Sons Inc., New York, 1955.
- (en) C. Samanta, P. Roy Chowdhury and D.N. Basu, « Predictions of alpha decay half lives of heavy and superheavy elements », Nucl. Phys. A, vol. 789, , p. 142–154 (DOI 10.1016/j.nuclphysa.2007.04.001)
- (en) P. Roy Chowdhury, C. Samanta, and D. N. Basu, « Search for long lived heaviest nuclei beyond the valley of stability », Phys. Rev. C, vol. 77, , p. 044603 (DOI 10.1103/PhysRevC.77.044603, lire en ligne)
- (en) P. Roy Chowdhury, C. Samanta, and D. N. Basu, « Nuclear half-lives for α -radioactivity of elements with 100 < Z < 130 », At. Data & Nucl. Data Tables, vol. 94, , p. 781 (DOI 10.1016/j.adt.2008.01.003)
- (en) Encyclopaedia Britannica : article « Transuranium Element », dont la brève section « End of Periodic Table » en fin d'article situe entre 170 et 210 la borne supérieure théorique du numéro atomique, et à Z ≈ 130 la limite d'observabilité des atomes.
- (en) S. Ćwiok, P.-H. Heenen et W. Nazarewicz, « Shape coexistence and triaxiality in the superheavy nuclei », Nature, vol. 433, no 7027, , p. 705-709 (PMID 15716943, DOI 10.1038/nature03336, Bibcode 2005Natur.433..705C, lire en ligne)
- (en) Hans Eggenkamp, « The Halogen Elements », Advances in Isotope Geochemistry: The Geochemistry of Stable Chlorine and Bromine Isotopes, , p. 3-13 (DOI 10.1007/978-3-642-28506-6_1, lire en ligne)
- (en) CEA Saclay – Spectroscopy of very heavy elements Slide #16 – Limit of stability: positron emission.
- (en) Walter Greiner et Stefan Schramm, « Resource Letter QEDV-1: The QED vacuum », American Journal of Physics, vol. 76, no 6, , p. 509-518(10) (DOI 10.1119/1.2820395, lire en ligne, consulté le ) avec notamment toute une liste de références à consulter sur le thème de l'électrodynamique quantique.
- (en) Yang Wang, Dillon Wong, Andrey V. Shytov, Victor W. Brar, Sangkook Choi, Qiong Wu, Hsin-Zon Tsai, William Regan, Alex Zettl, Roland K. Kawakami, Steven G. Louie, Leonid S. Levitov et Michael F. Crommie, « Observing Atomic Collapse Resonances in Artificial Nuclei on Graphene », Science, vol. 340, no 6133, , p. 734-737 (PMID 23470728, DOI 10.1126/science.1234320, arXiv 1510.02890, lire en ligne)
- (en) B. Fricke, W. Greiner et J. T. Waber, « The continuation of the periodic table up to Z = 172. The chemistry of superheavy elements », Theoretica chimica acta, vol. 21, no 3, , p. 235-260 (DOI 10.1007/BF01172015, lire en ligne)
- (en) Pekka Pyykkö, « A suggested periodic table up to Z ≤ 172, based on Dirac–Fock calculations on atoms and ions », Physical Chemistry Chemical Physics, vol. 13, no 1, , p. 161-168 (PMID 20967377, DOI 10.1039/C0CP01575J, Bibcode 2011PCCP...13..161P, lire en ligne)
- CNRS – Œuvres de Lavoisier : Tableau des substances simples
- On the Law of Octaves : Chemical News volume 12, 18 août 1865, page 83.
- Extrait : Annalen der Chemie, Supplementband, 7, 354 (1870).
- (en) Marco Fontani, Mariagrazia Costa et Mary Virginia Orna, The Lost Elements : The Periodic Table's Shadow Side, New York, Oxford University Press, (1re éd. 2014), 531 p. (ISBN 9780199383344), p. 182.
- Moseley's Periodic Law
- An early history of LBNL by Glenn T. Seaborg : Periodic table before World War II
- WebElements : The Janet Periodic Table.
- The INTERNET Database of Periodic Tables, sur le site meta-synthesis.com
- (en) M Rayner-Canham, Chemistry Was Their Life : Pioneering British Women Chemists, 1880–1949, Londres, Imperial College Press, , 542 p. (ISBN 978-1-86094-986-9, DOI 10.1142/p538, lire en ligne), p. 227
- Exemples : objets (vin, biscuit,...), concepts (Methodes de visualisations) ; et même à l'aide de logiciels (Kalzium)
- Philippe Bihouix et Benoît de Guillebon, Quel avenir pour les métaux ? Raréfaction des métaux : un nouveau défi pour la société, EDP Sciences, p. 24-25
- Philippe Bihouix et Benoît de Guillebon, Quel avenir pour les métaux ? Raréfaction des métaux : un nouveau défi pour la société, EDP Sciences, p. 39
Voir aussi
Articles connexes
Liens externes
- Notices dans des dictionnaires ou encyclopédies généralistes :
- "Mendeleïev, le tableau s'alourdit", La Méthode Scientifique, France Culture, le 26 février 2019
- Le tableau périodique selon le professeur Lovychenko, sur le site de l'université de Genève
- (en) « Le tableau périodique » et le (en) « tableau périodique officiel du 22 juin 2007 » (consulté le ), sur le site de l'union internationale de chimie pure et appliquée
- Animation, applications et recherches liées aux orbitales atomiques responsables du tableau périodique (Université Paris Sud)
- Tableau périodique adapté au niveau lycée (cours de physique chimie, programmes de l'éducation nationale française)
- (en) « The Photographic Periodic Table of the Elements » (consulté le ) : en cliquant sur un élément, on obtient des renseignements déjà détaillés, puis encore plus en cliquant sur Full technical data (qui donne aussi accès à des données détaillées sur chaque isotope).
- « Le tableau de Mendeleïev : 150 ans d’histoire », sur sagascience, site pédagogique du CNRS (consulté le )
- Portail de la chimie