نقص فيتامين بي12
| نقص فيتامين بي12 | |
|---|---|
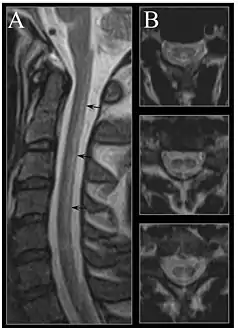 تظهر صورة التصوير بالرنين المغناطيسي للحبل الشوكي العنقي في النقص الشديد في فيتامين بي12 التنكس المشترك تحت الحاد. تظهر صورة التصوير بالرنين المغناطيسي للحبل الشوكي العنقي في النقص الشديد في فيتامين بي12 التنكس المشترك تحت الحاد. | |
| تسميات أخرى | عوز الكوبالامين، فقر دم الكوبالامين |
| معلومات عامة | |
| الاختصاص | طب الجهاز العصبي، أمراض الدم |
| الأسباب | |
| الأسباب | سوء الامتصاص، أنخفاض المدخول، زيادة المتطلبات[1] |
| عوامل الخطر | فقر الدم الخبيث، الإضطرابات الوراثية، التقدم في السن، حمية نباتية، التهاب المعدة الضموري وبعض أمراض الجهاز الهضمي المزمنة الأخرى[2] |
| المظهر السريري | |
| الأعراض | انخفاض القدرة على التفكير، شعور بالتعب، فقر الدم، أحاسيس غير طبيعية، اكتئاب، تهيج، تغييرات في المنعكس[1] |
| المضاعفات | فقر الدم الضخم الأرومات، ضررًا لا رجعة فيه للدماغ والجهاز العصبي[2] |
| الإدارة | |
| الوقاية | المكملات للمعرضين لخطر النقص[2] |
| التشخيص | مستويات في الدم أقل من 150–180 بمول/لتر (200–250 بيكوغرام/مل) عند البالغين[2] |
| العلاج | المكملات عن طريق الفم أو الحقن العضلي[3] |
| الوبائيات | |
| انتشار المرض | 6% (أصغر من 60 سنة)، 20% (أكبر من 60 سنة)[4] |
نقص فيتامين بي12 (بالإنجليزية: Vitamin B12 deficiency) المعروف أيضًا باسم نقص الكوبالامين، هي حالة طبية يكون فيها مستوى الدم والأنسجة أقل من المعتاد من فيتامين بي12.[5] يمكن أن تختلف الأعراض من لا شيء إلى شديدة.[1] عند النقص الطفيف، يمكن أن يكون هناك أعراض قليلة أو معدومة.[1][6] عند النقص المعتدل، شعور بالتعب، فقر الدم، وجع اللسان، تقرحات الفم، ضيق التنفس، شعور بالأغماء، سرعة نبضات القلب، تساقط الشعر، انخفاض ضغط الدم، شحوب الجلد، انخفاض القدرة على التفكير، ألم مفصلي شديد وبدء الأعراض العصبية، بما في ذلك الأحاسيس غير الطبيعية مثل الدبابيس والأبر، الخدران، وطنين الأذن، قد تحدث.[1][6] قد يؤدي النقص الحاد إلى أعراض انخفاض وظائف القلب وظهور الأعراض العصبية الأكثر حدة، بما في ذلك، تغييرات في المنعكس، ضعف وظيفة العضلات، مشاكل الذاكرة، ضبابية الرؤية، الهيجان، المشي غير المستقر، انخفاض التذوق والشم، انخفاض مستوى الوعي، الاكتئاب، الارتباك، القلق، الشعور بالذنب والذهان.[1][7] إذا تركت دون علاج، يمكن أن تصبح بعض هذه التغييرات دائمة.[8] أيضًا قد يحدث العُقم المؤقت، لكنه قابل للعكس مع العلاج.[1][7] عند الرضع خصوصًا النباتيين منهم، يمكن أن يؤدي النقص غير المكتشف وغير المعالج إلى النمو المتدني، انخفاض التطور، وصعوبات في الحركة.[2]
تُصنف الأسباب على أنها ضعف امتصاص فيتامين بي12 من المعدة أو الأمعاء، عدم كفاية المدخول، أو زيادة المتطلبات.[1] عادة ما ترتبط الأسباب بالحالات التي تؤدي إلى ضعف امتصاص فيتامين بي12 كما هو الحال مع التهاب المعدة المناعي الذاتي في فقر الدم الخبيث.[9] تشمل الأسباب الأخرى لإنخفاض الامتصاص إلى الإزالة الجراحية للمعدة، التهاب البنكرياس المزمن، الطفيليات المعوية، بعض الأدوية مثل الاستخدام طويل الأجل لمثبطات مضخة البروتون، حاصرات مستقبلات H2، والميتفورمين، وبعض الاضطرابات الوراثية.[1][10] يمكن أن يحدث عدم كفاية المدخول لدى النباتيين والذين يعانون من سوء التغذية أيضًا.[1][11] قد تحدث المتطلبات المتزايدة على سبيل المثال لدى الأشخاص المصابين بفيروس نقص المناعة البشرية - الإيدز، وأولئك الذين يعانون من قصر عُمر خلايا الدم الحمراء.[1] يعتمد التشخيص عادةً على مستويات فيتامين بي12 في الدم أقل من 150–180 بمول / لتر (200 إلى 250 بيكوغرام / مل) في البالغين.[2] يمكن مُلاحظة مستويات كاذبة طبيعية أو مرتفعة.[12] قد تشير مستويات حمض الميثيل مالونيك المرتفعة أيضًا إلى حدوث النقص.[2] أحيانًا ما يوجد نوع من فقر الدم يُعرف باسم فقر الدم الضخم الأرومات ولكن ليس بصورة دائمة.[2] قد لا يعاني الأفراد المصابون فيتامين بي12 المنخفض أو "الهامشي" في النطاق من 148 إلى 221 بمول / لتر (200–300 بيكوغرام / مل) في البداية من علامات أو أعراض عصبية أو دموية.[2]
يتم العلاج عن طريق مكملات فيتامين بي12، إما عن طريق الفم أو الحقن.[3] في البداية بجرعات يومية عالية، تليها جرعات أقل، تواترًا مع تحسن الحالة.[3] إذا تم العثور على سبب قابل للعكس، فيجب تصحيح هذا السبب إن أمكن.[13] إذا لم يتم العثور على سبب قابل للعكس، أو إذا وجد أنه لا يمكن القضاء عليه، يوصى عادةً بإعطاء فيتامين بي12 مدى الحياة.[14] يمكن الوقاية من نقص فيتامين بي12 عن طريق المكملات الغذائية الذي يوصى به للنباتيون الحوامل ذوات النظام الغذائي النباتي، الجرعات الزائدة غير ضارة عند الآخرين.[2] خطر السمية بسبب فيتامين بي12 منخفض جدًا.[2]
يُقدر أن نقص فيتامين بي12 في الولايات المتحدة والمملكة المتحدة يحدث في حوالي 6% ممن تقل أعمارهم عن 60 عامًا، و20% ممن تزيد أعمارهم عن 60 عامًا.[4] في أمريكا اللاتينية، يُقدر أن حوالي 40% متأثرين، وقد يصل هذا إلى 80% في أجزاء من أفريقيا وآسيا.[1] يعتبر النقص الهامشي أكثر شيوعًا وقد يحدث في ما يصل إلى 40٪ من السكان الغربيين.[2]
الأعراض، العلامات والمضاعفات

يظهر نقص فيتامين بي12 ببطء ويزداد سوءًا بمرور الوقت، ويمكن غالبًا الخلط بينه وبين الحالات الأخرى.[15] قد لا يتم التعرف عليه في كثير من الأحيان، حيث يصبح الجسم مُعتادًا على عدم الشعور بصحة جيدة. عادةً ما يستغرق ظهور النقص سنواتٍ عديدة.[2]
يمكن أن يؤدي نقص فيتامين بي12 إلى فقر الدم، والاضطرابات العصبية والهضمية.[16][17][18] قد لا يتسبب النقص الخفيف بأي أعراض ملحوظة، ولكن عند مستويات أقل من المعتاد، مجموعة من الأعراض، منها الشعور بالتعب، الضعف، الشعور بالأغماء، الدوخة، الصداع، أحمرار اللسان (لسان الكرزة)، برودة اليدين والقدمين، حمى منخفضة الدرجة، الرجفان، عدم تحمل البرد، تنفس سريع، سرعة نبضات القلب، سهولة تعرض الجلد للكدمات أو النزيف، انخفاض ضغط الدم، الشحوب، اضطراب المعدة (عسر الهضم)، الغثيان، فقدان الشهية، حرقة الفؤاد، فقدان الوزن، الإسهال، الإمساك، ألم مفصلي شديد، الشعور بالأحاسيس غير الطبيعية بما في ذلك الخدر والوخز (الدبابيس والأبر) في أصابع اليدين والقدمين، وطنين الأذن، قد تحدث.[16][19][20][21][22] من بين أمور أخرى، قد تترافق علامات وأعراض واسعة أيضًا، بما في ذلك، التهاب الشفة الزاوي، تقرحات الفم، نزف اللثة، ضعف الشعر وتساقطه، الشيب المبكر، مظهر مرهق ودوائر مُظلمة حول العينين، وكذلك أظافر هشة.[6]
في الحالات الأكثر حدة أو طويلة المدى من نقص فيتامين بي12، قد يحدث تلف في الخلايا العصبية.[7] في هذه الحالة، قد تتطور الأعراض، مثل فقد الحس، صعوبة استقبال الحس العميق، المشي غير المستقر (رنح)، ضعف التوازن، ضياع الإحساس في القدمين، ضعف العضلات، ضبابية الرؤية (إما بسبب اعتلال الشبكية[23] أو الاعتلال العصبي البصري[24])، عُسر التبول، مشاكل الخصوبة، أنخفاض حاسة التذوق والشم، انخفاض مستوى الوعي، ضعف المنعكس، الأكتئاب، الهيجان، الارتباك، فقدان الذاكرة، تغيرات المزاج، القلق، الخراقة، الضعف الإدراكي، الذهان، وفي الحالات الأكثر حدة، الخرف.[7][16][25] في بعض الحالات، يمكن أن يتطور نقص فيتامين بي12 بدون فقر الدم.[2] يؤثر نقص الأنسجة سلبًا على الخلايا العصبية، نخاع العظام، والجلد.[5]
يتكون المجمع العصبي، الذي يعرف بأنه التنكس المشترك تحت الحاد للحبل الشوكي[26] وكذلك (النخاع الشوكي الجنيني)، أو النخاع المفصلي[26] من الأعراض التالية:
- ضعف إدراك اللمسة العميقة، الضغط والاهتزاز، فقدان حاسة اللمس، خدر مستمر مزعج جدًا
- ترنح من نوع مسار العمود الظهري
- انخفاض أو فقدان المنعكسات العميقة للوتر العضلي
- مُنعكسات مرضية—بابينسكي، روسوليمو وآخرون، أيضًا، شلل جزئي شديد
يشير وجود الأعراض الحركية المحيطية أو التنكس تحت الحاد للحبل الشوكي إلى وجود نقص في فيتامين بي12 بدلاً من نقص الفولات. إذا لم يتم معالجة حمض الميثيل مالونيك من قبل فيتامين بي12، فإنه يبقى في الغمد المياليني، مسببًا سهولة في الكسر. قد ارتبط الخرف والاكتئاب مع هذا النقص أيضًا، من المحتمل ان يكون السبب من نقص في إنتاج الميثيونين بسبب عدم توافر القدرة لتحويل هوموسيستين إلى هذا المنتج. يعد الميثيونين عاملًا مساعدًا مهمًا في إنتاج العديد من الناقلات العصبية. يمكن أن تحدث كل من هذه الأعراض إما بمفردها أو مع أعراض أخرى. فيتامين بي12 ضروري لنمو الدماغ.[8] يمكن أن يسبب نقصه مشاكل في النمو العصبي يمكن عكسها جزئيًا بالعلاج المبكر.[27] قد لا تنعكس أعراض تلف الخلايا العصبية بعد تصحيح اضطرابات الدم إذا لم يتم عكس النقص مبكرًا. تم العثور على مجموعة فرعية صغيرة فقط من حالات الخرف يمكن عكسها باستخدام فيتامين بي12.[28] وأيضًا يترافق الطنين مع نقص فيتامين بي12 في الدم.[29]
قد يصاحب نقص فيتامين بي12 بعض اضطرابات الأكل أو الحمية الغذائية التقييدية.[30]
فقر الدم الخبيث
فقر الدم الخبيث هو مرض يحدث بسبب استجابة المناعة الذاتية التي تنتج أجسامًا مضادة تهاجم الخلايا الجدارية في بطانة المعدة وتمنعها من خلق العامل الجوهري الضروري لإمتصاص فيتامين بي12.[1][6] يعتبر السبب الرئيسي والأكثر شيوعًا لفقر الدم الناجم عن نقص فيتامين بي12 في البلدان المتقدمة،[2] حيث يتميز بثلاث من الأعراض الرئيسية:
- فقر الدم المصحوب بداء الأرومة الضخم في نخاع العظم (فقر الدم الضخم الأرومات). هذا بسبب تثبيط تخليق الحمض النووي (خصوصًا، البيورينات والثيميدين).
- أعراض الجهاز الهضمي: تغير في حركة الأمعاء، مثل الإسهال الخفيف أو الإمساك، وفقدان السيطرة على المثانة أو الأمعاء.[31] يُعتقد أن هذه ناتجة عن خلل في تخليق الحمض النووي الذي يمنع التكاثر في موقع به معدل دوران مرتفع للخلايا. قد يكون هذا أيضًا بسبب هجوم المناعة الذاتية على الخلايا الجدارية للمعدة في فقر الدم الخبيث. هناك ارتباط مع "المعدة البطيخة" (توسع أوعية غار المعدة) وفقر الدم الخبيث.[32]
- أعراض عصبية: قصور حسي أو حركي (انعكاسات غائبة، اهتزاز ضعيف أو إحساس بلمسة ناعمة)، تنكس مشترك تحت حاد في النخاع الشوكي، أو النوبات.[33][34][35] تشمل أعراض النقص لدى الأطفال التأخر في النمو، التراجع، التهيج، اضطرابات الحركة، ونقص التوتر.[36]
يمكن أن يظهر عدد من الأعراض العصبية عند الأطفال بسبب سوء التغذية أو فقر الدم الخبيث لدى الأم.[37] تشمل ضعف النمو، اللامبالاة، عدم الرغبة في الطعام، والتراجع في النمو. بينما تحل معظم الأعراض بالمكملات، فقد تستمر بعض المشكلات التنموية والمعرفية.[38][39]
المخاطر الأيضية في النسل
فيتامين بي12 هو عنصر غذائي دقيق مهم ضروري لدعم الطلبات الأيضية المتزايدة للجنين أثناء الحمل.[40] نقص فيتامين بي12 لدى النساء الحوامل شائع بشكل متزايد[40] وقد ثبت أنه يرتبط بآثار صحية كبيرة على صحة الأم، بما في ذلك زيادة السمنة،[40] وارتفاع مؤشر كتلة الجسم (BMI)،[40] مقاومة الأنسولين،[40] سكري الحمل، وسكري النوع 2 (T2D) في وقت لاحق من الحياة. وجدت دراسة أجريت على السكان البيض الحوامل غير المصابين بمرض السكري في إنجلترا أنه مقابل كل زيادة بنسبة 1٪ في مؤشر كتلة الجسم، كان هناك انخفاض بنسبة 0.6٪ في تعميم فيتامين بي12.[40] علاوة على ذلك، أظهرت دراسة أجريت على الحيوانات في النعاج أن اتباع نظام غذائي مقيد بي12 وحمض الفوليك والميثيونين حول الحمل، أدى إلى ذرية ذات نسبة أعلى من السمنة وضغط الدم ومقاومة الأنسولين والتي يمكن أن تفسر أنماط مثيلة الحمض النووي المتغيرة.
يشارك كل من فيتامين بي12 وحمض الفوليك في دورة التمثيل الغذائي للكربون الواحد. في هذه الدورة، يعتبر فيتامين بي12 عاملاً مساعدًا ضروريًا لميثيونين سينثيز، وهو إنزيم يشارك في مثيلة الهوموسيستين إلى ميثيونين. تشارك مثيلة الحمض النووي في عمل الجينات وهي آلية أساسية للتحكم في الوراثة اللاجينية في الثدييات. تعتمد هذه المثيلة على المتبرعين بالميثيل مثل فيتامين بي12 من النظام الغذائي.[41] نقص فيتامين بي12 لديه القدرة على التأثير على أنماط المثيلة في الحمض النووي، إلى جانب عوامل التخلق الأخرى مثل الميكرو (RNAs)، مما يؤدي إلى التعبير المتغير للجينات.[42] وبالتالي، يمكن للتعبير الجيني المتغير أن يؤدي إلى ضعف نمو الجنين وبرمجة الأمراض غير المعدية.[42][43]
يرتبط فيتامين بي12 وحالة الفولات أثناء الحمل بزيادة مخاطر انخفاض الوزن عند الولادة،[40] الولادة المبكرة،[40] مقاومة الأنسولين والسمنة[40] في النسل. بالإضافة إلى ذلك، فقد ارتبط بنتائج عكسية للجنين وحديثي الولادة بما في ذلك عيوب الأنبوب العصبي (NTDs)[44][45] وتأخر تكوّن النخاع أو إزالة الميالين.[46] يمكن أن تكون حالة الأم من فيتامين بي12 مهمة في تحديد الحالة الصحية اللاحقة للطفل، كما هو موضح في دراسة Pune لتغذية الأمهات، التي أجريت في الهند. في هذه الدراسة، أدت الأمهات اللواتي لديهن تركيزات عالية من حمض الفوليك وتركيزات منخفضة من فيتامين بي12 إلى زيادة نسبة السمنة ومقاومة الأنسولين لدى الأطفال في سن السادسة. خطر الإصابة بالسكري الحملي ولاحقًا عند الأمهات.[40]
فقر الدم
يعتبر نقص فيتامين بي12 من العوامل الأساسية المؤدية لظهور فقر الدم.[17] في البلدان التي يشيع فيها نقص فيتامين بي12، يفترض عمومًا أن هناك خطرًا أكبر للإصابة بفقر الدم. ومع ذلك، فإن المساهمة الإجمالية لنقص فيتامين بي12 في حدوث فقر الدم على الصعيد العالمي قد لا تكون كبيرة، إلا في حالات ضعف الامتصاص، كبار السن، النباتيين، وبعض الإضطرابات الوراثية. عندما يكون عدد خلايا الدم الحمراء أقل من المعتاد لا تحصل أنسجة الجسم وأعضائه على كمية كافية من الأكسجين، تعرف هذه الحالة بفقر الدم.[9] يتميز فقر الدم الضخم الأرومات الناجم عن نقص فيتامين بي12 بخلايا دم الحمراء التي تكون أكبر من الطبيعي وغير قادرة على إيصال الأكسجين إلى أعضاء الجسم.[9][47] تشير هذه الحالة السريرية إلى تخليق متغير للحمض النووي، حيث يعتبر فيتامين بي12 ضروري لإنتاج ونُضج خلايا الدم الحمراء في نخاع العظم.[47] عادة، مايبلغ المرضى البالغون إلى العناية الطبية عن الأعراض المتعلقة بفقر الدم، مثل الشعور بالتعب والضعف، ضيق التنفس، عدم تحمل المجهود، الشعور بالأغماء، الصداع، الشحوب، جفاف الشفاه واضطراب التذوق.[9][21] يعتبر فقر الدم الخبيث السبب الأكثر شيوعًا لفقر الدم الناجم عن نقص فيتامين بي12 لدى البالغين، الذي يعتمد على عدم كفاية امتصاص فيتامين بي12 بسبب نقص أو فقدان العامل الجوهري.[9] هناك عدد قليل نسبيًا من الدراسات التي قيمت تأثير تدابير أمراض الدم استجابةً لمكملات فيتامين بي12. ذكرت إحدى الدراسات التي أجريت على 184 طفلاً رضيعًا، أن الأفراد الذين يُعطون حقنًا شهرية بفيتامين بي12 (100 ميكروغرام) أو يتناولون مكملات من فيتامين بي12 وحمض الفوليك (100 ميكروغرام / يوم)، كانت لديهم تركيزات أعلى من الهيموجلوبين بعد 10–12 أسبوعًا، مقارنة بالأشخاص الذين يتناولون فقط حمض الفوليك أو أولئك الذين لا يأخذون حقن فيتامين بي12.[48] في النساء البالغات المكسيكيات اللواتي يعانين من نقص في مرحلة ما قبل المدرسة، وجد أن مكملات فيتامين بي12 لم تؤثر على أي متغيرات دموية.[49][50]
التدهور العصبي
يرتبط النقص الحاد في فيتامين بي12 بالتنكس المشترك تحت الحاد في النخاع الشوكي، والذي ينطوي على إزالة الميالين من الأعمدة الخلفية والجانبية للحبل الشوكي.[51] تشمل الأعراض ضعف الذاكرة والإدراك، الفقدان الحسي، الاضطرابات الحركية، ضياع الإحساس بالقدمين، فقدان وظائف العمود الخلفي، والاضطرابات في استقبال الحس العميق.[52][53] في المراحل المتقدمة من نقص فيتامين بي12، لوحظت حالات الذهان وجنون العظمة والاكتئاب الشديد، مما قد يؤدي إلى إعاقة دائمة إذا تركت دون علاج.[52][53] وقد أظهرت الدراسات الانعكاس السريع للأعراض العصبية لنقص فيتامين بي12، بعد العلاج بجرعة عالية من مكملات فيتامين بي12؛ مما يشير إلى أهمية العلاج الفوري في عكس المظاهر العصبية.[54]
التدهور المعرفي
تشمل المظاهر النفسية لنقص فيتامين بي12 الهلوسة، الهيجان، تغيرات في الشخصية، الجنون، انخفاض القدرة المعرفية (مثل انخفاض الذاكرة والإدراك)، الاكتئاب والخرف.[55][56][57][58] يتم وصف هذه المشاكل من خلال آليات مختلفة مثل الإنتاج المختل للناقلات العصبية وارتفاع مستويات الهموسيستين وحمض الميثيل مالونيك (MMA). تشمل الأعراض عند الرضع الهيجان، اخفاق في النمو، اللامبالاة، الأعياء، فقدان الشهية، وتراجع في التطور.[59][38] عندما لا يكون هناك سبب واضح آخر للاضطرابات النفسية، يجب النظر في الفحص والمكملات الغذائية بفيتامين بي12.[60]
هشاشة العظام
من الممكن أن تكون هشاشة العظام مرتبطة بأنخفاض تركيز فيتامين بي12 في الدم.[61][62] وجدت الدراسات الحديثة وجود صلة بين ارتفاع tHcy البلازما وزيادة خطر الإصابة بكسور العظام، ولكن من غير المعروف ما إذا كان هذا مرتبطًا بزيادة مستويات tHcy أو بمستويات فيتامين بي12 (التي تشارك في استقلاب الهوموسيستين).[63]
بالنظر إلى أنه تم العثور على ضعف تمعدن العظام لدى الأفراد الذين يعانون من فقر الدم الخبيث،[64] وأن محتوى فيتامين بي12 داخل خلايا العظام في الأدبيات الطبية قد أظهر أنه يؤثر على عمل خلايا تكوين العظام (الأرومات العظمية)؛[65] من الممكن أن يرتبط نقص بي12 سببيا بسوء صحة العظام.
أسفرت تجارب التدخل العشوائية التي تحقق في ارتباط مكملات بي12 وصحة العظام عن نتائج مختلطة - حيث وجدت دراستان تأثيرات إيجابية بين مكملات فيتامينات ب على كثافة العظام على المرضى المعرضين لخطر الإصابة بهشاشة العظام والذين يعانون من فرط الهوموسستئين في الدم.[66][67] ومع ذلك، لم يلاحظ أي تحسن في كثافة المعادن بالعظام في مجموعة من كبار السن الأصحاء.[68] علاوة على ذلك، هناك حاجة لتجارب أكثر تأكيدًا لتأثير وآليات نقص فيتامين بي12 على تمعدن العظام.
الأسباب
لا يمكن لجسم الإنسان أن يُنتج فيتامين بي12، ويجب الحصول عليه من النظام الغذائي. عندما يتم تناول الأطعمة التي تحتوي على فيتامين بي12، فعادة ما يرتبط الفيتامين بالبروتين ويتم إطلاقه بواسطة البروتياز الذي يفرزه البنكرياس في الأمعاء الدقيقة. بعد إطلاقه، يتم امتصاص معظم فيتامين بي12 في اللفائفي الجزء الأخير من الأمعاء الدقيقة، بعد الارتباط ببروتين يعرف باسم العامل الجوهري. تُصنف الأسباب الناجمة عن نقص فيتامين بي12 على أنها عدم كفاية الإمتصاص، عدم كفاية المدخول الغذائي أو زيادة المتطلبات.[1] عدم كفاية المدخول الغذائي أقل شيوعًا، حيث يُمكن للكبد تخزين مايكفي من فيتامين بي12 لمدة ثلاث إلى خمس سنوات في ظل الظروف الطبيعية.[17]
سوء الإمتصاص
- يؤدي ضعف امتصاص فيتامين بي12 إلى فقر الدم الخبيث وهو نوع من فقر الدم الضخم الأرومات. يأتي فقر الدم الخبيث من نقص العامل الجوهري في المعدة الذي تنتجه الخلايا الجدارية في المعدة، والمطلوب في اللفائفي لامتصاص فيتامين بي12. يعتبر فقر الدم الخبيث السبب الأكثر شيوعًا لنقص فيتامين بي12.[69][70] يمكن أن يؤدي أي اضطراب يؤدي إلى فقدان الخلايا الجدارية إلى ضعف الامتصاص، ويشمل التهاب المعدة الضموري، وهي حالة ايضًا ما تؤثر على كبار السن،[71] وجراحات المعدة التي تنطوي على إزالة كل أو جزء من المعدة، مثل جراحة المجازة المعدية على شكل-Y. تؤدي الإزالة الجراحية للأمعاء الدقيقة كما هو الحال في مرض كرون إلى متلازمة الأمعاء القصيرة وعدم القدرة على امتصاص بي12. يمكن أن ينتج ضعف الامتصاص أيضًا عن متلازمة العروة العمياء حيث تمتص البكتيريا في الأمعاء الدقيقة الفيتامين.[72] بعض أنواع العدوى مثل داء الجيارديات،[73] وداء العوساء التي تسببها الطفيليات يمكن أن تسبب أيضًا سوء الامتصاص.[74]
- يمكن أن تسبب أشكال فقد حمض المعدة (بما في ذلك تلك المستحثة صناعيًا بواسطة الأدوية مثل مثبطات مضخة البروتون ومضادات مستقبلات الهيستامين 2) سوء امتصاص بي12 من الأطعمة، لأن الحمض ضروري لفصل بي12 عن بروتينات الطعام وبروتينات اللعاب الملزمة.[75] يُعتقد أن هذه العملية هي السبب الأكثر شيوعًا لانخفاض فيتامين بي12 لدى كبار السن، والذين غالبًا ما يكون لديهم درجة معينة من الكلورهيدريا دون أن تكون منخفضة رسميًا في العامل الجوهري، لا تؤثر هذه العملية على امتصاص كميات صغيرة من فيتامين بي12 في المكملات الغذائية مثل الفيتامينات المتعددة، لأنها لا ترتبط بالبروتينات، كما هو الحال مع فيتامين بي12 في الأطعمة.[76]
- قد يُساهم الاستخدام طويل الأمد لهيدروكلوريد الرانيتيدين في نقص فيتامين بي12.[77]
- اضطراب جيني، يمكن أن يكون نقص ترانسكوبالامين الثاني سببا.[78]
- قد يتداخل دواء السكري ميتفورمين مع امتصاص فيتامين بي12 الغذائي.[79]
- مرض حساسية القمح غير المعالج، قد يسبب أيضًا في ضعف امتصاص الفيتامين، ربما بسبب تلف الغشاء المخاطي للأمعاء الدقيقة. في بعض الأشخاص، قد يستمر نقص فيتامين بي12 على الرغم من العلاج بنظام غذائي خال من الغلوتين وتتطلب مكملات غذائية.[80]
- إساءة استخدام لأكسيد النيتروز، والاستخدام الترفيهي.[81]
- التعرض المزمن للقوالب السامة والسموم الفطرية الموجودة من المياه الموجودة في المباني المتضررة.[82]
- ارتبط نقص فيتامين بي12 الناجم عن العدوى لفترات بواسطة جرثومة المعدة (هيليكوباكتر بيلوري) بشكل إيجابي بإيجابية CagA والنشاط الالتهابي في المعدة، بدلا من ضمور المعدة.[83]
عدم كفاية المدخول

يحصل الجسد عادةً على ما يكفي من فيتامين بي12 من الأطعمة ذات المصادر الحيوانية. يمكن أن يؤدي عدم كفاية المدخول الغذائي من المنتجات الحيوانية مثل البيض، اللحوم، الحليب، الأسماك، الطيور (وبعض أنواع الطحالب الصالحة للأكل) إلى حالة النقص.[84][85] يتعرض الخضريين، وبدرجة أقل النباتيين، لخطر الإصابة بنقص فيتامين بي12 إذا لم يستهلكوا مكملات غذائية أو أطعمة مدعمة بالفيتامينات.[76] يتعرض الأطفال لخطر أكبر للإصابة بنقص فيتامين بي12 بسبب عدم كفاية المدخول الغذائي، حيث يكون لديهم مخزون أقل من الفيتامينات واحتياج أكبر نسبيًا من الفيتامينات لكل سعرة حرارية من الطعام.[86][87]
زيادة المُتطلبات
يمكن أن تحدث زيادة احتياجات الجسم بسبب الإيدز وانحلال الدم (انهيار خلايا الدم الحمراء) - مما يحفز زيادة إنتاج الخلايا الحمراء.
الآلية
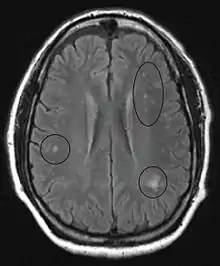
فسيولوجي
تتراوح الكمية الإجمالية لفيتامين بي12 المخزنة في الجسم بين 2 و5 ملليغرامات لدى البالغين. يتم تخزين ما يقارب 50٪ في الكبد، ولكن يتم فقدان ما يقرب من 0.1٪ كل يوم، بسبب الإفرازات في الأمعاء—لا يتم إعادة امتصاص كافة الفيتامين الموجود في الأمعاء. في حين أن الصفراء هي الوسيلة الرئيسية لإفراز بي12، يتم إعادة تدوير معظم هذا عن طريق الدورة الدموية المعوية الكبدية. نظرًا للكفاءة القصوى لهذه الآلية، يمكن للكبد تخزين ما يكفي من فيتامين بي12 لمدة ثلاثة إلى خمس سنوات في ظل ظروف طبيعية وفاعلة الوظيفة.[88] ومع ذلك، فإن تغير معدل مستويات فيتامين بي12 عند انخفاض التناول الغذائي يعتمد على التوازن بين متغيرات عديدة.[89]
أيضي
يسبب نقص فيتامين بي12 تغيرات محددة لأيض مادتين ذات صلة بالمعالجة السريرية عند البشر:
- الهوموسيستين (الهوموسيستين إلى الميثيونين، يحفزه سينسيز الميثيونين) مما يؤدي إلى فرط هوموسيستين الدم الذي يؤدي إلى الدوالي الوريدية.
- حمض الميثيل مالونيك (ميثيل مالونيل التميم A إلى سكسينيل التميم A، والتي يتم إنتاج ميثيل مالونيل التميم A من حمض الميثيل مالونيك في تفاعل سابق)
يتم تنشيط الميثيونين إلى S-adenosyl-الميثيونين، الذي يساعد في تخليق البيورين، الثيميدين، إنتاج المايلين، والبروتين/الناقلات العصبية/الأحماض الدهنية/إنتاج الدهون الفوسفورية ومثيلة الحمض النووي. يزود 5-ميثيل رباعي هيدروفولات مجموعة ميثيل، التي يتم تحريرها إلى التفاعل مع الهوموسيستين، منتجة الميثيونين. يحتاج هذا التفاعل إلى كوبالامين كعامل مساعد. إنتاج 5- ميثيل رباعي هيدروفولات هو تفاعل غير عكسي. إذا كان هنالك غياب لفيتامين بي12 فإن التفاعل الأمامي من الهوموسيستين إلى الميثيونين لا يحدث، ويتم توقيف تجديد رباعي هيدروفولات.[90] بسبب مشاركة فيتامين بي12 والفولات (ملح حمض الفوليك) في أيض الهوموسيستين، فإن فرط الهوموسيستين في الدم هو علامة غير محددة للنقص. يستخدم حمض الميثيل مالونيك كاختبار خاص لنقص فيتامين بي12.
الجهاز العصبي
تكون الأنسجة العصبية في حالة اسنفجية الشكل مع وذمة للألياف ونقص في الأنسجة. يتحلل المايلين، إلى جانب الألياف المحورية. في المراحل اللاحقة، يحدث التصلب الليفي للأنسجة العصبية. تحدث هذه التغييرات في الأجزاء الظهرية من النخاع الشوكي والمسالك الهرمية في الحبال الجانبية وتسمى التنكس المشترك تحت الحاد للحبل الشوكي.[91]
في الدماغ نفسه، تكون التغييرات أقل حدة: تحدث عندما تتحلل مصادر صغيرة من الألياف العصبية وتراكم الخلايا النجمية، وعادة ما تكون تحت القشرة، وكذلك نزيف دائري مع طارة من الخلايا الدبقية. يمكن أن يتم ملاحظة التغيرات المرضية أيضاً في الجذور الخلفية للحبل، وإلى حد أقل، في الأعصاب الطرفية. يمكن أن تلاحظ الاضطرابات باستخدام التصوير بالرنين المغناطيسي.[92]
التشخيص
يتطلب نقص فيتامين بي12 المزيد من التحقيق عن أسبابه. لا يوجد تشخيص جوهري لتأكيد نقص فيتامين بي12،[93] غالبًا ماتكون مستويات فيتامين بي12 في مصل الدم منخفضة في نقص فيتامين بي12، لكن إذا كان هنالك وجود لعلامات سريرية تتعارض مع المستويات الطبيعية لفيتامين بي12 فإن الاستقصاءات الإضافية مُّبررة؛ وكثيرًا ما يشتبه في التشخيص أولاً، حيث يتطلب التشخيص عدة أختبارات.[17][93][94][95] يتم تشخيص نقص فيتامين بي12 عن طريق مستويات مصل فيتامين بي12 في الدم، مستويات حمض الميثيل مالونيك و/أو الهوموسيستين، وتعداد الدم الكامل.[16][17][93] في بعض الأحيان، يمكن اختبار الدم بحثًا عن الأجسام المضادة ضد العامل الجوهري والخلايا الجدارية في المعدة.[95][96]
قد تظهر اختبارات الدم مستويات منخفضة من فيتامين بي12، مستويات مرتفعة من حمض الميثيل مالونيك و/أو الهوموسيستين، وقد يظهر تعداد الدم الكامل الروتيني فقر الدم مع ارتفاع متوسط الحجم الكروي (MCV).[17][95] وجود اجسام مضادة للعامل الجوهري والخلايا الجدارية يمكن أن يكون مؤشرًا على فقر الدم الخبيث. يمكن أن تميز اختبارات الأجسام المضادة هذه بين فقر الدم الخبيث وسوء امتصاص بي12-الغذائي.[95]
يمكن أن يتطور النقص بدون فقر الدم أو ضمن مستويات فيتامين بي12 الطبيعية، فحص حمض الميثيل مالونيك و/أو الهوموسيستين مطلوب. يشير أرتفاع المستويات إلى حدوث النقص، في العادة تكون المؤشرات موثوقة أكثر.[97][98] في بعض الحالات، قد يتم اللجوء إلى عينة الدم الطرفية؛ مما قد تتيح رؤية الخلايا الكبيرة والكريات البيض متعددة الأشكال النووية المجزأة.[95] يمكن أن تسبق الأعراض العصبية والنفسية علامات الدم وغالبًا ما تكون مظهرا من مظاهر نقص فيتامين بي12.[99]
إذا كان تلف الجهاز العصبي موجودًا ولم يكن اختبار الدم حاسما، فيمكن إجراء ثقب قطني لقياس مستويات السائل النخاعي B-12.[100] في شفط نخاع العظام أو الخزعة، ترى الأرومات الضخمة.[101]
كان اختبار شيلينج طريقة نظائر لاسلكية، عفا عليها الزمن الآن - لاختبار انخفاض مستويات فيتامين بي12.[95][102]
مستوى المصل
| المستوى | الفئة | الملاحظات |
| >400 بيكوغرام/مل | مثالي | قد تشير إلى المستويات المثالية من فيتامين بي12؛ النقص قد يكون غير محتمل |
| 300–200 بيكوغرام/مل | نقص هامشي | قد تكون هنالك حاجة إلى مزيد من الأختبارات؛ في حالة تعارض الأعراض السريرية مع المستويات الطبيعية |
| <200 بيكوغرام/مل | نقص | عادة ماتشير المستويات المنخفضة إلى وجود نقص |
فحص الدم يوضح مستويات فيتامين بي12، عمومًا، من الممكن تحديد نقص فيتامين بي12 عن طريق المصل،[17] في السنوات الأخيرة، يمكن أعتبار مصل فيتامين بي12 نوعًا ما غير موثوقًا،[15] قد يكون النقص موجودًا ضمن مستويات المصل الطبيعية.[15] عندما تتعارض الأعراض السريرية مع المستويات الطبيعية في المصل، قد تكون هناك حاجة لعمل أختبارات أخرى. يتراوح المعدل الطبيعي لمصل الفيتامين بي12 بين (980–200 بيكوغرام/مل). المستويات الأقل من 300 بيكوغرام/مل تشير تقريبًا إلى النقص الهامشي؛ في حين أن المستويات الأقل من 200 بيكوغرام/مل تشير إلى النقص.[93]
طرح بعض الباحثين بأن المعايير القياسية الحالية لمستويات فيتامين بي12 منخفضة جدًا.[103] أظهرت دراسة يابانية بأن الحدود الطبيعية تكون بين (500-1300 بيكوغرام/مليلتر).[104]
العلاج
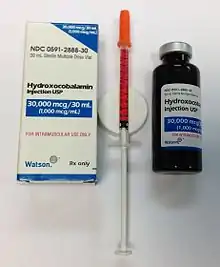
يتم العلاج بإعطاء مكملات فيتامين بي12، إما عن طريق الفم أو الحقن ويبدو أنه فعال بنفس القدر في أولئك الذين لديهم مستويات منخفضة بسبب نقص امتصاص فيتامين بي12. عندما يتم إعطاء جرعات كبيرة عن طريق الفم - فإن امتصاصها لا يعتمد على وجود عامل جوهري أو لفائفي سليم. بدلاً من ذلك، تؤدي هذه المكملات ذات الجرعات الكبيرة إلى امتصاص بنسبة 1٪ إلى 5٪ على طول الأمعاء بأكملها عن طريق الانتشار السلبي. بشكل عام، مطلوب 1 إلى 2 ملغ يوميًا كجرعة كبيرة. حتى فقر الدم الخبيث يمكن علاجه بالكامل عن طريق الفم.[105]
يجب أن يأخذ العلاج في الاعتبار سبب وشدة الحالة.[6] قد تختلف مدة ومسار العلاج.[6] إذا كان السبب الدفين قابلاً للعكس، مثل سوء التغذية، الحمية النباتية، والاستخدام طويل المدى للأدوية مثل مثبطات مضخة البروتون، حاصرات مستقبلات H2، والميتفورمين، كذلك بعض أضطرابات القناة الهضمية، فقد يكون من الضروري علاج أو تغيير السبب الدفين.[2] إذا لم يتم ايجاد السبب الكمين أو وجد انه لا يمكن القضاء عليه على سبيل المثال اولئك الذين يعانون من فقر الدم الخبيث، قد تكون هنالك حاجة إلى العلاج مدى الحياة.[5]
إذا كان النقص حادًا أو مُصاحبًا لاعراض عصبية، يجب مراعاة استخدام الحقن.[13] تعتبر الحقن ذات مفعول سريع للقضاء على الاعراض.[13] في معظم الحالات، يحدث التحسن من أسبوع إلى أسبوعين، طالما يتم تحقيق أشباع الجسم من فيتامين بي12. قد يحتاج النشاط إلى أن يكون محدودًا أثناء العلاج. في الحالات الأقل حدة، يوصى عادة بالجرعات العالية من المكملات الفموية حتى يُلاحظ المزيد من التحسن. لا توفر الحمية النباتية الصرفة ما يكفي من فيتامين بي12، لذلك عادةً ما يوصى بالمكملات الغذائية.[2] الاضطرابات الأخرى قد تحتاج إلى علاج بناءًا على السبب الرئيسي.[2] يتوفر بخاخ للأنف، حبوب تحت اللسان، هلام بالنسبة لأولئك الذين يجدون صعوبة في البلع.[2]
في حالة ترافق نقص فيتامين بي12 مع نقص الفولات، يجب استبدال فيتامين بي12 أولًا لمنع التنكس المشترك تحت الحاد للحبل الشوكي. إذا تركت دون علاج، يمكن أن تسبب آثارًا جانبية خطيرة دائمة تؤثر على الجهاز العصبي والدماغ.[7]
الوبائيات
يعد نقص فيتامين بي12 شائعًا ويحدث في جميع أنحاء العالم. في الولايات المتحدة والمملكة المتحدة، يعاني حوالي 6% من عامة السكان من النقص. في أولئك الذين تزيد أعمارهم عن الستين، حوالي 20% يعانون من نقص. بل إن المعدلات أعلى في البلدان النامية: 40% في أمريكا اللاتينية يعانون من النقص؛ في بعض أجزاء أفريقيا، 70 في المائة؛ وفي بعض أجزاء الهند، 70 إلى 80 بالمائة.
وفقًا لمنظمة الصحة العالمية (WHO)، يمكن اعتبار نقص فيتامين بي12 مشكلة صحية عامة عالمية تؤثر على ملايين الأفراد.[106] ومع ذلك - فإن حدوث وانتشار نقص فيتامين بي12 في جميع أنحاء العالم غير معروف بسبب محدودية البيانات السكانية المتاحة (راجع الجدول أدناه).
تشير دراسة في عام 2000 بأن نقص فيتامين بي12 أكثر انتشارًا على بعد واسع مما كان يعتقد سابقًا. أوجدت الدراسة بأن 39% من المجموعة التي تم دراستها المكونة من 3000 كانت لديهم قيم منخفضة.[87] استخدمت دراسة جامعة تافتس تركيز فيتامين بي12 258 بيكومول/لتر (350 بيكوغرام/مليلتر) كمعيار "للمستوى المنخفض". ومع ذلك، فإن الدراسات الحديثة[107] أوجدت بإن نقص فيتامين بي12 يمكن أن يحدث مع تراكيز لفيتامين بي12 أعلى (500-600 بيكوغرام/مليلتر). على نقيض هذه الخلفية، هنالك أسباب لاعتقاد بأن نقص فيتامين بي12 موجودة في نسب أكثر بكثير من السكان عوضاً عن 39% كما ذكرتها جامعة تافتس.
إن نقص فيتامين بي12 منتشر على نطاق واسع في العالم النامي،[108] مع مستويات ملحوظة للنقص في أفريقيا،[108] كينيا، الهند،[108] المكسيك،[108] فنزويلا، أيضًا وفي جنوب ووسط أمريكا.[108] ويفسر ذلك بسبب قلة تناول المنتجات اللحومية، خاصة بين الفقراء.[109]
يكون نقص فيتامين بي12 أكثر شيوعاً عند كبار السن.[109] ويعود السبب لانخفاض امتصاص بي12 بشكل كبير في وجود التهاب المعدة الضموري، الذي يكون شائعًا عند كبار السن.
جدول يوضح انتشار نقص فيتامين بي12 في جميع أنحاء العالم (المصل/البلازما B12 أقل من 200 pg/mL)
| الفئة | عدد الدراسات | عدد المشاركون | نقص فيتامين بي12 (%) |
| الأطفال (أقل من سنة إلى 18 سنة) | 14 | 22,331 | 12.5 |
| النساء الحوامل | 11 | 11,381 | 27.5 |
| النساء غير الحوامل | 16 | 18,520 | 16 |
| جميع البالغين (أقل من 60 عامًا) | 18 | 81.438 | 6 |
| كبار السن (60+ عامًا) | 25 | 30,449 | 19 |
مستمدة من الجدول 2 المتاح على[110]
التاريخ
في البداية، تم وصف الأعراض من قبل الدكتور جيمس سكارث كومب لأول مرة في معاملات الجمعية الطبية العلاجية في إدنبرة في عام 1824.[111] بين عامي 1849 و1887، وصف توماس أديسون حالة من فقر الدم الخبيث، والتي سُميت لاحقًا ”أنيميا أديسون“،[112] ووصف ويليام أوسلر وويليام جاردنر حالة اعتلال الأعصاب لأول مرة، ووصف هايم خلايا حمراء كبيرة في الدم في هذه الحالة، والتي أطلق عليها اسم "كريات الدم العملاقة" (تسمى الآن الخلايا الكبيرة)، حدد باول إرليش الأرومات الضخمة في نخاع العظم، ووصف لودفيغ ليشثيم حالة من اعتلال النخاع.[113]
كان فقر الدم الخبيث مرضًا قاتلًا قبل حوالي عام 1920 — حتى تم التعرف على أهمية الكبد في تكون الدم، كان علاج فقر الدم الخبيث غير ناجح وتعسفي. قد يكون هذا قد حفز جورج ويبل، المهتم بأمراض الكبد، للتحقيق في دور الكبد في تكون الدم، حيث درس ويبل وهوبر وروبشيت عددًا متنوعًا من العلاجات للأثار على الهيموغلوبين وتجديد الدم — من بينها الكبد النيء فقط أظهر وعدًا حقيقيًا.[114] يُقال إن الصدفة لعبت دورًا في هذا الاكتشاف، حيث لاحظ جورج ويبل أن تجدد الدم كان سيئًا في الكلاب التي تتغذى بالكبد المطبوخ بعد فقدان الدم المزمن. لو لم يكن فني المختبر الكسول قد أعطى الكلاب كبدًا نيئًا، فربما لم يتم اكتشاف الاستجابة الأكثر دراماتيكية في تلك المرحلة من التاريخ.[114] تقريبًا في 1926، سعى جورج مينوت وويليام بي مورفي، اللذان علما باكتشاف ويبل، تجربة الكبد النيء كعلاج لفقر الدم الخبيث، حيث تم افتراض أن تناول الكبد قد يعالج فقر الدم الخبيث.[112][115] أعد إدوين كون مستخلصًا للكبد كان أقوى بنسبة 50 إلى 100 مرة في علاج فقر الدم الخبيث من منتجات الكبد الطبيعية.[112] أوضح ويليام كاسل أن عصارة المعدة تحتوي على "عامل جوهري" والذي عندما يقترن بتناول اللحوم يؤدي إلى امتصاص الفيتامين في هذه الحالة.[113] في عام 1934، شارك جورج ويبل في جائزة نوبل في علم وظائف الأعضاء والطب مع ويليام بي مورفي وجورج مينوت لاكتشاف علاج لمرض قاتل سابقًا لسبب غير معروف باستخدام تركيز الكبد،[116] والذي وجد لاحقًا أنه يحتوي على كميات كبيرة من فيتامين بي12.[115]
الحيوانات الأخرى

المجترات، مثل الماشية والأغنام، تمتص فيتامين بي12 الذي يتم تصنيعه بواسطة بكتيريا الأمعاء الخاصة بها.[117] يجب استهلاك كميات كافية من الكوبالت والنحاس لحدوث توليف فيتامين بي12. في أوائل القرن العشرين، أثناء تطوير زراعة الهضبة البركانية للجزيرة الشمالية في نيوزيلندا، كان للماشية ما يسمى "مرض الأدغال".[118] تم اكتشاف في عام 1934 أن التربة البركانية تفتقر إلى أملاح الكوبالت الضرورية لتوليف فيتامين بي12 بواسطة بكتيريا الأمعاء.[118] وجد أن "مرض الساحل" للأغنام في الكثبان الرملية الساحلية في جنوب أستراليا في ثلاثينيات القرن العشرين ينشأ في نقص التغذية في العناصر النزرة، الكوبالت، والنحاس.[118] يؤثّر نقص الكوبالت على صحّة المواشي، إذ يؤدّي إلى اضطراب في النموّ والرضاعة وحدوث حالة من فقر الدم وفقدان الشهية.[118] تم التغلب على نقص الكوبالت من خلال تطوير "رصاص الكوبالت"، والكريات الكثيفة من أكسيد الكوبالت الممزوجة بالطين المعطاة عن طريق الفم، والتي تم الاحتفاظ بها بعد ذلك في الكرش الحيواني.[118]
المجتمع والثقافة
في عام 2020، تصدرت حالة نقص فيتامين بي12 عناوين الصحف عندما ظهر أن مراهقًا من بريستول، إنجلترا، أصبح أعمى (بسبب ضمور في الأعصاب البصرية) عانى من فقر الدم الخبيث الشديد بعد تناول نظام غذائي مقيد للغاية يتكون من الخبز الأبيض، الرقائق والبطاطس المقلية. مع عدم وجود اللحوم تقريبًا.[119][120] أفاد المريض أنهم أكلوا هذه الأنواع من الطعام لأنهم يكرهون قوام الطعام الآخر، وبالتالي أكلوا نظامهم الغذائي المحدود بقلق شديد.في هذه الحالة، كان نقص كوبالامين الدم مصحوبًا بعواقب أخرى لسوء التغذية - بما في ذلك نقص الزنك والسيلينيوم، نقص فيتامين د، إنعدام النحاس، وانخفاض كثافة العظام.[121]
الهوامش
المراجع
- Hunt, Alesia؛ Harrington, Dominic؛ Robinson, Susan (04 سبتمبر 2014)، "Vitamin B12 deficiency"، BMJ (باللغة الإنجليزية)، 349: g5226، doi:10.1136/bmj.g5226، ISSN 1756-1833، PMID 25189324، مؤرشف من الأصل في 26 يونيو 2022.
- "Office of Dietary Supplements - Vitamin B12"، ods.od.nih.gov (باللغة الإنجليزية)، مؤرشف من الأصل في 11 يوليو 2022، اطلع عليه بتاريخ 12 يوليو 2022.
- Vidal-Alaball, Josep؛ Butler, Christopher؛ Cannings-John, Rebecca؛ Goringe, Andrew؛ Hood, Kerry؛ McCaddon, Andrew؛ McDowell, Ian؛ Papaioannou, Alexandra (20 يوليو 2005)، "Oral vitamin B12 versus intramuscular vitamin B12 for vitamin B12 deficiency"، The Cochrane database of systematic reviews (3): CD004655، doi:10.1002/14651858.CD004655.pub2، ISSN 1469-493X، PMID 16034940، مؤرشف من الأصل في 12 نوفمبر 2020.
- Langan, Robert C.؛ Goodbred (15 سبتمبر 2017)، "Vitamin B12 Deficiency: Recognition and Management"، American Family Physician، 96 (6): 384–389، ISSN 1532-0650، PMID 28925645، مؤرشف من الأصل في 7 أبريل 2022.
- Vitamins in the prevention of human diseases، Berlin: Walter de Gruyter، 2011، ص. 245، ISBN 978-3110214482، مؤرشف من الأصل في 5 أغسطس 2021.
- "Pernicious Anemia Clinical Presentation: History, Physical Examination"، emedicine.medscape.com (باللغة الإنجليزية)، مؤرشف من الأصل في 14 سبتمبر 2017، اطلع عليه بتاريخ 12 مايو 2018.
- "Complications"، nhs.uk، 20 أكتوبر 2017، مؤرشف من الأصل في 12 نوفمبر 2020.
- Lachner؛ Steinle؛ Regenold (2012)، "The neuropsychiatry of vitamin B12 deficiency in elderly patients."، The Journal of neuropsychiatry and clinical neurosciences، 24 (1): 5–15، doi:10.1176/appi.neuropsych.11020052، PMID 22450609.
- Azzini, Elena؛ Raguzzini؛ Polito (07 سبتمبر 2021)، "A Brief Review on Vitamin B12 Deficiency Looking at Some Case Study Reports in Adults"، International Journal of Molecular Sciences، 22 (18): 9694، doi:10.3390/ijms22189694، ISSN 1422-0067، PMID 34575856، مؤرشف من الأصل في 2 مارس 2022.
- "Proton Pump Inhibitors, H2-Receptor Antagonists, Metformin, and Vitamin B-12 Deficiency: Clinical Implications"، Advances in Nutrition، 9 (4): 511S–518S، يوليو 2018، doi:10.1093/advances/nmy023، PMC 6054240، PMID 30032223.
- "How prevalent is vitamin B(12) deficiency among vegetarians?"، Nutrition Reviews، 71 (2): 110–7، فبراير 2013، doi:10.1111/nure.12001، PMID 23356638.
- Wainwright, P.؛ Narayanan؛ Cook (2015-12)، "False-normal vitamin B12 results in a patient with pernicious anaemia"، Clinical Biochemistry، 48 (18): 1366–1367، doi:10.1016/j.clinbiochem.2015.08.009، ISSN 1873-2933، PMID 26277634، مؤرشف من الأصل في 12 مايو 2022.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Wardlaw (2008)، Clinical neurology، London: Manson، ص. 466، ISBN 9781840765182، مؤرشف من الأصل في 3 يناير 2020.
- Schwartz (2012)، The 5-minute pediatric consult (ط. 6th)، Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins، ص. 535، ISBN 9781451116564، مؤرشف من الأصل في 2 يناير 2020.
- Scarpa, Elisabetta؛ Candiotto؛ Sartori؛ Radossi؛ Maschio؛ Tagariello (2013-10)، "Undetected vitamin B12 deficiency due to false normal assay results"، Blood Transfusion، 11 (4): 627–629، doi:10.2450/2012.0183-12، ISSN 1723-2007، PMID 23356970، مؤرشف من الأصل في 23 فبراير 2021.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - "What causes vitamin B12 deficiency anemia?"، uofmhealth.org، Healthwise Staff، 08 أكتوبر 2021، مؤرشف من الأصل في 24 نوفمبر 2020.
- "فيتامين B12 - اضطرابات التغذية"، دليل MSD الإرشادي إصدار المُستخدِم، مؤرشف من الأصل في 27 أغسطس 2021، اطلع عليه بتاريخ 27 أغسطس 2021.
- E. H. (01 يناير 2014)، José؛ Ferro, José M. (المحررون)، Chapter 61 - The neurology of folic acid deficiency، Neurologic Aspects of Systemic Disease Part II (باللغة الإنجليزية)، Elsevier، ج. 120، ص. 927–943، مؤرشف من الأصل في 11 مارس 2021.
- "Vitamin B12 Deficiency: Causes, Symptoms, and Treatment"، WebMD (باللغة الإنجليزية)، مؤرشف من الأصل في 28 يوليو 2021، اطلع عليه بتاريخ 17 أغسطس 2021.
- "Vitamin deficiency anemia - Symptoms and causes"، Mayo Clinic (باللغة الإنجليزية)، مؤرشف من الأصل في 14 أغسطس 2021، اطلع عليه بتاريخ 17 أغسطس 2021.
- "Vitamin B12 lack symptoms"، Cedars-Sinai (باللغة الإنجليزية)، مؤرشف من الأصل في 12 سبتمبر 2021، اطلع عليه بتاريخ 12 سبتمبر 2021.
- "How a Vitamin B Deficiency Affects Blood Pressure"، LIVESTRONG.COM (باللغة الإنجليزية)، مؤرشف من الأصل في 6 سبتمبر 2021، اطلع عليه بتاريخ 26 أكتوبر 2021.
- Li, Kenneth؛ McKay (23 مارس 2000)، "Ischemic Retinopathy Caused by Severe Megaloblastic Anemia"، New England Journal of Medicine، 342 (12): 860–860، doi:10.1056/NEJM200003233421205، ISSN 0028-4793، PMID 10727590، مؤرشف من الأصل في 12 يونيو 2018.
- Ata, Fateen؛ Bint I Bilal؛ Javed؛ Shabir Chaudhry؛ Sharma؛ Fatima Malik؛ Choudry؛ Bhaskaran Kartha (05 نوفمبر 2020)، "Optic neuropathy as a presenting feature of vitamin B-12 deficiency: A systematic review of literature and a case report"، Annals of Medicine and Surgery، 60: 316–322، doi:10.1016/j.amsu.2020.11.010، ISSN 2049-0801، PMID 33204422، مؤرشف من الأصل في 6 يوليو 2021.
- "Harmful and Sneaky - Vitamin B12 deficiency | Unjury Protein"، unjury.com، مؤرشف من الأصل في 14 سبتمبر 2021، اطلع عليه بتاريخ 14 سبتمبر 2021.
- Tsoriev, Andrei، "Subacute combined degeneration of the cord (funicular myelosis) | Radiology Case | Radiopaedia.org"، Radiopaedia (باللغة الإنجليزية)، مؤرشف من الأصل في 5 فبراير 2022، اطلع عليه بتاريخ 06 فبراير 2022.
- Hasbaoui, Brahim El؛ Mebrouk؛ Saghir؛ Yajouri؛ Abilkassem؛ Agadr (04 مارس 2021)، "Vitamin B12 deficiency: case report and review of literature"، The Pan African Medical Journal، 38: 237، doi:10.11604/pamj.2021.38.237.20967، ISSN 1937-8688، PMID 34046142، مؤرشف من الأصل في 16 فبراير 2022.
- Moore, Eileen؛ Mander؛ Ames؛ Carne؛ Sanders؛ Watters (2012-04)، "Cognitive impairment and vitamin B12: a review"، International Psychogeriatrics (باللغة الإنجليزية)، 24 (4): 541–556، doi:10.1017/S1041610211002511، ISSN 1741-203X، مؤرشف من الأصل في 9 سبتمبر 2021.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - "Can Vitamin B12 Cure Tinnitus?"، Tinnitus and You (باللغة الإنجليزية)، 13 يونيو 2021، مؤرشف من الأصل في 20 أغسطس 2021، اطلع عليه بتاريخ 09 سبتمبر 2021.
- "Optic neuropathy as a presenting feature of vitamin B-12 deficiency: A systematic review of literature and a case report"، Annals of Medicine and Surgery (باللغة الإنجليزية)، 60: 316–322، 01 ديسمبر 2020، doi:10.1016/j.amsu.2020.11.010، ISSN 2049-0801، مؤرشف من الأصل في 04 سبتمبر 2021.
- Briani, Chiara؛ Dalla Torre؛ Citton؛ Manara؛ Pompanin؛ Binotto؛ Adami (15 نوفمبر 2013)، "Cobalamin Deficiency: Clinical Picture and Radiological Findings"، Nutrients، 5 (11): 4521–4539، doi:10.3390/nu5114521، ISSN 2072-6643، PMID 24248213، مؤرشف من الأصل في 16 نوفمبر 2021.
- DN Amarapurka MD, ND Patel MD (سبتمبر 2004)، "Gastric Antral Vascular Ectasia Syndrome"، Journal of The Association of Physcians of India، 52: 757.
- "[Encephalomyelopathy due to vitamin B12 deficiency with seizures as a predominant symptom]"، Rinshō Shinkeigaku = Clinical Neurology، 49 (4): 179–85، أبريل 2009، doi:10.5692/clinicalneurol.49.179، PMID 19462816، مؤرشف من الأصل في 11 مايو 2020.
- "Recurrent seizures: an unusual manifestation of vitamin B12 deficiency"، Neurology India، Neurologyindia.com، 52 (1): 122–123، مارس 2004، PMID 15069260، مؤرشف من الأصل في 31 يوليو 2018.
- Mustafa TAŞKESEN, Ahmet YARAMIŞ, Selahattin KATAR, Ayfer GÖZÜ PİRİNÇÇİOĞLU, Murat SÖKER، "Neurological presentations of nutritional vitamin B12 deficiency in 42 breastfed infants in Southeast Turkey" (PDF)، Turk J Med Sci، 41 (6): 1091–1096، مؤرشف من الأصل (PDF) في 20 أكتوبر 2016، اطلع عليه بتاريخ 29 ديسمبر 2013.
{{استشهاد بدورية محكمة}}: صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - "'Vitamin B12 deficiency and seizures'"، Developmental Medicine and Child Neurology (Open access)، 50 (9): 720، سبتمبر 2008، doi:10.1111/j.1469-8749.2008.03083.x، PMID 18754925، مؤرشف من الأصل في 9 سبتمبر 2017.
- Wong, C. W. (2015-04)، "Vitamin B12 deficiency in the elderly: is it worth screening?"، Hong Kong Medical Journal = Xianggang Yi Xue Za Zhi، 21 (2): 155–164، doi:10.12809/hkmj144383، ISSN 1024-2708، PMID 25756278، مؤرشف من الأصل في 22 أكتوبر 2021.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - "Effects of vitamin B12 and folate deficiency on brain development in children"، Food and Nutrition Bulletin، 29 (2 Suppl): S126–31، يونيو 2008، PMC 3137939، PMID 18709887.
- Visser, Petra، "Vitamin B12 Deficiency in Children | Stichting B12 Tekort"، https://stichtingb12tekort.nl/ (باللغة الهولندية)، مؤرشف من الأصل في 18 يناير 2021، اطلع عليه بتاريخ 27 أكتوبر 2021.
{{استشهاد ويب}}: روابط خارجية في|موقع= - "Validate User"، academic.oup.com، مؤرشف من الأصل في 26 مايو 2022، اطلع عليه بتاريخ 26 مايو 2022.
- Krikke, Gg؛ Grooten؛ Vrijkotte؛ van Eijsden؛ Roseboom؛ Painter (2016-02)، "Vitamin B 12 and folate status in early pregnancy and cardiometabolic risk factors in the offspring at age 5-6 years: findings from the ABCD multi-ethnic birth cohort"، BJOG: An International Journal of Obstetrics & Gynaecology (باللغة الإنجليزية)، 123 (3): 384–392، doi:10.1111/1471-0528.13574، مؤرشف من الأصل في 27 مايو 2022.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - "Validate User"، academic.oup.com، مؤرشف من الأصل في 26 مايو 2022، اطلع عليه بتاريخ 26 مايو 2022.
- Yajnik, Chittaranjan Sakerlal؛ Deshmukh (01 يونيو 2012)، "Fetal programming: Maternal nutrition and role of one-carbon metabolism"، Reviews in Endocrine and Metabolic Disorders (باللغة الإنجليزية)، 13 (2): 121–127، doi:10.1007/s11154-012-9214-8، ISSN 1573-2606، مؤرشف من الأصل في 12 مارس 2022.
- Ray, Joel G.؛ Wyatt؛ Thompson؛ Vermeulen؛ Meier؛ Wong؛ Farrell؛ Cole (2007-05)، "Vitamin B12 and the Risk of Neural Tube Defects in a Folic-Acid-Fortified Population"، Epidemiology (باللغة الإنجليزية)، 18 (3): 362–366، doi:10.1097/01.ede.0000257063.77411.e9، ISSN 1044-3983، مؤرشف من الأصل في 26 مايو 2022.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - "Validate User"، academic.oup.com، مؤرشف من الأصل في 26 مايو 2022، اطلع عليه بتاريخ 26 مايو 2022.
- Lövblad, Karl-Olof؛ Ramelli؛ Remonda؛ Nirkko؛ Ozdoba؛ Schroth (01 فبراير 1997)، "Retardation of myelination due to dietary vitamin B12 deficiency: cranial MRI findings"، Pediatric Radiology (باللغة الإنجليزية)، 27 (2): 155–158، doi:10.1007/s002470050090، ISSN 1432-1998، مؤرشف من الأصل في 5 يونيو 2022.
- "Understanding Megaloblastic Anemia"، Healthline (باللغة الإنجليزية)، 12 يناير 2021، مؤرشف من الأصل في 20 أبريل 2021، اطلع عليه بتاريخ 15 أكتوبر 2021.
- Edelstein, T.؛ Stevens؛ Baumslag؛ Metz (1968-02)، "FOLIC ACID AND VITAMIN B12 SUPPLEMENTATION DURING PREGNANCY IN A POPULATION SUBSISTING ON A SUBOPTIMAL DIET*"، BJOG: An International Journal of Obstetrics and Gynaecology (باللغة الإنجليزية)، 75 (2): 133–137، doi:10.1111/j.1471-0528.1968.tb02022.x، ISSN 1470-0328، مؤرشف من الأصل في 22 أبريل 2022.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Shahab-Ferdows, S., Randomized Placebo-controlled Vitamin B12 Supplementation Trial in Deficient Rural Mexican Women: Baseline Assessment, Transcobalamin Genotype and Response of Biochemical and Functional Markers to Supplementation. 2007: University of California, Davis.
- Reid, E.D., et al., Hematological and biochemical responses of rural Mexican preschoolers to iron alone or iron plus micronutrients. Vol. 15. 2001. A731-A731.
- Hunt, Alesia؛ Harrington؛ Robinson (04 سبتمبر 2014)، "Vitamin B12 deficiency"، BMJ (باللغة الإنجليزية)، 349: g5226، doi:10.1136/bmj.g5226، ISSN 1756-1833، PMID 25189324، مؤرشف من الأصل في 4 أكتوبر 2021.
- Quadros, Edward V. (2010-1)، "Advances in the Understanding of Cobalamin Assimilation and Metabolism"، British journal of haematology، 148 (2): 195–204، doi:10.1111/j.1365-2141.2009.07937.x، ISSN 0007-1048، PMID 19832808، مؤرشف من الأصل في 10 مارس 2021.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Gröber, Uwe؛ Kisters؛ Schmidt (12 ديسمبر 2013)، "Neuroenhancement with Vitamin B12—Underestimated Neurological Significance"، Nutrients، 5 (12): 5031–5045، doi:10.3390/nu5125031، ISSN 2072-6643، PMID 24352086، مؤرشف من الأصل في 8 نوفمبر 2020.
- Ralapanawa, Dissanayake Mudiyanselage Priyantha Udaya Kumara؛ Jayawickreme؛ Ekanayake؛ Jayalath (18 سبتمبر 2015)، "B12 deficiency with neurological manifestations in the absence of anaemia"، BMC Research Notes، 8: 458، doi:10.1186/s13104-015-1437-9، ISSN 1756-0500، PMID 26385097، مؤرشف من الأصل في 13 أبريل 2021.
- Reversible dementia in young persons due to cobalamin deficiency. Kumar S, Narasimha A, Holla B, Viswanath B, Narayanaswamy JC, Math SB, Chandrashekar CR. The Journal of Neuropsychiatry and Clinical Neurosciences 2013;25:E62-E63. doi:10.1176/appi.neuropsych.12040083 http://journals.psychiatryonline.org/article.aspx?articleid=1660553 نسخة محفوظة 2014-04-13 على موقع واي باك مشين.
- Sethi NK, Robilotti E, Sadan Y (2005)، "Neurological Manifestations Of Vitamin B-12 Deficiency"، The Internet Journal of Nutrition and Wellness، 2 (1)، مؤرشف من الأصل في 14 مايو 2019.
{{استشهاد بدورية محكمة}}: صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - "Cobalamin-responsive psychosis as the sole manifestation of vitamin B12 deficiency"، The Israel Medical Association Journal، 3 (9): 701–703، سبتمبر 2001، PMID 11574992، مؤرشف من الأصل في 28 مارس 2016.
- "Pernicious anemia: MedlinePlus Medical Encyclopedia"، Nlm.nih.gov، مؤرشف من الأصل في 5 يوليو 2016، اطلع عليه بتاريخ 29 ديسمبر 2013.
- "Effect of vitamin B12 deficiency on neurodevelopment in infants: current knowledge and possible mechanisms"، Nutrition Reviews، 66 (5): 250–5، مايو 2008، doi:10.1111/j.1753-4887.2008.00031.x، PMID 18454811، مؤرشف من الأصل في 18 نوفمبر 2008.
- PhD, Viatcheslav Wlassoff,، "Vitamin B12 Deficiency and its Neurological Consequences"، www.brainblogger.com، مؤرشف من الأصل في 18 يونيو 2021، اطلع عليه بتاريخ 15 أكتوبر 2021.
{{استشهاد ويب}}: صيانة CS1: extra punctuation (link) - Dhonukshe-Rutten, Rosalie AM؛ Pluijm؛ Groot؛ Lips؛ Smit؛ Staveren (2005)، "Homocysteine and Vitamin B12 Status Relate to Bone Turnover Markers, Broadband Ultrasound Attenuation, and Fractures in Healthy Elderly People"، Journal of Bone and Mineral Research (باللغة الإنجليزية)، 20 (6): 921–929، doi:10.1359/JBMR.050202، ISSN 1523-4681، مؤرشف من الأصل في 25 مايو 2021.
- Tucker, Katherine L.؛ Hannan؛ Qiao؛ Jacques؛ Selhub؛ Cupples؛ Kiel (2005)، "Low Plasma Vitamin B12 Is Associated With Lower BMD: The Framingham Osteoporosis Study"، Journal of Bone and Mineral Research (باللغة الإنجليزية)، 20 (1): 152–158، doi:10.1359/JBMR.041018، ISSN 1523-4681، مؤرشف من الأصل في 11 يناير 2022.
- Herrmann, Markus؛ Schmidt؛ Umanskaya؛ Wagner؛ Taban-Shomal؛ Widmann؛ Colaianni؛ Wildemann؛ Herrmann (01 ديسمبر 2007)، "The role of hyperhomocysteinemia as well as folate, vitamin B6 and B12 deficiencies in osteoporosis – a systematic review" (باللغة الإنجليزية)، 45 (12): 1621–1632، doi:10.1515/CCLM.2007.362، ISSN 1437-4331، مؤرشف من الأصل في 9 مايو 2021.
{{استشهاد بدورية محكمة}}: Cite journal requires|journal=(مساعدة) - Carmel, Ralph؛ Lau؛ Baylink؛ Saxena؛ Singer (14 يوليو 1988)، "Cobalamin and Osteoblast-Specific Proteins"، New England Journal of Medicine، 319 (2): 70–75، doi:10.1056/NEJM198807143190202، ISSN 0028-4793، PMID 3260008، مؤرشف من الأصل في 13 مايو 2021.
- Kim, G. S.؛ Kim؛ Park؛ Lee؛ Park (01 ديسمبر 1996)، "Effects of vitamin B12 on cell proliferation and cellular alkaline phosphatase activity in human bone marrow stromal osteoprogenitor cells and UMR106 osteoblastic cells"، Metabolism - Clinical and Experimental (باللغة الإنجليزية)، 45 (12): 1443–1446، doi:10.1016/S0026-0495(96)90171-7، ISSN 0026-0495، PMID 8969275، مؤرشف من الأصل في 11 يناير 2022.
- van Meurs, Joyce B.J.؛ Dhonukshe-Rutten؛ Pluijm؛ van der Klift؛ de Jonge؛ Lindemans؛ de Groot؛ Hofman؛ Witteman (13 مايو 2004)، "Homocysteine Levels and the Risk of Osteoporotic Fracture"، New England Journal of Medicine، 350 (20): 2033–2041، doi:10.1056/NEJMoa032546، ISSN 0028-4793، PMID 15141041، مؤرشف من الأصل في 29 يوليو 2020.
- Herrmann, Markus؛ Umanskaya؛ Traber؛ Schmidt-Gayk؛ Menke؛ Lanzer؛ Lenhart؛ Schmidt؛ Herrmann (01 ديسمبر 2007)، "The effect of B-vitamins on biochemical bone turnover markers and bone mineral density in osteoporotic patients: a 1-year double blind placebo controlled trial" (باللغة الإنجليزية)، 45 (12): 1785–1792، doi:10.1515/CCLM.2007.352، ISSN 1437-4331، مؤرشف من الأصل في 9 مايو 2021.
{{استشهاد بدورية محكمة}}: Cite journal requires|journal=(مساعدة) - Green, Timothy J.؛ McMahon؛ Skeaff؛ Williams؛ Whiting (2007-02)، "Lowering homocysteine with B vitamins has no effect on biomarkers of bone turnover in older persons: a 2-y randomized controlled trial"، The American Journal of Clinical Nutrition، 85 (2): 460–464، doi:10.1093/ajcn/85.2.460، ISSN 0002-9165، PMID 17284744، مؤرشف من الأصل في 11 يناير 2022.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Green, Ralph؛ Allen؛ Bjørke-Monsen؛ Brito؛ Guéant؛ Miller؛ Molloy؛ Nexo؛ Stabler (29 يونيو 2017)، "Vitamin B12 deficiency"، Nature Reviews Disease Primers (باللغة الإنجليزية)، 3 (1): 1–20، doi:10.1038/nrdp.2017.40، ISSN 2056-676X، مؤرشف من الأصل في 4 سبتمبر 2021.
- Rojas Hernandez, Cristhiam M.؛ Oo (2015-03)، "Advances in mechanisms, diagnosis, and treatment of pernicious anemia"، Discovery Medicine، 19 (104): 159–168، ISSN 1944-7930، PMID 25828519، مؤرشف من الأصل في 13 أغسطس 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ=(مساعدة) - Baik, H.w.؛ Russell (01 يوليو 1999)، "Vitamin b12 deficiency in the elderly"، Annual Review of Nutrition، 19 (1): 357–377، doi:10.1146/annurev.nutr.19.1.357، ISSN 0199-9885، مؤرشف من الأصل في 7 سبتمبر 2021.
- Jimenez, Juan A.؛ Rodriguez؛ Gamboa؛ Rodriguez؛ Garcia (07 نوفمبر 2012)، "Diphyllobothrium pacificum Infection is Seldom Associated with Megaloblastic Anemia"، The American Journal of Tropical Medicine and Hygiene، 87 (5): 897–901، doi:10.4269/ajtmh.2012.12-0067، ISSN 0002-9637، PMID 22987655، مؤرشف من الأصل في 08 سبتمبر 2021.
- "Giardia infection causes vitamin B12 deficiency"، Australian and New Zealand Journal of Medicine، 16 (1): 78–9، فبراير 1986، doi:10.1111/j.1445-5994.1986.tb01127.x، PMID 3458451.
- Jimenez, Juan A.؛ Rodriguez؛ Gamboa؛ Rodriguez؛ Garcia (07 نوفمبر 2012)، "Diphyllobothrium pacificum Infection is Seldom Associated with Megaloblastic Anemia"، The American Journal of Tropical Medicine and Hygiene، 87 (5): 897–901، doi:10.4269/ajtmh.2012.12-0067، ISSN 0002-9637، PMID 22987655، مؤرشف من الأصل في 9 يناير 2022.
- "Proton pump inhibitor and histamine 2 receptor antagonist use and vitamin B12 deficiency"، Jama، 310 (22): 2435–2442، ديسمبر 2013، doi:10.1001/jama.2013.280490، PMID 24327038.
- "أسباب نقص فيتامين ب12 ومعلومات مهمة"، Webteb، مؤرشف من الأصل في 24 نوفمبر 2020، اطلع عليه بتاريخ 08 سبتمبر 2021.
- "Effect of chronic ranitidine treatment on secretion of intrinsic factor"، Br Med J (Clin Res Ed)، 285 (6337): 264، 1982، doi:10.1136/bmj.285.6337.264، PMC 1499627، PMID 6124297.
- Nagao, Takayo؛ Hirokawa (13 أبريل 2017)، "Diagnosis and treatment of macrocytic anemias in adults"، Journal of General and Family Medicine، 18 (5): 200–204، doi:10.1002/jgf2.31، ISSN 2189-6577، PMID 29264027، مؤرشف من الأصل في 10 يونيو 2021.
- "Risk factors of vitamin B(12) deficiency in patients receiving metformin"، Archives of Internal Medicine، 166 (18): 1975–9، أكتوبر 2006، doi:10.1001/archinte.166.18.1975، PMID 17030830.
- Caruso, Roberta؛ Pallone؛ Stasi؛ Romeo؛ Monteleone (01 ديسمبر 2013)، "Appropriate nutrient supplementation in celiac disease"، Annals of Medicine، 45 (8): 522–531، doi:10.3109/07853890.2013.849383، ISSN 0785-3890، مؤرشف من الأصل في 28 نوفمبر 2021.
- "Nitrous oxide has multiple deleterious effects on cobalamin metabolism and causes decreases in activities of both mammalian cobalamin-dependent enzymes in rats"، The Journal of Clinical Investigation، The American Society For Clinical Investigation، 67 (5): 1270–1283، مايو 1981، doi:10.1172/JCI110155، PMC 370693، PMID 6112240.
- Anyanwu, Ebere C.؛ Morad؛ Campbell (26 أغسطس 2004)، "Metabolism of Mycotoxins, Intracellular Functions of Vitamin B12, and Neurological Manifestations in Patients with Chronic Toxigenic Mold Exposures. A Review"، The Scientific World Journal، 4: 736–745، doi:10.1100/tsw.2004.133، ISSN 2356-6140، PMID 15349513، مؤرشف من الأصل في 6 أبريل 2019.
- Ulasoglu, Celal؛ Temiz؛ Sağlam (09 ديسمبر 2019)، "The Relation of Cytotoxin-Associated Gene-A Seropositivity with Vitamin B12 Deficiency in Helicobacter pylori-Positive Patients"، BioMed Research International، 2019: 1450536، doi:10.1155/2019/1450536، ISSN 2314-6133، PMID 31886171، مؤرشف من الأصل في 20 فبراير 2022.
- "Purification and characterization of a corrinoid compound from Chlorella tablets as an algal health food"، Journal of Agricultural and Food Chemistry، 50 (17): 4994–7، أغسطس 2002، doi:10.1021/jf020345w، PMID 12166996.
- "Algae acquire vitamin B12 through a symbiotic relationship with bacteria"، Nature، 438 (7064): 90–3، نوفمبر 2005، doi:10.1038/nature04056، PMID 16267554.
- "Microbial production of vitamin B12"، Applied Microbiology and Biotechnology، 58 (3): 275–85، مارس 2002، doi:10.1007/s00253-001-0902-7، PMID 11935176.
- McBride, Judy (02 أغسطس 2000)، "B12 Deficiency May Be More Widespread Than Thought"، Agricultural Research Service، United States Department of Agriculture، مؤرشف من الأصل في 4 أغسطس 2016، اطلع عليه بتاريخ 02 يوليو 2012.
- Voet, Donald؛ Voet, Judith G. (2010)، Biochemistry، New York: J. Wiley & Sons، ص. 957، ISBN 978-0470-57095-1، مؤرشف من الأصل في 27 أغسطس 2021.
- Yamada (2013)، "Chapter 9. Cobalt: Its Role in Health and Disease"، في Astrid Sigel, Helmut Sigel and Roland K. O. Sigel (المحرر)، Interrelations between Essential Metal Ions and Human Diseases، Metal Ions in Life Sciences، Springer، ج. 13، ص. 295–320، doi:10.1007/978-94-007-7500-8_9.
- "Vitamin B12-folate interrelationships"، Annual Review of Nutrition، 5: 115–41، 1985، doi:10.1146/annurev.nu.05.070185.000555، PMID 3927946.
- "Vitamin B12 / Pathophysiology Text"، LifeSave.org، ص. 215، مؤرشف من الأصل في 7 فبراير 2018، اطلع عليه بتاريخ 31 ديسمبر 2013.
- "Severe vitamin B12 deficiency in an exclusively breastfed 5-month-old Italian infant born to a mother receiving multivitamin supplementation during pregnancy"، BMC Pediatrics (Full text)، Biomedcentral.com، 12: 85، 2012، doi:10.1186/1471-2431-12-85، PMID 22726312، مؤرشف من الأصل في 24 سبتمبر 2015.
- "Vitamin B12 Deficiency" (باللغة الإنجليزية)، مؤرشف من الأصل في 18 أكتوبر 2020، اطلع عليه بتاريخ 07 نوفمبر 2021.
- "Vitamin B12 and Folate"، Lab Tests Online (باللغة الإنجليزية)، 24 مارس 2021، مؤرشف من الأصل في 18 سبتمبر 2021، اطلع عليه بتاريخ 15 أكتوبر 2021.
- Snow, Christopher F. (28 يونيو 1999)، "Laboratory Diagnosis of Vitamin B12 and Folate Deficiency: A Guide for the Primary Care Physician"، Archives of Internal Medicine، 159 (12): 1289–1298، doi:10.1001/archinte.159.12.1289، ISSN 0003-9926، مؤرشف من الأصل في 18 يناير 2021.
- "Possible cause of false normal B-12 assays"، Bmj، 333 (7569): 654–5، سبتمبر 2006، doi:10.1136/bmj.333.7569.654-c، PMC 1570871، PMID 16990334.
- "Test used to diagnose B12 deficiency may be inadequate"، news-medical.net، 28 أكتوبر 2004، مؤرشف من الأصل في 15 يناير 2009، اطلع عليه بتاريخ 04 ديسمبر 2007.
- "Metabolic vitamin B12 status on a mostly raw vegan diet with follow-up using tablets, nutritional yeast, or probiotic supplements"، Annals of Nutrition & Metabolism، 44 (5–6): 229–34، 2000، doi:10.1159/000046689، PMID 11146329، مؤرشف من الأصل في 22 نوفمبر 2011.
- Lindenbaum, John؛ Healton؛ Savage؛ Brust؛ Garrett؛ Podell؛ Margell؛ Stabler؛ Allen (30 يونيو 1988)، "Neuropsychiatric Disorders Caused by Cobalamin Deficiency in the Absence of Anemia or Macrocytosis"، New England Journal of Medicine، 318 (26): 1720–1728، doi:10.1056/NEJM198806303182604، ISSN 0028-4793، PMID 3374544، مؤرشف من الأصل في 15 يونيو 2022.
- "Diagnosing vitamin B-12 deficiency on the basis of serum B-12 assay"، Bmj، 333 (7564): 385–6، أغسطس 2006، doi:10.1136/bmj.333.7564.385، PMC 1550477، PMID 16916826.
- "What is the role of bone marrow aspiration in the diagnosis of megaloblastic anemia?"، www.medscape.com، مؤرشف من الأصل في 16 أكتوبر 2021، اطلع عليه بتاريخ 15 أكتوبر 2021.
- Nickoloff, Eileen؛ Demers (01 يناير 1988)، "Schilling Test: Physiologic Basis for and use as a Diagnostic Test"، CRC Critical Reviews in Clinical Laboratory Sciences، 26 (4): 263–276، doi:10.3109/10408368809105892، ISSN 0590-8191، مؤرشف من الأصل في 4 أبريل 2019.
- "Are U.S. lower normal B12 limits too low?"، Journal of the American Geriatrics Society، 44 (10): 1274–5، أكتوبر 1996، doi:10.1111/j.1532-5415.1996.tb01389.x، PMID 8856015.
- "Serum and cerebrospinal fluid vitamin B12 levels in demented patients with CH3-B12 treatment--preliminary study"، The Japanese Journal of Psychiatry and Neurology، 42 (1): 65–71، مارس 1988، doi:10.1111/j.1440-1819.1988.tb01957.x، PMID 3398357.
- "Effective treatment of cobalamin deficiency with oral cobalamin"، Blood، 92 (4): 1191–1198، أغسطس 1998، PMID 9694707، مؤرشف من الأصل في 7 يناير 2009.
- de Benoist, Bruno (01 يونيو 2008)، "Conclusions of a WHO Technical Consultation on Folate and Vitamin B12 Deficiencies"، Food and Nutrition Bulletin (باللغة الإنجليزية)، 29 (2_suppl1): S238–S244، doi:10.1177/15648265080292S129، ISSN 0379-5721، مؤرشف من الأصل في 4 سبتمبر 2021.
- Thomas, Donald (22 يونيو 2011)، New Jump Swing Healthy Aging and Athletic Nutrition Program، Xlibris، ص. 41، ISBN 978-1-4628-8427-8، مؤرشف من الأصل في 7 مايو 2020.
- Stabler, Sally P.؛ Allen (14 يوليو 2004)، "VITAMIN B12 DEFICIENCY AS A WORLDWIDE PROBLEM"، Annual Review of Nutrition (باللغة الإنجليزية)، 24 (1): 299–326، doi:10.1146/annurev.nutr.24.012003.132440، ISSN 0199-9885، مؤرشف من الأصل في 3 أكتوبر 2021.
- "Vitamin B12 deficiency in the elderly"، Annual Review of Nutrition، 19: 357–77، 1999، doi:10.1146/annurev.nutr.19.1.357، PMID 10448529.
- "Chapter Six - Vitamin B12"، Advances in Food and Nutrition Research، Academic Press، ج. 83، 2018، ص. 215–279، doi:10.1016/bs.afnr.2017.11.005، ISBN 9780128118030، PMID 29477223.
- "History of Leith, Edinburgh » James Scarth Combe"، web.archive.org، 20 يونيو 2018، مؤرشف من الأصل في 20 يونيو 2018، اطلع عليه بتاريخ 10 يناير 2022.
{{استشهاد ويب}}: صيانة CS1: BOT: original-url status unknown (link) - "The discovery of Pernicious anaemia"، ari.info (باللغة الإنجليزية)، مؤرشف من الأصل في 7 مارس 2021، اطلع عليه بتاريخ 15 نوفمبر 2021.
- Wintrobe's clinical hematology (ط. Thirteenth edition)، Philadelphia، 2014، ISBN 9781451172683، OCLC 864836128، مؤرشف من الأصل في 10 يناير 2022.
{{استشهاد بكتاب}}:|edition=has extra text (مساعدة) - Sinclair, Leonard (01 مايو 2008)، "Recognizing, treating and understanding pernicious anaemia"، Journal of the Royal Society of Medicine، 101 (5): 262–264، doi:10.1258/jrsm.2008.081006، ISSN 0141-0768، PMID 18463283، مؤرشف من الأصل في 31 ديسمبر 2021.
- "The Nobel Prize in Physiology or Medicine 1934"، NobelPrize.org (باللغة الإنجليزية)، مؤرشف من الأصل في 30 أكتوبر 2021، اطلع عليه بتاريخ 15 نوفمبر 2021.
- Scott, John M.؛ Molloy (2012)، "The Discovery of Vitamin B12"، Annals of Nutrition and Metabolism (باللغة الإنجليزية)، 61 (3): 239–245، doi:10.1159/000343114، ISSN 0250-6807، PMID 23183296، مؤرشف من الأصل في 6 يونيو 2020.
- Gille, Doreen؛ Schmid, Alexandra (01 فبراير 2015)، "Vitamin B12 in meat and dairy products"، Nutrition Reviews، 73 (2): 106–115، doi:10.1093/nutrit/nuu011، ISSN 0029-6643، مؤرشف من الأصل في 20 يونيو 2022.
- Lee Russell (25 سبتمبر 2008)، Vitamins in Animal and Human Nutrition (باللغة الإنجليزية)، John Wiley & Sons، ISBN 978-0-470-37668-3، مؤرشف من الأصل في 17 يوليو 2022.
- "Teenager 'blind' from living off crisps and chips"، BBC News (باللغة الإنجليزية)، 03 سبتمبر 2019، مؤرشف من الأصل في 22 أغسطس 2021، اطلع عليه بتاريخ 09 سبتمبر 2021.
- "A Teen Boy's Diet of Fries and Sausage Led to Blindness, a New Case Study Says"، Time (باللغة الإنجليزية)، مؤرشف من الأصل في 14 أغسطس 2020، اطلع عليه بتاريخ 23 نوفمبر 2021.
- "Teenager goes blind after living on diet of chips and sausages"، ITV News (باللغة الإنجليزية)، 02 سبتمبر 2019، مؤرشف من الأصل في 21 فبراير 2020، اطلع عليه بتاريخ 09 سبتمبر 2021.
- مجلة العلوم والتقنية أمراض الدم.
قراءات إضافية
- Pacholok, Sally M.؛ Stuart (2011)، Could It Be B12?: An Epidemic of Misdiagnoses، Fresno, CA: Linden Publishing، ISBN 978-1-61035-065-5.
- Hooper, M. (2012)، Pernicious Anaemia: The Forgotten Disease - the causes and consequences of Vitamin B12 Deficiency، London: Hammersmith Press، ISBN 978-1-78161-004-6.
وصلات خارجية
- http://www.webmd.com/a-to-z-guides/vitamin-b12-deficiency-anemia-topic-overview WebMD overview
- Vitamin B12 and Folate at Lab Tests Online
- بوابة طب