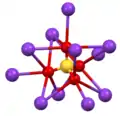
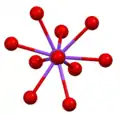
كبريتات البوتاسيوم
كبريتات البوتاسيوم مركب كيميائي صيغته K2SO4، ويوجد على شكل صلب أبيض اللون. عُرف المركب منذ أوائل القرن 14، وعكف على دراسته جلاوبر وبويل.
| كبريتات البوتاسيوم | |
|---|---|
 Arcanite Arcanite | |
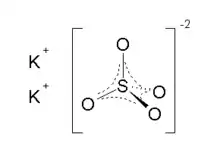 كبريتات البوتاسيوم | |
| أسماء أخرى | |
Potassium sulphate | |
| المعرفات | |
| رقم CAS | 7778-80-5 |
| بوب كيم (PubChem) | 24507 |
مواصفات الإدخال النصي المبسط للجزيئات
| |
| |
| الخواص | |
| الصيغة الجزيئية | K2SO4 |
| الكتلة المولية | 174.259 غ/مول |
| المظهر | صلب أبيض |
| الرائحة | عديم الرائحة |
| الكثافة | 2.66 غ/سم3[1] |
| نقطة الانصهار | 1069 °س، 1342 °ك، 1956 °ف |
| نقطة الغليان | 1689 °س، 1962 °ك، 3072 °ف |
| الذوبانية في الماء | 111 غ/ل (20 °س) 120 غ/ل (25 °س) 240 غ/ل (100 °س) |
| الذوبانية | ينحل جزئياً في الغليسرول غير منحل في الأسيتون والكحول وثنائي كبريتيد الكربون |
| حموضة (pKa) | ~7 |
| معامل الانكسار (nD) | 1.495 |
| البنية | |
| البنية البلورية | نظام بلوري معيني قائم |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
الخواص
يوجد المركب في الشروط القياسية على شكل صلب أبيض اللون، وهو قابل للانحلال في الماء، لكنه لا ينحل في الكحول.
الاستخدامات
يستخدم أساسا كبريتات البوتاسيوم سماداً؛ كما يستخدم الملح الخام في بعض الأحيان في صناعة الزجاج.
معرض صور
مراجع
- Patnaik, Pradyot (2002)، Handbook of Inorganic Chemicals، McGraw-Hill، ISBN 0-07-049439-8.
- H. Schultz, G. Bauer, E. Schachl, F. Hagedorn, P. Schmittinger (2005)، "Potassium Compounds"، Ullmann's Encyclopedia of Industrial Chemistry، Weinheim: Wiley-VCH، doi:10.1002/14356007.a22_039.
- بوابة الكيمياء
- بوابة زراعة
This article is issued from Wikipedia. The text is licensed under Creative Commons - Attribution - Sharealike. Additional terms may apply for the media files.