Enlace de hidrógeno
El enlace de hidrógeno es la fuerza eminentemente electrostática atractiva entre un átomo electronegativo y un átomo de hidrógeno unido covalentemente a otro átomo electronegativo. Resulta de la formación de una fuerza carga-dipolo con un átomo de hidrógeno unido a un átomo de nitrógeno, oxígeno o flúor (de ahí el nombre de "enlace de hidrógeno"), que no debe confundirse con un enlace covalente a átomos de hidrógeno. La energía de un enlace de hidrógeno (típicamente de 5 a 30 kJ/mol) es significativamente menor a la de los enlaces covalentes débiles (155 kJ/mol), y un enlace covalente típico es solo 20 veces más fuerte que un enlace de hidrógeno intermolecular. Estos enlaces pueden ocurrir entre moléculas (intermolecularidad), o entre diferentes partes de una misma molécula (intramolecularidad).[2] El enlace de hidrógeno es una fuerza electrostática dipolo-dipolo fija muy fuerte cuando están muchas moléculas unidas, ya que da gran estabilidad, pero más débil que el enlace covalente o el enlace iónico. La fuerza del enlace de hidrógeno se ubica en algún lugar intermedio entre un enlace covalente y una fuerza de Van der Waals (fuerza de dispersión). Este tipo de enlace ocurre tanto en moléculas inorgánicas tales como el agua, y en moléculas orgánicas como el ADN.

El enlace de hidrógeno intermolecular es responsable del punto de ebullición alto del agua (100 °C). Esto es debido al fuerte enlace de hidrógeno, en contraste a los otros hidruros de calcógenos. El enlace de hidrógeno intramolecular es responsable parcialmente de la estructura secundaria, estructura terciaria y estructura cuaternaria de las proteínas y ácidos nucleicos.
Enlace
Un átomo de hidrógeno unido a un átomo relativamente electronegativo es un átomo donante del enlace de hidrógeno.[3] Este átomo electronegativo puede ser flúor, oxígeno o nitrógeno. Un átomo electronegativo tal como el flúor, oxígeno o nitrógeno es un aceptor de enlace de hidrógeno, sin importar si está enlazado covalentemente o no a un átomo de hidrógeno. Un ejemplo de un donante de enlace de hidrógeno es el etanol, que tiene un átomo de hidrógeno enlazado covalentemente al oxígeno; un ejemplo de aceptor de enlace de hidrógeno que no tiene un átomo de hidrógeno enlazado covalentemente a él es el átomo de oxígeno en el éter dietílico.

El carbono también puede participar en enlaces de hidrógeno, cuando el átomo de carbono está enlazado a algunos átomos electronegativos, como en el caso de cloroformo, CHCl3. El átomo electronegativo atrae la nube electrónica alrededor del núcleo de hidrógeno y, al descentralizar la nube, deja al átomo con una carga positiva parcial. Debido al pequeño tamaño del hidrógeno en comparación a otros átomos y moléculas, la carga resultante, aunque solo parcial, representa una gran densidad de carga. Un enlace de hidrógeno resulta cuando esta densidad de carga positiva fuerte atrae a un par libre de electrones de otro heteroátomo, que se convierte en el aceptor de enlace de hidrógeno.
El enlace de hidrógeno suele ser descrito como una interacción electrostática dipolo-dipolo. Sin embargo, también tiene algunas características del enlace covalente: es direccional, fuerte, produce distancias interatómicas menores que la suma de los radios de van der Waals, y usualmente involucra un número limitado de compañeros de interacción, que puede ser interpretado como un tipo de valencia. Estas características covalentes son más significativas cuando los aceptores se unen a átomos de hidrógeno de donantes más electronegativos.
La naturaleza parcialmente covalente de un enlace de hidrógeno da origen a las preguntas: "¿A qué molécula pertenece el núcleo de hidrógeno?" y "¿Cuál debería ser etiquetado como 'donante' y cuál como 'aceptor'?" Generalmente, es fácil determinar esto basándose simplemente en las distancias interatómicas del sistema X—H...Y: típicamente, la distancia X—H es ~1.1 Å, mientras que la distancia H...Y es ~ 1.6 a 2.0 Å. Los líquidos que muestran enlace de hidrógeno se llaman líquidos asociativos.
Los enlaces de hidrógeno pueden variar en fuerza, desde muy débiles (1-2 kJ mol−1) a extremadamente fuertes (>155 kJ mol−1), como en el ion HF2−.[4] Algunos valores típicos incluyen:
- F—H...F (155 kJ/mol)
- O—H...N (29 kJ/mol)
- O—H...O (21 kJ/mol)
- N—H...N (13 kJ/mol)
- N—H...O (8 kJ/mol)
- +OH3...:OH2 (18 kJ/mol[5]) (Información obtenida usando dinámica molecular como se detalla en la referencia, y debería ser comparada con 7.9 kJ/mol para agua en bruto, obtenida también usando la misma dinámica molecular.)
La longitud de los enlaces de hidrógeno depende de la fuerza del enlace. La fuerza del enlace misma es dependiente de la temperatura, presión, ángulo de enlace y ambiente (generalmente caracterizado por la constante dieléctrica local). La longitud típica de un enlace de hidrógeno en agua es 1.97 Å (197 pm). El ángulo de enlace ideal depende de la naturaleza del donante del enlace de hidrógeno. Los resultados experimentales del donante fluoruro de hidrógeno con diversos aceptores muestran los siguientes ángulos:[6]
| Aceptor···Donante | Simetría TREPEV | Ángulo (°) |
| HCN···HF | lineal | 180 |
| H2CO ··· HF | trigonal plana | 110 |
| H2O ··· HF | piramidal | 46 |
| H2S ··· HF | piramidal | 89 |
| SO2 ··· HF | trigonal plana | 145 |
Historia
En su libro The Nature of the Chemical Bond (en español: La Naturaleza del Enlace Químico), Linus Pauling concede los créditos a T.S. Moore y T.F. Winmill de la primera mención del enlace de hidrógeno, en 1912 (J. Chem. Soc. 101, 1635). Moore y Winmill usaron el enlace de hidrógeno para justificar el hecho que el hidróxido de trimetilamonio es una base más débil que el hidróxido de tetrametilamonio. La descripción del enlace de hidrógeno en su forma más conocida, en el agua, vino algunos años después, en 1920, por Latimer y Rodebush (JACS, 42, 1419).
Enlace de hidrógeno en el agua

El ejemplo de enlace de hidrógeno más ubicuo es el agua. En una molécula aislada de agua se encuentran dos átomos de hidrógeno y un átomo de oxígeno. Dos moléculas de agua pueden formar un enlace de hidrógeno entre ellas; en el caso más simple, cuando solo dos moléculas están presentes, se llama dímero de agua y se usa frecuentemente como un sistema modelo. Cuantas más moléculas estén presentes, como en el caso del agua líquida, más enlaces son posibles, debido a que el oxígeno de una molécula de agua tiene dos pares libres de electrones, cada uno de los cuales puede formar un enlace de hidrógeno con átomos de hidrógeno de otras dos moléculas de agua. Esto puede repetirse, de tal forma que cada molécula de agua está unida mediante enlaces de hidrógeno a hasta cuatro otras moléculas de agua, como se muestra en la figura (dos a través de sus pares libres, y dos a través de sus átomos de hidrógeno).
El elevado punto de ebullición del agua se debe al gran número de enlaces de hidrógeno que cada molécula tiene, en relación con su baja masa molecular, y a la gran fuerza de estos enlaces de hidrógeno. El agua tiene puntos de ebullición, fusión y viscosidad muy altos, comparados con otras sustancias no unidas entre sí por enlaces de hidrógeno. La razón para estos atributos es la dificultad, para romper estos enlaces. El agua es única porque sus átomos de oxígeno tiene dos pares libres y dos átomos de hidrógeno, significando que el número total por enlaces de una molécula de agua es cuatro. Por ejemplo, el fluoruro de hidrógeno -que tiene tres pares libres en el átomo de flúor, pero solo un átomo de hidrógeno- puede tener un total de solo dos; el amoníaco tiene el problema opuesto: tres átomos de hidrógeno, pero solo un par libre.
- H-F...H-F...H-F
El número exacto de enlaces de hidrógeno en los cuales una molécula en el agua líquida participa fluctúa con el tiempo, y depende de la temperatura. A partir de simulaciones de agua líquida TIP4P a 25 °C, se estima que cada molécula de agua participa en un promedio de 3,59 enlaces de hidrógeno. A 100 °C, este número disminuye a 3,24, debido al incremento en el movimiento molecular y consecuente densidad disminuida, mientras que a 0 °C, el número promedio de enlaces de hidrógeno se incrementa a 3,69.[7] Un estudio más reciente encontró un número mucho menor de enlaces de hidrógeno: 2,357 a 25 °C[8] Las diferencias pueden deberse al uso de un método diferente para definir y contar enlaces de hidrógeno.
Donde las fuerzas de enlace son más equivalentes, se podría encontrar los átomos de dos moléculas de agua partidas en dos iones poliatómicos de carga opuesta, específicamente hidróxido (OH−) e hidronio (H3O+). (Los iones hidronio también son conocidos como iones 'hidroxonio').
- H-O− H3O+
Sin embargo, en agua pura bajo condiciones normales de presión y temperatura, esta última formulación es aplicable solo raramente; en promedio aproximadamente una en cada 5,5 × 108 moléculas cede un protón a otra molécula de agua, en concordancia con la constante de disociación para el agua bajo tales condiciones. Es una parte crucial de la unicidad del agua.
Enlaces de hidrógeno bifurcados y sobrecoordinados en el agua
Puede darse que un solo átomo de hidrógeno participe en dos enlaces de hidrógeno, en vez de en uno. Este tipo de enlace es denominado "bifurcardo". Se ha sugerido que el enlace de hidrógeno bifurcado es un paso esencial en la reorientación del agua;.[9]
Los aceptores de enlaces de hidrógeno (que terminan en los pares libres del átomo de oxígeno) son más propensos a formar la bifurcación (en efecto, se le denomina oxígeno sobrecoordinado) que los donantes.[10]
Enlace de hidrógeno en macromoléculas y polímeros
Los enlaces de hidrógeno determinan la estructura y propiedades de diferentes sistemas macromoleculares, tanto de origen natural como sintético. Las macromoléculas de polímeros naturales tales como las proteínas (seda, seda de araña, queratinas, fibroínas, etc) o algunos polisacáridos estructurales tales como las celulosas o la quitina se encuentran en alto grado asociadas por puentes de hidrógeno. Asimismo las macromoléculas de numerosos polímeros sintéticos como las poliamidas o los poliuretanos se encuentran en distinto grado asociados por enlaces de hidrógeno.[11]
Enlaces de hidrógeno en ADN y proteínas

El enlace de hidrógeno también juega un rol importante en la determinación de las estructuras tridimensionales adoptadas por las proteínas y ácidos nucleicos. En estas macromoléculas, el enlace de hidrógeno entre partes de la misma molécula ocasiona que se doble en una forma específica, que ayuda a determinar el rol fisiológico o bioquímico de la molécula. Por ejemplo, la estructura de doble hélice del ADN se debe primordialmente a los enlaces de hidrógeno entre los pares de bases, que unen una cadena complementaria a la otra y permiten la replicación.
En las proteínas, los enlaces de hidrógeno se forman entre átomos de oxígeno esqueletales y átomos de hidrógeno amida. Cuando el espaciamiento de los residuos de aminoácido que participan en un enlace de hidrógeno es regular entre las posiciones i e i + 4, se forma una hélice alfa. Cuando el espaciamiento es menor, entre las posiciones i e i + 3, se forma una hélice 310. Cuando dos cadenas se unen por enlaces de hidrógeno que involucran residuos alternantes de cada cadena participante, se forma una lámina beta. Los enlaces de hidrógeno también toman parte en la formación de la estructura terciaria de las proteínas, a través de la interacción de los grupos R. (Véase también plegamiento de proteínas).
Enlace de hidrógeno simétrico
Un enlace de hidrógeno simétrico es un tipo especial de enlace de hidrógeno en el que el núcleo de hidrógeno está exactamente a mitad de camino entre dos átomos del mismo elemento. La fuerza del enlace a cada uno de estos átomos es igual. Constituye un ejemplo de un enlace de tres centros y dos electrones. Este tipo de enlace es mucho más fuerte que los enlaces de hidrógeno "normales". El orden efectivo de enlace es 0.5, así que su fuerza es comparable a un enlace covalente. Se ha visto en hielo a altas presiones, y también en la fase sólida de muchos ácidos anhidros, como el fluoruro de hidrógeno y el ácido fórmico a altas presiones. También se le ha visto en el anión bifluoruro [F-H-F]−.
Los enlaces de hidrógeno simétricos han sido observados recientemente espectroscópicamente en el ácido fórmico a presión alta (>GPa). Cada átomo de hidrógeno forma un enlace covalente parcial con dos átomos, en vez de con uno. Se ha postulado la existencia de enlaces de hidrógeno simétricos en el hielo a altas presiones (Hielo X). Se forman bajas barreras de enlace de hidrógeno cuando la distancia entre dos heteroátomos es muy pequeña.
Enlace de hidrógeno
El enlace de hidrógeno puede ser comparado con el cercanamente relacionado enlace de dihidrógeno, que también es una interacción enlazante intermolecular que involucra a átomos de hidrógeno. Estas estructuras han sido conocidas por algún tiempo, y bien caracterizadas por cristalografía de rayos X; sin embargo, una comprensión de su relación con el enlace de hidrógeno convencional, enlace iónico y enlace covalente permanece oscura. Generalmente, el enlace de hidrógeno está caracterizado por un aceptor de protones, que es un par libre de electrones en átomos no metálicos (principalmente en el nitrógeno y oxígeno). En algunos casos, estos aceptores de protones pueden ser orbitales pi o algún complejo metálico. Sin embargo, en el enlace de dihidrógeno, un hidruro metálico sirve como aceptor de protones; formando una interacción hidrógeno-hidrógeno.
La difracción de neutrones ha mostrado que la geometría molecular de estos complejos es similar a los enlaces de hidrógeno, en el que la longitud de enlace se adapta muy bien a los sistemas complejo metálico/donante de hidrógeno.
Teoría avanzada del enlace de hidrógeno
La naturaleza del enlace fue aclarada recientemente. Un artículo ampliamente publicado[12] probó, a partir de interpretaciones de anisotropía en el perfil de Compton del hielo ordinario, que el enlace de hidrógeno es parcialmente covalente. Parte de la información de resonancia magnética nuclear sobre los enlaces de hidrógeno en las proteínas también indica que hay enlace covalente.
Más generalmente, el enlace de hidrógeno puede ser visto como un campo escalar electrostático dependiente de la métrica, entre dos o más enlaces intermoleculares. Esto es ligeramente diferente de los estados ligados intramoleculares de, por ejemplo, el enlace covalente o el enlace iónico; sin embargo, el enlace de hidrógeno sigue siendo un fenómeno de estado ligado, puesto que la energía de interacción tiene una suma neta negativa. La teoría inicial del enlace de hidrógeno propuesta por Linus Pauling sugería que los enlaces de hidrógeno tenían una naturaleza parcialmente covalente. Esto permaneció como una conclusión controvertida hasta finales de la década de 1990, cuando mediante técnicas de RMN empleadas por F. Cordier et al. para transferir información entre núcleos enlazados por hidrógeno, una característica que solo sería posible si el enlace de hidrógeno contuviera algún carácter covalente.
Fenómenos debidos al enlace de hidrógeno
- Punto de ebullición mucho más alto del NH3, H2O y HF, en comparación con compuestos análogos más pesados PH3, H2S, y HCl
- Viscosidad del ácido fosfórico anhidro y del glicerol.
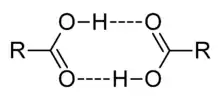
- Formación de dímeros en ácidos carboxílicos y de hexámeros en el fluoruro de hidrógeno, que ocurre incluso en fase gaseosa, resultando en grandes desviaciones de la ley de los gases ideales.
- La alta solubilidad en agua de muchos compuestos como el amoníaco es explicada por el enlace de hidrógeno con las moléculas de agua.
- La azeotropía negativa de mezclas de HF y agua.
- La delicuescencia del NaOH es causada, en parte, por la reacción de OH- con la humedad para formar especies H3O2- enlazadas por hidrógeno. Un proceso análogo sucede entre la NaNH2 y el NH3, y entre el NaF y el HF.
- El hecho de que el hielo sea menos denso que el agua líquida se debe a una estructura cristalina estabilizada por enlaces de hidrógeno.
- La presencia de enlaces de hidrógeno puede causar una anomalía en la sucesión normal de los estados de agregación para ciertas mezclas de compuestos químicos, con el incremento o disminución de temperatura. Estos compuestos pueden ser líquidos hasta una cierta temperatura, luego son sólidos incluso con el incremento de temperatura, y finalmente líquidos cuando la temperatura se eleva sobre el "intervalo anómalo".[13]
- La goma inteligente utiliza enlaces de hidrógeno como su única forma de enlace, así que puede "sanarse" cuando se pincha, debido a que puede aparecer nuevos enlaces de hidrógeno entre las dos superficies del mismo polímero.
Enlace de hidrógeno o enlace por puente de hidrógeno
Tanto enlace de hidrógeno o enlace por puente de hidrógeno son correctos pero tienen significados muy distintos. En este caso el término que hace referencia a la fuerza eminentemente electrostática atractiva entre un átomo electronegativo y un átomo de hidrógeno unido covalentemente a otro átomo electronegativo es el enlace de hidrógeno. Tanto en castellano como en inglés se ha extendido el término puente de hidrógeno pero este nombre es incorrecto y no es recomendable usarlo, aunque en muchos libros de texto se siga usando.
Según IUPAC en inglés se escribe hydrogen bond (enlace de hidrógeno) y no hydrogen bridged bond (enlace por puente de hidrógeno) o hydrogen bridge (puente de hidrógeno). Por lo tanto, hay que hacer una traducción directa a todas las demás lenguas incluido el castellano y en consecuencia el término correcto es enlace de hidrógeno.
La confusión entre los dos términos se originó en inglés y se extendió a los demás idiomas. Después se corrigió el término en inglés, pero en algunos idiomas como el castellano el error ha quedado demasiado profundizado. Tanto es así, que es habitual leer libros de texto recientes que siguen usando mal el término. Además de eso, el hecho de que el enlace de hidrógeno no sea un enlace químico sino un enlace intermolecular ha favorecido el uso de la palabra puente, lo cual evita la confusión de pensar que el enlace de hidrógeno sea un enlace químico equivalente al enlace covalente o el iónico. En los libros de texto de secundaria muchas veces se usa la palabra puente para que los estudiantes que no están familiarizados con la terminología química no mezclen los conceptos. En campos como la farmacia, la biología, la genética, las ingenierías... también se pueden encontrar libros que no dominan del todo la terminología química y que usan la palabra puente para referirse a esta interacción, pero su uso sigue siendo erróneo.
En realidad, los puentes de hidrógeno no tienen nada que ver con los enlaces de hidrógeno. Los puentes de hidrógeno son enlaces covalentes no convencionales que se crean para que un compuesto determinado se estabilice. Por ejemplo, en el caso de los boranos, el borano más simple (BH3) es inestable debido a que en esta molécula el boro solo puede tener seis electrones de valencia y no ocho como cabríia esperar en los elementos del segundo periodo, los cuales se estabilizan al tener ocho electrones de valencia. En consecuencia, el trihidruro de boro tiende a unirse con otra molécula para crear el diborano B2H6, donde se crean dos puentes de hidrógenos para que cada boro tenga ocho electrones de valencia a su disposición y por lo tanto la configuración de los gases nobles (en este caso el neón). Cada puente de hidrógeno se forma mediante B-H-B y al contrario que un enlace covalente convencional, donde se usan dos electrones para unir dos átomos (2c-2c), se usan un par de electrones para unir los tres átomos (3c-2e). Por lo tanto, cada boro consigue los ocho electrones de valencia que necesita para su estabilidad. A esto se le llama “puente de hidrógeno”, que no tiene nada que ver con “enlace de hidrógeno”.
Se ha explicado el caso del diborano, pero existen muchos tipos de boranos con estructuras mucho más complejas y existen más tipos de enlaces aparte de los puentes de hidrógeno. Estos son los diferentes enlaces que pueden llegar a presentar los boranos
- BH = 2c-2e Enlace boro-hidrógeno terminal
- BHB = 3c-2e Enlace por puente de hidrógeno
- BB = 2c‑2e Enlace boro-boro
- BBB = 3c-2e Enlace por puente de boro abierto
- BBB = 3c-2e Enlace de boro cerrado
El objetivo de explicar la estructura de los boranos y sus enlaces es el de hacer comprender al lector que el enlace por puente de hidrógeno tiene una naturaleza muy diferente a la del enlace de hidrógeno.[14][15][16][17]
Referencias
- Felix H. Beijer, Huub Kooijman, Anthony L. Spek, Rint P. Sijbesma, E. W. Meijer (1998). «Self-Complementarity Achieved through Quadruple Hydrogen Bonding». Angew. Chem. Int. Ed. 37: 75-78. doi:10.1002/(SICI)1521-3773(19980202)37:1/2<75::AID-ANIE75>3.0.CO;2-R.
- Unión Internacional de Química Pura y Aplicada. «hydrogen bond». Compendium of Chemical Terminology. Versión en línea (en inglés).
- Campbell, Neil A.; Brad Williamson; Robin J. Heyden (2006). Biology: Exploring Life. Boston, Massachusetts: Pearson Prentice Hall. ISBN 0-13-250882-6.
- Emsley, J. (1980). «Very Strong Hydrogen Bonds». Chemical Society Reviews 9: 91-124. doi:10.1039/cs9800900091.
- Omer Markovitch and Noam Agmon (2007). «Structure and energetics of the hydronium hydration shells». J. Phys. Chem. A 111 (12): 2253-2256. doi:10.1021/jp068960g.
- A. C. Legon;D. J. Millen. Chem. Soc. Rev. 1987, 16,467-498.
- W. L. Jorgensen and J. D. Madura (1985). «Temperature and size dependence for Monte Carlo simulations of TIP4P water». Mol. Phys. 56 (6): 1381. doi:10.1080/00268978500103111.
- Jan Zielkiewicz (2005). «Structural properties of water: Comparison of the SPC, SPCE, TIP4P, and TIP5P models of water». J. Chem. Phys. 123: 104501. doi:10.1063/1.2018637..
- Damien Laage and James T. Hynes (2006). «A Molecular Jump Mechanism for Water Reorientation». Science 311: 832. PMID 16439623. doi:10.1126/science.1122154.
- Omer Markovitch & Noam Agmon (2008). «The Distribution of Acceptor and Donor Hydrogen-Bonds in Bulk Liquid Water». Molecular Physics 106: 485. ISBN 8970701877921
|isbn=incorrecto (ayuda). doi:10.1080/00268970701877921. - L. C. Cesteros-Iturbe (2004). Aplicaciones de la FTIR al estudio de las interacciones polímero-polímero. Revista Iberoamericana de Polímeros, 5(3), 111-132
- E.D. Isaacs, et al., Physical Review Letters vol. 82, pp 600-603 (1999)
- Law-breaking liquid defies the rules Archivado el 29 de abril de 2011 en Wayback Machine. at physicsworld.com
- Brown, H. C., Boranes in Organic Chemistry, Comell University Press, 1972.
- Muetterties, E. L., ed., The Chemistry of Boron and its Compounds, Wiley, 1967
- Boscke, F., ed., New Results in Boron Chemistry, Fortschritte der Chemischen Forschung, Springer Verlag, 1971
- Muetterties, E. L. y Knoth, W. H., Polyhedral Boranes, Dekker, 1968
- George A. Jeffrey. An Introduction to Hydrogen Bonding (Topics in Physical Chemistry). Oxford University Press, USA (March 13, 1997). ISBN 0-19-509549-9
- Robert H. Crabtree, Per E. M. Siegbahn, Odile Eisenstein, Arnold L. Rheingold, and Thomas F. Koetzle (1996). «A New Intermolecular Interaction: Unconventional Hydrogen Bonds with Element-Hydride Bonds as Proton Acceptor». Acc. Chem. Res. 29 (7): 348-354. doi:10.1021/ar950150s.
- Alexander F. Goncharov, M. Riad Manaa, Joseph M. Zaug, Richard H. Gee, Laurence E. Fried, and Wren B. Montgomery (2005). «Polymerization of Formic Acid under High Pressure». Phys. Rev. Lett. 94 (6): 065505. doi:10.1103/PhysRevLett.94.065505.
- F. Cordier, M. Rogowski, S. Grzesiek and A. Bax (1999). «Observation of through-hydrogen-bond (2h)J(HC') in a perdeuterated protein». J Magn Reson. 140: 510-2. doi:10.1006/jmre.1999.1899.
- R. Parthasarathi, V. Subramanian, N. Sathyamurthy (2006). «Hydrogen Bonding Without Borders: An Atoms-In-Molecules Perspective». J. Phys. Chem. (A) 110: 3349-3351.
- Z. Liu, G. Wang, Z. Li, R. Wang (2008). «Geometrical Preferences of the Hydrogen Bonds on Protein−Ligand Binding Interface Derived from Statistical Surveys and Quantum Mechanics Calculations». J. Chem. Theory Comput. (A) 4 (11): 1959-1973. doi:10.1021/ct800267x.
Enlaces externos
- The Bubble Wall (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última). (presentación de diapositivas del National High Magnetic Field Laboratory explicando la cohesión, tensión superficial y enlaces de hidrógeno; en inglés).
