كيمياء حيوية لاعضوية
الكيمياء الحيوية اللاعضوية هي الحقل الذي يدرس دور المعادن في علم الأحياء، ويتضمن هذا النوع من الكيمياء دراسة الظواهر الطبيعية كسلوك البروتينات المعدنية ودراسة المعادن المنتجة صناعياً بما فيها ما يسمى المعادن اللاأساسية. في الطب وعلم السموم: تدخل العديد من العمليات الحيوية، كالتنفس، دنيا الكيمياء اللاعضوية، ويندرج تحت هذا العنوان أيضاً دراسة النماذج والمشابهات التي تحاكي سلوك البروتينات المعدنية.[1]
وكخليط من الكيمياء الحيوية والكيمياء اللاعضوية، فالكيمياء الحيوية اللا عضوية مهمة في توضيح آثار البروتينات المنقولة إلكترونياً وروابط الركيزة وتفعيلها والذرة ومجموعة النواقل الكيميائية فضلاً عن البروتينات المعدنية في الكيمياء الحيوية.
تركيب العضويات الحية
حوالي 99% من كتلة الثدييات يتكون من العناصر: الكربون والنتروجين والكالسيوم والصوديوم والكلور والبوتاسيوم والهيدروجين والفوسفور والأكسجين والكبريت.[2] تحوي المركبات العضوية (البروتينات والسكريات والشحوم) غالبية من الكربون والنتروجين ومعظم الأكسجين والهدروجين موجود على شكل ماء، والمجموع الكلي للجزيئات الحيوية الحاوية على المعدن في الخلية يدعى «الجزء المعدني» (الميتالوم The metallome).
تاريخ
استخدم بول إيرليك (باول إرليخ) الزرنيخ العضوي (من المواد الزرنيخية) لعلاج الزهري (الداء الإفرنجي)، مما يدل على أهمية المعادن، أو أشباه المعادن على أقل تقدير، في الطب، الأمر الذي أبصر النور مع اكتشاف روزنبرغ (Rosenberg) الدور المضاد للسرطان للسيسبلاتين (cis-PtCl2(NH3)2)). يعتبر اليورياز (يورياز) أول بروتين يُبلوَر على الإطلاق، (انظر جيمس ب. سومنر جيمس سومنر)، وظهر لاحقاً احتواؤه على النيكل في موقعه النشط.
شوهد Vitamin B12 (فيتامين ب12)، لب فقر الدم الوبيل، مبلوراً بيانياً من قبل دوروثي كروفوت هودجكن (دوروثي هودجكن) مما يؤكد وجود الكوبالت في كرية حمراء كبْروية كورينية. أظهرت بنية واطسون وكريك (Watson-Crick) للدنا أن البوليميرات الحاوية على الفوسفات تلعب دوراً بنيوياً مفتاحياً.
المواضيع في الكيمياء الحيوية اللاعضوية
هناك عدة أنظمة بيّنة عن المتمايزات في الكيمياء الحيوية اللاعضوية، المجالات الرئيسة هي:
النقل والتخزين الشاردي المعدني
يغطي هذا الموضوع مجموعة من القنوات الشاردية والمضخات الشاردية (مضخة صوديوم-بوتاسيوم على سبيل المثال) والفجوات وحاملات الحديد، وبعض البروتينات والجزيئات الصغيرة والتي تتحكم بتركيز الشوارد المعدنية في الخلايا، إن العديد من المعادن المطلوبة استقلابياً غير متاحة بسهولة، ويعزى ذلك إلى الندرة والذوبان، مما يعتبر قضية جدّية. وقد طورت العضويات عدداً من الإستراتيجيات لجمع مثل هذه العناصر ونقلها.
علم الإنزيمات
إن العديد من التفاعلات في العلوم الحياتية ومن ضمنها الماء والشوارد المعدنية غالباً ما تكون في المراكز التحفيزية (المواقع الفعالة) لهذه الإنزيمات، أي البروتينات المعدنية. غالباً ما يكون الماء المتفاعل لجيناً (انظر المعقد المائي المعدني)، ومن الأمثلة: إنزيمات الهيدراز هي أنهيدرازات كربونية، الإنزيمات المعدنية الفوسفاتية، الإنزيمات البروتينية المعدنية. يسعى الكيميائي الحيوي اللاعضوي لفهم وتكرار وظائف هذه البروتينات المعدنية.
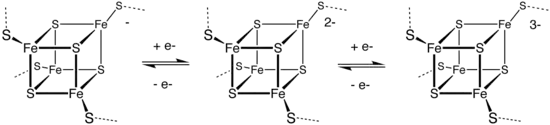
وإن البروتينات ناقلة الإلكترون المتضمنة للمعدن شائعة أيضاً. ويمكن تصنيفها ضمن ثلاثة طبقات رئيسة: بروتينات شوارد الكبريت (كالريبريدوكسين والفيريدوكسين والبروتينات الرسكية)، فبروتينات النحاس الأزرق، فالسيتوكرومات. تعتبر هذه البروتينات ناقلة الإلكترون متممة للنواقل الإلكترونية اللامعدنية كالنيكوتيناميد أدنين ثنائي النوكليوتيد (ناد NAD) والفلافين أدنين ثنائي النوكليوتيد (فاد FAD). تشكل حلقة النتروجين استعمالاً للمعادن ممتداً لأجل التحويل البيني المسترجع.
بروتينات التفعيل ونقل الأكسجين
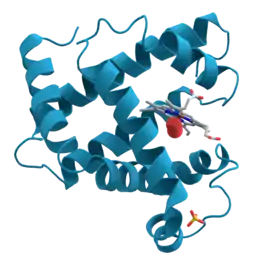
تتطلب الحياة الهوائية استعمالاً واسعاً للمعادن كالحديد والنحاس والمنغنيز، تستعمل كريات الدم الحمراء ما نسميه بالخضاب (الهيم) الموجود في صيغة خضاب الدم (الهيموغلوبين) لنقل الأكسجين، ولعله يكون أكثر الأنظمة المعدنية ملاحظة في علم الأحياء. ومن أنظمة نقل الأكسجين الأخرى هناك: الميوغلوبين (يمكننا أن نشير إليه على أنه الخضاب العضلي) والهيموسيانين وأخيراً الهيميريثرين (مادة في دم ديدان الأرض). يعتبر كل من الأكسيداز والأكسيجيناز نظامين معدنيَين وجدا في الطبيعة حيث يُستفاد من الأكسجين في إنفاذ تفاعلات مهمة كتوليد الطاقة في السيتوكروم ج أكسيداز (Cytochrome c Oxidase) أو في أكسدة جزيئات صغيرة في السيتوكروم ب450 أكسيداز (Cytochrome P450 Oxidase) أو في الميتان أحادية الأكسيجيناز. صُممت بعض البروتينات المعدنية لحماية الأنظمة الحيوية من الآثار المؤذية المحتملة للأكسجين أو غيره من الجزئيات المتفاعلة الحاوية على الأكسجين كبيروكسيد الهيدروجين، تتضمن هذه الأنظمة: البيروكسيداز والكاتالاز وفوق أكسيد الديسموتاز. إن أحد متممات البروتينات المعدنية لتلك التي تتفاعل مع الأكسجين هو معقّد الأكسجين التطوري الموجود في النباتات، ويعتبر هذا النظام جزءاً من آلية البروتين المعقدة والتي تنتج الأكسجين عندما تأدية النباتات لعملية التركيب الضوئي.
الكيمياء الحيوية العضوية المعدنية
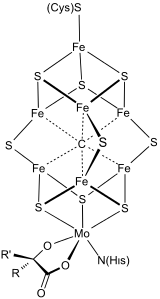
تبرز الأنظمةُ الحيوية العضوية المعدنية (الفِلِزّيّة) الروابطَ الكربونية-المعدنية كعناصر بنيوية أو كوسائط، وتتضمن الإنزيمات والبروتينات الحيوية العضوية المعدنية الهيدروجيناز والـ (FeMoco) في النتروجيناز بالإضافة إلى الميثيل كوبالامين، ويصدر هؤلاء طبيعياً المركبات العضوية المعدنية. تركز هذه الباحة أكثر على استعمال المعادن من قبل العضويات وحيدات الخلية، وتعتبر المركبات العضوية المعدنية مركبات ذات معنى في الكيمياء البيئية.[3]
المعادن في المجال الطبي
يحتوي عدد من الأدوية على المعادن، يعول هذا الموضوع على دراسة تصميم وآليات تأثير المستحضرات الدوائية الحاوية على المعدن، والمركبات التي تتفاعل مع الشوارد المعدنية ذاتية المنشأ في مواقع الإنزيم الفعالة. يعتبر السيسبلاتين أكثر الأدوية المضادة للسرطان استعمالاً على نطاق واسع، احتواء عامل التباين في الرنين المغناطيسي MRI على الغادولينيوم يعتبر أمراً شائعاً، استخدمت كربونات الليثيوم لعلاج الطور الهوسي من الاضطراب ثنائي القطب. وقد سُوقت الأدوية المضادة لالتهاب المفاصل الذهبية تجارياً، الأورانوفين على سبيل المثال وهو دواء مضاد للروماتيزم. تعتبر الجزيئات المطلقة لأحادي أكسيد الكربون معقداتٍ معدنية طُوِّرت لكبح وكبت الالتهاب عبر إطلاقها كميات قليلة من أحادي أكسيد الكربون. وقد فحصت أهمية أكسيد النتريك العصبونية والقلبية الوعائية، متضمناً إنزيم أكسيد النتريك سينثاز (انظر أيضاً: تمثُّل النتروجين).
الكيمياء البيئية
تشدد الكيمياء البيئية تقليدياً على على التفاعل بين المعادن الثقيلة والعضويات، وقد سبب أكليل الزئبق كارثة كبيرة سُميت داء ميناماتا، ويعتبر التسمم الزرنيخي مشكلة واسعة الانتشار وتعزى بشكل أساسي إلى تلوث المياه الأرضية بالزرنيخ، الأمر الذي يؤثر على عدة ملايين من الناس في البلاد النامية. يتطلب استقلاب الزئبق والمركبات الحاوية على الزرنيخ إنزيمات الكوبالامين القاعدية.
التمعدن الحيوي
توصف عملية التمعدن الحيوي بأنها العملية التي تنتج العضويات الحية المعادنَ فيها، غالباً يكون هدفها تقسية وتصليب نسج موجودة. مثل هذه الأنسجة تسمّى بالنسج المتمعدنة[4][5][6] ؛ وتعد كل من السيليكات في الطحالب والمشطورات والكربونات في اللافقاريات بالإضافة إلى فوسفات الكالسيوم والكربونات في الفقاريات أمثلة على هذه النسج. ومن الأمثلة الأخرى: النحاس والحديد والذهب المترسبة في الجراثيم المنطوية عليها. غالباً ما يكون للمعادن المشكلة حيوياً استعمالات خاصة كالحاسة الممغنطة في الجراثيم ذات الانجذاب المغناطيسي (Fe3O4) وكذلك أجهزة تحسس الجاذبية (CaCO3, CaSO4, BaSO4) وتخزين ونقل الحديد (Fe2O3•H2O في بروتين الفيريتين). ولأن الحديد خارج الخلوي[7] متورط بشدة في التحريض على التكلس [8][9] فالتحكم به أساسي في القشور النامية، ولبروتين الفيريتين دورٌ هام في التحكم بتوزُّع الحديد.[10]
أنواع من العناصر اللاعضوية في علم الأحياء
المعادن (الفِلِزّات) الأرضية القلوية
تتصرف العناصر اللاعضوية الوفيرة كشوارد كهرلية (تنحل بالكهرباء)، وأكثر هذه الشوارد أهمية هي الصوديوم والبوتاسيوم والكالسيوم والمغنزيوم والكلوريد والفوسفات بالإضافة إلى شوارد البيكربونات العضوية. وتحفظ الكمية الدقيقة المضبوطة للمواد العابرة للأغشية الخلوية معدلات الضغط الحلولي والحامضية PH.[12] كما أنها -أي الشوارد- ذات أهمية خاصة بالنسبة للأعصاب والعضلات، ككوامن فعل في هذه الأنسجة منتجة من التبادل بين الكهرليات من جهة والسائل خارج الخلوي والعصارة الخلوية.[13] من جهة أخرى، تدخل الكهرليات إلى الخلية وتخرج منها عبر بروتينات في الغشاء الخلوي تدعى القنوات الشاردية، فعلى سبيل المثال؛ يعتمد التقلص العضلي على الكالسيوم والصوديوم والبوتاسيوم خلال القنوات الشاردية والنُبيبات المستعرضة.[14]
المعادن المتحولة
غالباً ما توجد المعادن المتحولة كعناصر زهيدة في العضويات، مع كون الزنك والحديد الأكثر وفرة[15][16][17]، تستخدم هذه المعادن في البروتينات على شكل تمائم وتعد أساسية لنشاط الإنزيمات كالكاتالاز والبروتين الحاملة للأكسجين كخضاب الدم.[18] ترتبط هذه التمائم بشدة إلى بروتينات محددة، وعلى الرغم من أن تمائم الإنزيم يمكن تعديلها خلال الطور التحفيزي، إلا أن هذه التمائم دائماً ما تعود إلى حالتها الأولية بعد انتهاء التحفيز. تضمن المغذيات زهيدة المقدار المعدنية في العضويات عبر نواقل معينة وتربط إلى بروتينات التخزين كالفيريتين أو الثيونين المعدني عند عدم استخدامها.[19][20] يعتبر الكوبالت أساسياً لوظيفة فيتامين ب12.[21]
مركبات المجموعة الأساسية
تعتبر العديد من العناصر علاوة على المعادن فعالة حيوياً، وإن السُلْفار والفوسفور مطلوبان مدى الحياة، ويكاد ينحصر وجود الفوسفور على الفوسفات واستراته المختلفة، أما السلفور فيوجد بضروب متنوعة من حالات الأكسدة. تتراوح من سلفات (SO42−) وصولاً إلى (S2−). أما السيلينيوم فيعد عنصراً زهيداً مضمناً ضمن بروتينات تتميز بكونها مضادة للأكسدة. أما الكادميوم فمهم لمسيّته.[22]
انظر أيضاً
المصادر
- Stephen J. Lippard, Jeremy M. Berg, Principles of Bioinorganic Chemistry, University Science Books, 1994, ISBN 0-935702-72-5
- Heymsfield S, Waki M, Kehayias J, Lichtman S, Dilmanian F, Kamen Y, Wang J, Pierson R (1991)، "Chemical and elemental analysis of humans in vivo using improved body composition models"، Am J Physiol، 261 (2 Pt 1): E190–8، PMID 1872381.
{{استشهاد بدورية محكمة}}: صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Sigel, A.؛ Sigel, H.؛ Sigel, R.K.O., المحررون (2010)، Organometallics in Environment and Toxicology، Metal Ions in Life Sciences، Cambridge: RSC publishing، ج. 7، ISBN 978-1-84755-177-1.
- Astrid Sigel, Helmut Sigel and Roland K.O. Sigel, المحرر (2008)، Biomineralization: From Nature to Application، Metal Ions in Life Sciences، Wiley، ج. 4، ISBN 978-0-470-03525-2.
- Weiner, Stephen; Lowenstam, Heinz A. (1989)، On biomineralization، Oxford [Oxfordshire]: Oxford University Press، ISBN 0-19-504977-2.
{{استشهاد بكتاب}}: صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Jean-Pierre Cuif, Yannicke Dauphin, James E. Sorauf (2011)، Biominerals and fossils through time، Cambridge، ISBN 978-0-521-87473-1.
{{استشهاد بكتاب}}: صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Gabbiani G, Tuchweber B (1963)، "The role of iron in the mechanism of experimental calcification"، J Histochem Cytochem، 11 ((6)): 799–803، doi:10.1177/11.6.799، مؤرشف من الأصل في 14 أبريل 2020، اطلع عليه بتاريخ أغسطس 2020.
{{استشهاد بدورية محكمة}}: تحقق من التاريخ في:|تاريخ الوصول=(مساعدة) - Schulz, K.؛ Zondervan, I.؛ Gerringa, L.؛ Timmermans, K.؛ Veldhuis, M.؛ Riebesell, U. (2004)، "Effect of trace metal availability on coccolithophorid calcification."، Nature، 430 (7000): 673–676، Bibcode:2004Natur.430..673S، doi:10.1038/nature02631، PMID 15295599.
- Anghileri, L. J.؛ Maincent, P.؛ Cordova-Martinez, A. (1993)، "On the mechanism of soft tissue calcification induced by complexed iron"، Experimental and toxicologic pathology : official journal of the Gesellschaft fur Toxikologische Pathologie، 45 (5–6): 365–368، doi:10.1016/S0940-2993(11)80429-X، PMID 8312724.
- Jackson, D. J.؛ Wörheide, G.؛ Degnan, B. M. (2007)، "Dynamic expression of ancient and novel molluscan shell genes during ecological transitions"، BMC Evolutionary Biology، 7: 160، doi:10.1186/1471-2148-7-160، PMC 2034539، PMID 17845714.
- Greenwood, Norman N.؛ Earnshaw, Alan (1997)، Chemistry of the Elements (ط. الثانية)، Butterworth-Heinemann، ISBN 0-08-037941-9.
- Sychrová H (2004)، "Yeast as a model organism to study transport and homeostasis of alkali metal cations" (PDF)، Physiol Res، 53 Suppl 1: S91–8، PMID 15119939، مؤرشف من الأصل (PDF) في 8 أغسطس 2017.
- Levitan I (1988)، "Modulation of ion channels in neurons and other cells"، Annu Rev Neurosci، 11: 119–36، doi:10.1146/annurev.ne.11.030188.001003، PMID 2452594.
- Dulhunty A (2006)، "Excitation-contraction coupling from the 1950s into the new millennium"، Clin Exp Pharmacol Physiol، 33 (9): 763–72، doi:10.1111/j.1440-1681.2006.04441.x، PMID 16922804.
- Dlouhy, Adrienne C.؛ Outten, Caryn E. (2013)، "Chapter 8 The Iron Metallome in Eukaryotic Organisms"، في Banci, Lucia (Ed.) (المحرر)، Metallomics and the Cell، Metal Ions in Life Sciences، Springer، ج. 12، doi:10.1007/978-94-007-5561-1_8، ISBN 978-94-007-5560-4. electronic-book ISBN 978-94-007-5561-1 ISSN 1559-0836 electronic-ISSN 1868-0402
- Mahan D, Shields R (1998)، "Macro- and micromineral composition of pigs from birth to 145 kilograms of body weight"، J Anim Sci، 76 (2): 506–12، PMID 9498359، مؤرشف من الأصل في 30 أبريل 2011.
- Husted S, Mikkelsen B, Jensen J, Nielsen N (2004)، "Elemental fingerprint analysis of barley (Hordeum vulgare) using inductively coupled plasma mass spectrometry, isotope-ratio mass spectrometry, and multivariate statistics"، Anal Bioanal Chem، 378 (1): 171–82، doi:10.1007/s00216-003-2219-0، PMID 14551660.
{{استشهاد بدورية محكمة}}: صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Finney L, O'Halloran T (2003)، "Transition metal speciation in the cell: insights from the chemistry of metal ion receptors"، Science، 300 (5621): 931–6، Bibcode:2003Sci...300..931F، doi:10.1126/science.1085049، PMID 12738850.
- Cousins R, Liuzzi J, Lichten L (2006)، "Mammalian zinc transport, trafficking, and signals"، J Biol Chem، 281 (34): 24085–9، doi:10.1074/jbc.R600011200، PMID 16793761، مؤرشف من الأصل في 05 نوفمبر 2008.
{{استشهاد بدورية محكمة}}: صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Dunn L, Rahmanto Y, Richardson D (2007)، "Iron uptake and metabolism in the new millennium"، Trends Cell Biol، 17 (2): 93–100، doi:10.1016/j.tcb.2006.12.003، PMID 17194590.
{{استشهاد بدورية محكمة}}: صيانة CS1: أسماء متعددة: قائمة المؤلفون (link) - Cracan, Valentin؛ Banerjee, Ruma (2013)، "Chapter 10 Cobalt and Corrinoid Transport and Biochemistry"، في Banci, Lucia (Ed.) (المحرر)، Metallomics and the Cell، Metal Ions in Life Sciences، Springer، ج. 12، doi:10.1007/978-94-007-5561-10_10، ISBN 978-94-007-5560-4. electronic-book ISBN 978-94-007-5561-1 ISSN 1559-0836 electronic-ISSN 1868-0402
- Maret, Wolfgang؛ Moulis, Jean-Marc (2013)، "Chapter 1. The Bioinorganic Chemistry of Cadmium in the Context of its Toxicity"، في Astrid Sigel, Helmut Sigel and Roland K. O. Sigel (المحرر)، Cadmium: From Toxicology to Essentiality، Metal Ions in Life Sciences، Springer، ج. 11، ص. 1–30.
- بوابة الكيمياء
- بوابة الكيمياء الحيوية