Tellure
Le tellure est l'élément chimique de numéro atomique 52, de symbole Te. Ce quatrième élément du groupe VI A est considéré comme un métalloïde du groupe des chalcogènes.
| Tellure | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Disque de tellure de 3,5 cm de diamètre. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Position dans le tableau périodique | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Symbole | Te | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom | Tellure | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Numéro atomique | 52 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe | 16 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Période | 5e période | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bloc | Bloc p | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Famille d'éléments | Métalloïde | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuration électronique | [Kr] 4d10 5s2 5p4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électrons par niveau d’énergie | 2, 8, 18, 18, 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés atomiques de l'élément | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse atomique | 127,60 ± 0,03 u[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon atomique (calc) | 140 pm (123 pm) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de covalence | 138 ± 4 pm[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de van der Waals | 206 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| État d’oxydation | ±2, 4, 6 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électronégativité (Pauling) | 2,1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxyde | Acide faible | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergies d’ionisation[3] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1re : 9,009 6 eV | 2e : 18,6 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3e : 27,96 eV | 4e : 37,41 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5e : 58,75 eV | 6e : 70,7 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7e : 137 eV | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopes les plus stables | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés physiques du corps simple | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| État ordinaire | Solide diamagnétique | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Allotrope à l'état standard | Cristallisé | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Autres allotropes | Amorphe | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse volumique | 6,23 g·cm-3 (20 °C)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Système cristallin | Hexagonal | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureté (Mohs) | 2,25 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Couleur | Gris argenté | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point de fusion | 449,51 °C[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point d’ébullition | 988 °C[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergie de fusion | 17,49 kJ·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergie de vaporisation | 114,1 kJ·mol-1 (1 atm, 988 °C)[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molaire | 20,46×10-3 m3·mol-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pression de vapeur | 1,3 mbar (520 °C)[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vitesse du son | 2 610 m·s-1 à 20 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chaleur massique | 202 J·kg-1·K-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité électrique | 200 S·m-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité thermique | 2,35 W·m-1·K-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilité | sol. dans HCl + bromate[5] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Divers | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No CAS | [6] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No ECHA | 100.033.452 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No CE | 236-813-4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Précautions | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH[4] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Attention |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unités du SI & CNTP, sauf indication contraire. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Cet article concerne l'élément chimique nommé tellurium en latin, le corps simple et ses composés ou combinaisons. Pour l' autre signification, voir Tellure (musée).
Généralités et histoire


L'élément tellure a été soupçonné plus que découvert en 1782 par Franz-Joseph Müller von Reichenstein dans des minerais d'or de Transylvanie, en particulier la sylvanite. Grâce à Pál Kitaibel, qui a entretenu la flamme de la recherche, il a été isolé par Martin Heinrich Klaproth qui a proposé le nom latin tellurium en 1798. « Tellurium » est encore le nom anglais de l'élément. Ce nom dérive du mot latin féminin tellus, telluris, signifiant la Terre, le globe terrestre et accessoirement en mythologie ancienne la déesse romaine de la Terre, Tellus.
Le tellurium a été découvert moins de deux décennies avant le sélénium, dont le nom fait référence à la Lune. Le Suédois Berzelius, spécialiste des occurrences et des impuretés du tellurium, a prouvé l'existence du corps simple et de l'élément sélénium dans les chambres de plomb du procédé menant à l'acide sulfurique. Le chimiste n'a publié qu'en 1818 après avoir assimilé les rudiments, quasi-analogues, de la chimie des corps simples et composés de ces deux éléments[7]. Il a de suite simplifié ces noms en leurs initiales Te et Se, devenus depuis leurs symboles chimiques. Se et Te font partie du groupe VI A, constitué des éléments O, S, Se, Te, Po et Lv. La chimie du S, du Se et du Te présente un grand nombre d'analogies, comme le reconnaissait déjà Berzélius. La plupart des composés de ces trois éléments sont isomorphes. De plus, dans la nature, ces trois éléments analogues sont souvent réunis.
L'adjectif « telluré » qualifie un corps chimique, un minéral ou une matière qui contient du tellure en proportion notable. L'adjectif « tellurifère » indique plutôt la présence non négligeable de matière tellurée dans un assemblage connu ou inconnu.
Isotopes
Le tellure possède 38 isotopes connus, de nombre de masse variant entre 105 et 142, et 17 isomères nucléaires. Parmi ces isotopes, 6 sont stables, 120Te, 122Te, 123Te, 124Te, 125Te et 126Te et deux radioisotopes à très longue demi-vie, 128Te et 130Te. Ces 8 isotopes constituent la totalité du tellure naturel, les deux radioisotopes étant les plus abondants (respectivement 31,7 % et 34,1 % du tellure naturel), suivi de 126Te (18,8 %). Le tellure partage ainsi cette caractéristique avec l'indium et le rhénium d'avoir des radioisotopes naturels plus abondants que ses isotopes stables. La masse atomique standard attribuée au tellure est de 127,60(3) u.
Occurrences dans les milieux naturels, minéralogie et géologie
Le clarke est 0,002 g/t. S'il est à l'origine d'un corps simple naturel, il est surtout associé à des éléments chalcophiles, en particulier Au, Ag, Fe, Hg, Se, As, Sb.

Le tellure se caractérise par une grande diversité minéralogique : on connaît 158 minéraux tellurés, ce qui est exceptionnel pour un élément aussi peu abondant dans la croûte terrestre. Les ions (poly)tellurites ou les tellurates, stables en milieu très alcalin, sont toutefois très rares dans la nature.
Il n'existe que très peu de minéraux spécifiques du tellure. La tellurite TeO2, appelée autrefois tellurine[réf. nécessaire], est un minéral rare.
Gisements
Le tellure est aussi trouvé souvent en combinaison avec l'or Au, le plomb Pb, le bismuth Bi, l'antimoine Sb, etc.
Le gisement de tellure le plus profond connu est à 2 690 mètres sous terre dans le bouclier canadien. Il est associé au bloc 123A et l'extraction aurait dû débuter en 2012. [citation nécessaire] Une confirmation est obtenue à la suite de la découverte de tellure à 2 990 mètres de profondeur dans une « carotte » de forage au diamant de calibre BQ[8]. Sa qualité de plus grand gisement de tellure semble se dessiner avec la présence de ces mêmes tellures à 2 590 mètres. Le plus intéressant est que ces tellures, contrairement à ceux de hautes teneurs en or, ne semblent pas bouger dans l'espace et sont donc beaucoup plus faciles à cibler et à extraire pour un ingénieur.
Un indice sous le niveau 311 (3 110 m de profondeur) montre de possibles tellurures carbonifères. Soumis à de fortes pressions, de possibles diamants bruts pourraient ainsi s'y retrouver, même si on les retrouve habituellement entre 120-150 km de profondeur. Il se retrouve dans une matrice de porphyroblaste. Ce serait le premier gisement aurifère-diamantifère au monde[citation nécessaire].

Corps simples et corps composés chimiques
Le tellure peut être rapproché du sélénium. Plus lourd, il s'en distingue par un caractère plus métallique. Notez qu'il a été, à l'instar du sélénium, trouvé presque partout à la Belle Époque dans les chambres à plomb lors de l'ancienne fabrication de l'acide sulfurique, par exemple par le chimiste anglais Edward Divers expatrié au Japon.
Le corps simple, ses propriétés et sa chimie de base

Le corps simple tellure polymorphe existe dans la nature essentiellement sous la forme grise, à savoir un corps d'aspect métallique, semi-conducteur cassant, blanc bleuâtre, parfois blanc gris, lamelleux et fragile. Ce corps cristallin de maille hexagonale, de densité moyenne 6,25 et fondant avant 500 °C est encore nommé tellure natif par les minéralogistes car il appartient la catégorie des éléments natifs[9]. Le tellure brun, amorphe et bien plus rare, se transforme à température ambiante en tellure gris métal hexagonal.

Le tellure gris obtenu et purifié au laboratoire est le plus souvent un métalloïde ou semi-métal argenté, parfois gris acier, cassant et facilement pulvérisé (poudre grise à brunâtre) à odeur alliacée[10]. Sa masse volumique avoisine 6,23 g cm−3 à 20 °C.
En effet, en dépit de son éclat ou aspect métallique, ses propriétés de conduction de la chaleur et de l'électricité sont médiocres.
Il s'agit d'un semi-conducteur. L'énergie d'activation (apportée par le photon) est de l'ordre de 0,31 eV. La mobilité électronique est de l'ordre de 1 100 cm2 V−1 s−1 dans la théorie des bandes.
Son point de fusion est de l'ordre de 449,6 °C et son point d'ébullition dépasse 988 °C ou 987,85 °C. Le tellure se vaporise au rouge. Sa densité de vapeur est élevée.
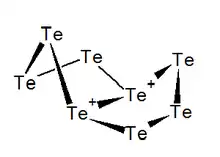
Ce corps simple cristallin, formé de longues chaînes en hélice de Ten, se caractérise par des liaisons essentiellement covalentes, il est relativement stable. Toutefois, fortement chauffé, le tellure s'enflamme à l'air en donnant principalement de l'anhydride tellureux TeO2[11]. Sa combustion dans l'air produit une flamme bleue.
Ses particules finement dispersées forment un aérosol explosif dans l'air. L'explosion peut être déclenchée par un équipement électrique défectueux ou par n'importe lequel d'un point chaud ; ses explosions de poudre, souvent secondaires, peuvent être dévastatrices.
Le tellure liquide attaque le fer, le cuivre et l'acier inoxydable, par exemple de type 10/18.
Insoluble dans l'eau et dans l'acide chlorhydrique, le tellure se dissout dans les acides oxydants, par exemple dans l'acide nitrique et dans l'eau régale, et dans les bases.
Il existe un test de détection chimique classique, en complément du test de flamme vert pâle. L'addition d'acide sulfurique concentré provoque une précipitation de sulfite de tellure rouge :
- Te solide cristal + H2SO4 aq liquide fumant concentré → TeSO3 poudre de sulfite de Te rouge + H2O
Alliage
Les associations du tellure avec les métaux et l'hydrogène sont nommées par tradition tellurures. Le corps simple forme des alliages avec le fer, l'acier et la fonte, mais aussi le cuivre et le plomb, l'or et l'argent, le cadmium et le zinc.
Le tellure graphique est un tellurure naturel d'or et d'argent.
Chimie du tellure
Le tellure présente un caractère semi-métallique affirmé, son électronégativité de l'ordre de 2,1 est plus faible que celles du S (2,5) et du Se (2,4). La réactivité du Te est moyenne par rapport à ces derniers corps simples[12].
L'anion tellurure Te2− de rayon ionique 2,21 Å est beaucoup plus volumineux que l'anion séléniure correspondant ou encore l'anion sulfure.
Le tellure réagit avec l'oxygène, il brûle à l'air pour engendrer le dioxyde de tellure, solide très peu à quasi-insoluble dans l'eau, caractérisé par un réseau ionique. Cet anhydride tellureux est attaqué par des acides oxydants. Il réagit avec les alcalis pour donner des tellurites neutres, des bitellurites et des tétratellurites.
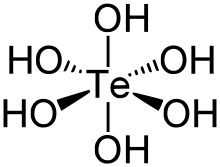
H2TeO3 n'existerait pas, mais l'ion tellurite TeO32− est observé en présence de bases fortes. Les structures analogues à l'acide sulfurique H2SO4 ou sélénique H2SeO4 n'existent pas. Mais l'acide tellurique de formule Te(OH)6, est obtenu directement l'action d'oxydants puissants sur le corps simple solide Te ou le dioxyde de tellure. Cet acide, d'ailleurs faible (pK de l'ordre de 7), se caractérise par l'ion Te6+ de très faible rayon ionique 0,56 Å au centre d'un octaèdre régulier dont les sommets sont occupés par des ions hydroxyles OH−. Le cation hexavalent représente l'état le plus excité d'un point de vue quantique, il démontre une hybridation sp3 d2. Il s'agit d'un composé covalent, assez volatil et oxydant, à l'instar de TeF6 facilement hydrolysable par l'eau.
À l'instar de l'anhydride sélénieux, l'anhydride tellureux est décomposé par l'acide sulfureux et le gaz hydrogène sulfuré. Dans le premier cas, le corps simple tellure peut être obtenu directement, mais dans le second, le chimiste obtient des sulfures de tellure, du type TeS2 et TeS3, acides vis-à-vis des sulfures alcalins.
Il se combine avec l'hydrogène ou un grand nombre de métaux pour former au sens large des « dérivés telluriques », comme le tellurure d'hydrogène H2Te, un gaz nauséabond à température ambiante, plus acide et plus instable que H2Se, peu soluble dans l'eau et toxique, ou le nombre exceptionnel de tellurures métalliques, à commencer par le tellurure de sodium Na2Te et le tellurure de potassium.
H2Te se prépare comme H2Se. Il se dissocie sous l'influence de la chaleur en magnifiques cristaux de tellure, obtenus en général en dessous du point chaud de 500 °C. Le chimiste Alfred Ditte a montré que ce gaz réactif se décomposait à l'air, tout comme les tellurures alcalins.
Il n'existe pas de polytellurures d'hydrogène stables.
Utilisation du corps simple et ses associations (alliages)
- Dans certains détonateurs, on combine le tellure avec du peroxyde de baryum.
- Semi-conducteur (de type « P ») utilisé dans les diodes laser, les cellules photovoltaïques, les détecteurs infrarouge. En semi-conducteur ternaire avec le cadmium et le mercure : Le tellurure de mercure-cadmium est utilisé comme photodétecteur (de type photodiode) de rayonnement infrarouge.
- Peut être associé au sélénium dans les imprimantes laser et photocopieurs.
- Thermocouple (Te/Pb).
- Alliage : en faible quantité dans l'acier et le cuivre, il en facilite l'usinage.
Combinaisons

Liste de tellurures :
- tellurure d'hydrogène ;
- tellurure de plomb, de bismuth, d'or, d'argent, de cobalt (CoTe et CoTe2), de mercure HgTe, etc. Ils peuvent être considérés comme des alliages.
Les tellurures désignaient autrefois les sels de l'acide tellurhydrique.
Il n'existe pas de polytellurures d'hydrogène.
Autres combinaisons avec des non-métaux :
- halogénures de tellure stables
- fluorures Te2F10, TeF4, TeF6
- chlorures TeCl2, TeCl4
- bromures TeBr2, TeBr4
- iodures TeI4
- monoxyde de Te TeO
- TeO2 insoluble dans l'eau
- TeO3
- sulfures de tellure
- TeS2 rouge à brun
- TeS3
Notes sur les principaux oxydes TeO, TeO2, TeO3, les acides et les ions correspondants.
Les tellurites et les polytellurites désignent les sels acides ou neutres obtenus après attaque des bases fortes sur l'anhydride tellureux TeO2. L'acide tellurique rarement observé s'écrirait H2TeO3 et l'ion tellurique correspond à TeO32−.
Les tellurates, très rares, désignaient les sels de l'anhydride tellurique TeO3.
Les halogénures peuvent s'hydrolyser, par exemple :
- TeF6 gaz + 6 H2O eau liquide → 6 HF + H6TeO6 poudre humide qui par fort asséchement, se décompose
- H6TeO6 → TeO3 + 3 H2O vapeur
Ils peuvent former de nombreux complexes, par exemple TeCl62− avec l'ion chlorure apporté par l'acide chlorhydrique :
- TeCl4 gaz + HCl aq → H2[TeCl6] poudre humide qui par fort asséchement, se décompose
Il est possible d'obtenir de manière similaire l'ion complexe TeBr62−.
Utilisation des composés
- Le tellure, sous forme de composé (par exemple d'oxyde de tellure), est utilisé dans certains verres de chalcogénure[13] dédiés à l'optique infrarouge.
- Vulcanisation du caoutchouc : le diéthyldithiocarbamate de tellure. Il entre sous divers composés dans la formulation des principaux procédés de vulcanisation. Te[S2CN(C2H5O)2]4 est utilisé comme catalyseur.
- Colorants en céramique
- Identification bactériologique : les Staphylococcus aureus sont capables de réduire le tellurite en sels de tellure. Voir Gélose Baird Parker.
- Les composés de tellure sont largement utilisés en chimie organique synthétique pour la réduction et l'oxydation, le cyclofonctionnement, la déshalogénation, les réactions de génération de carbanion et l'élimination des groupes protecteurs[14]. Les composés organométalliques sont des intermédiaires dans la synthèse d'amines, de diols et de produits naturels[15],[16].
- Le tellure est un constituant clé des catalyseurs à base d'oxyde mixte à haut rendement pour l'oxydation sélective du propane en acide acrylique[17],[18],[19],[20].
- Le tellure peut être utilisé dans les détecteurs d'ammoniac[21].
- Les tellures d'alkyle sont parfois utilisés dans des fongicide, algicide, parasiticide, en usage dispersif. Le tellure est alors un oligo-élément non essentiel : son rôle biochimique n'est pas complètement compris[22].
Toxicité, écotoxicité, précautions
Corps simple
L'inhalation provoque une somnolence, des maux de tête et des nausées, associés à une sécheresse de la bouche et un goût métallique. L'inhalation d'une dose infime de tellure donne une haleine et une odeur corporelle ressemblant à celle de l'ail[23].
Le contact avec l'œil se traduit par un rougissement de l'œil et des douleurs oculaires.
L'ingestion induit des douleurs abdominales, une constipation et des vomissements.
La valeur d'exposition admissible dans l'air est de 0,1 mg/m3 d'air (ACGIH 1999)[24],[25].
Corps composés
La plupart de ses composés sont toxiques, avec des atteintes au foie et au système nerveux central. Certains pays ont produit des normes spécifiques[26].
Production annuelle
La production mondiale s'élèverait entre 250 et 1 000 tonnes par an, principalement extraites, en même temps que le sélénium, des résidus de traitement du plomb et du cuivre.
Dans les années 1990, la production de tellure était contrôlée par quatre pays principaux : les États-Unis, le Canada, le Japon et le Pérou. La production annuelle, associée à celle de sélénium, était estimée de l'ordre de 1 000 tonnes, pour une valeur de 1 200 FF/t.
Les ingénieurs chimistes, à la suite d'Elias Anton Cappelen Smith, l'ont extrait des boues anodiques des minerais raffinés de cuivre.
Notes et références
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-420-09084-0)
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, « Covalent radii revisited », Dalton Transactions, , p. 2832 - 2838 (DOI 10.1039/b801115j)
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC, , 89e éd., p. 10-203
- Entrée « Tellurium » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 21 août 2018 (JavaScript nécessaire)
- (en) Thomas R. Dulski, A manual for the chemical analysis of metals, vol. 25, ASTM International, , 251 p. (ISBN 0803120664, lire en ligne), p. 71
- Base de données Chemical Abstracts interrogée via SciFinder Web le 15 décembre 2009 (résultats de la recherche)
- Il est possible d'admettre au moins, pour expliquer la dénomination relative, la boutade suédoise : « Si ce n'est pas la Terre, c'est la Lune ! ».
- (en) « Exploration diamond drilling », dans Wikipedia, (lire en ligne).
- (en) « Tellurium », sur mindat.org. Il est souvent combiné avec l'or et l'argent.
- Il était autrefois obtenu par calcination du tellurure de bismuth avec un mélange de potasse (carbonate de potassium) et de charbon actif. Le tellurure de potassium ainsi formé était dissous dans l'eau. L'absorption de l'air ou d'oxygène, lente ou accélérée par barbotage, laissait finalement de la potasse (éventuellement caustique) et du tellure pulvérisé.
- Ce dioxyde est l'analogue du dioxyde de sélénieux, ou anhydride sélénieux. Ces corps composés pourraient engendrer en principe dans l'eau ou un solvant protique les acides correspondants, H2TeO3 et H2SeO3, analogue de l'acide sélénieux H2SO3.
- Cela sert souvent de mauvaise justification à une toxicité plus faible.
- E. B. Araújo, E. Idalgo, A. P. A. Moraes et A. G. Souza Filho, « Crystallization kinetics and thermal properties of 20Li2O–80TeO2 glass », Materials Research Bulletin, vol. 44, no 7, , p. 1596–1600 (DOI 10.1016/j.materresbull.2009.01.019, lire en ligne, consulté le ).
- Nicola Petragnani et Lo Wai-Ling, « Organometallic Reagents for Synthetic Purposes: Tellurium », Journal of the Brazilian Chemical Society, vol. 9, no 5, , p. 415–425 (ISSN 0103-5053, DOI 10.1590/S0103-50531998000500002, lire en ligne, consulté le ).
- Fabricio Vargas, Fabiano T. Toledo et João V. Comasseto, « N-Functionalized organolithium compounds via tellurium/lithium exchange reaction », Journal of the Brazilian Chemical Society, vol. 21, no 11, , p. 2072–2078 (ISSN 0103-5053, DOI 10.1590/S0103-50532010001100007, lire en ligne, consulté le ).
- Renan S. Ferrarini, Jefferson L. Princival, João V. Comasseto et Dos Santos, « A concise enantioselective synthesis of (+)-endo-brevicomin accomplished by a tellurium/metal exchange reaction », Journal of the Brazilian Chemical Society, vol. 19, no 5, , p. 811–812 (ISSN 0103-5053, DOI 10.1590/S0103-50532008000500002, lire en ligne, consulté le ).
- Kinetic studies of propane oxidation on Mo and V based mixed oxide catalysts, (lire en ligne).
- (en) « Surface chemistry of phase-pure M1 MoVTeNb oxide during operation in selective oxidation of propane to acrylic acid », Journal of Catalysis, , p. 48-60 (DOI 10.1016/j.jcat.2011.09.012, lire en ligne).
- (en) « Multifunctionality of Crystalline MoV(TeNb) M1 Oxide Catalysts in Selective Oxidation of Propane and Benzyl Alcohol », ACS Catalysis, vol. 3, no 6, , p. 1103-1113 (DOI 10.1021/cs400010q, lire en ligne).
- (en) « The reaction network in propane oxidation over phase-pure MoVTeNb M1 oxide catalysts », Journal of Catalysis, , p. 369-385 (DOI 10.1016/j.jcat.2013.12.008, lire en ligne).
- M. Bianchetti, E. Heredia, C. Oviedo et N. Walsöe de Reca, « A thin film sensor to detect ammonia at room temperature in humid media », Anales de la Asociación Química Argentina, vol. 93, nos 1-3, , p. 27–34 (ISSN 0365-0375, lire en ligne, consulté le ).
- Rodrigo L. O. R. Cunha, Iuri E. Gouvea et Luiz Juliano, « A glimpse on biological activities of tellurium compounds », Anais da Academia Brasileira de Ciências, vol. 81, no 3, , p. 393–407 (ISSN 0001-3765, DOI 10.1590/S0001-37652009000300006, lire en ligne, consulté le ).
- Conseil national de recherche du Canada.
- Fiche NIOSH de sécurité
- Fiche IRSST (consultée le 7 novembre 2008).
- Exemples de normes pour la Belgique
Voir aussi
Bibliographie
- Alain Foucault, Jean-François Raoult, Fabrizio Cecca et Bernard Platevoet, Dictionnaire de Géologie, 8e éd., français/anglais, édition Dunod, 2014, 416 p. Avec la simple entrée « tellure » p. 348.
- Bruce H. Mahan, Chimie, InterEdition, Paris, 1977, 832 p. (Traduction de University Chemistry, 2e éd., Addison-Wesley Publishing Company, Massachusetts, 1969 (ISBN 978-2-7296-0065-5)), en particulier p. 631 et p. 640-41.
- Paul Pascal, Nouveau traité de chimie minérale, Paris, Masson, (réimpr. 1966), 32 vol.
« 13.1 & 13.2 Oxygène, azote, oxydes, eau oxygénée, la combustion, soufre, sélénium, tellure, polonium »
Articles connexes
- Calavérite
- Cellule thermophotovoltaïque, usage du Te pour le dopage des cellules en GaSb
- Chalcogène
- Chalcogénure
- Chalcophile
- Dioxyde de tellure
- Éléments de la période 5
- Groupe fonctionnel (groupe du Te)
- Isotopes du tellure
- Nagyagite
- Petzite
- Processus rp
- Quetzalcoatlite
- Radioconducteur
- Récepteur à cristal, en particulier son usage dans le détecteur à galène
- Rickardite
- Rodalquilarite
- Sylvanite
- TAGS
- Telluro- préfixe
- Tellurophène, un métallole
- Tellure natif
- Tellurures
- Tellurure d'antimoine
- Tellurure d'argent
- Tellurure de bismuth(III)
- Tellurure de cadmium
- Tellurure de germanium
- Tellurure d'hydrogène
- Tellurure de mercure-cadmium, fabriqué en France par Sofradir
- Tellurure de plomb(II)
- Tellurure de sodium
- Tétradymite
- Verre de chalcogénure
- Zemannite
Liens externes
- Présentation du radionucléide 123, avec introduction de la chimie du tellure
- BRGM, Panorama 2010 du marché du tellure, septembre 2011
- (en) Fiche internationale de sécurité chimique traduite par l'Institut Scientifique de Santé Publique (Belgique)
- (en) Te Présentation de l'élément et propriétés du corps simple
- (en) « Technical data for Tellurium » (consulté le ), avec en sous-pages les données connues pour chaque isotope
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
| Métaux Alcalins |
Alcalino- terreux |
Lanthanides | Métaux de transition |
Métaux pauvres |
Métal- loïdes |
Non- métaux |
Halo- gènes |
Gaz nobles |
Éléments non classés |
| Actinides | |||||||||
| Superactinides | |||||||||
- Portail de la physique
- Portail de la chimie