دورة تحريك حراري
دورة التحريك الحراري أو الدورة الترموديناميكية في الفيزياء والكيمياء والهندسة هي دورة مكونة من عدة تغيرات للحالة لوسط شغل (كالبخار، أو الماء أو غاز) وتسير دوريا بحيث تعود بعد كل دورة إلى الحالة الابتدائية التي تتصف ب ضغط معين ودرجة حرارة معينة وكثافة معينة. (توصف تلك الحالات وغيرها من صفات نظام بأنها دوال الحالة). الدورة الترموديناميكية هي عملية تقنية تتحول خلالها الحرارة إلى شغل مثل محرك احتراق داخلي أو جهاز تدفئة أو ثلاجة.
| الديناميكا الحرارية |
| فروع الديناميكا الحرارية |
| ترموديناميكا الغلاف الجوي | ترموديناميكا بيولوجية | ترموديناميك الثقب الأسود | ترموديناميك كيميائي | ترموديناميك كلاسيكي | توازن ترموديناميكي | ترموديناميك اللاتوازن | ترموديناميك الظاهراتي | ديناميكا لونية كمية | ترموديناميكا إحصائية |
| قوانين الديناميكا الحرارية |
| القانون الصفري | القانون الأول | القانون الثاني | القانون الثالث |
| العمليات الديناميكية الحرارية |
| عملية متساوية الضغط | عملية متساوية الحرارة | عملية كظومة (أديباتية) | عملية متساوية الأنتالبية |
| مصطلحات |
| نظام دينامي حراري | حالة نظام ديناميكي | نظام مغلق | نظام مفتوح | نظام معزول | دورة حركة حرارية| دورة كارنو | دورة أوتو |دورة ديزل |دورة رانكن |تفاضل تام |
| خواص ترموديناميكية للسوائل |
|
يتحكم القانون الأول للديناميكا الحرارية في الدورة وينص على أن: "صافي الحرارة الداخلة في النظام تساوي صافي الشغل المؤدى من النظام". وطبيعة تتابع مسيرة العمليات تعمل على تكرار الدورة مما يجعل الدورة فكرة أساسية في الحركة الحرارية.
الحرارة والشغل
كانت أول آلات دورة الحركة الحرارية هي «دورة القدرة»، مثل دورة محرك بخاري أو محرك الاحتراق الداخلي ودورة الطلمبة الحرارية. ففي دورة القدرة تتحول الحرارة إلى شغل ميكانيكي، بينما في دورة الطلمبة الحرارية فهي تنقل الحرارة من درجة حرارة منخفضة إلى درجة حرارة عالية عن طريق إمدادها بشغل. وتتكون الدورات عموما من عمليات شبه مستقرة (لا تتغير مع الزمن، بل تعود كل منها إلى حالتها الأولى خلال الدورات المتعاقبة)، وبذلك يمكن أن تشتغل كدورة قدرة (إنتاج شغل ميكانيكي) أو كطلمبة حرارية (تحول الشغل إلى حرارة) عن طريق التحكم في اتجاه العملية.
تمثل الدورة برسوم بيانية منها نوع يبين العلاقة بين تغير الحجم وتغير الضغط ويسمى مخطط الضغط والحجم ونوع آخر يبين العلاقة بين تغير درجة الحرارة والإنتروبية ويسمى مخطط درجة الحرارة والإنتروبي، وفيها يبين اتجاه عمل الدورة عما إذا كانت دورة قدرة (في اتجاه عقرب الساعة) أو تعمل الدورة كطلمبة حرارية (في عكس اتجاه عقرب الساعة).
علاقتها بالشغل
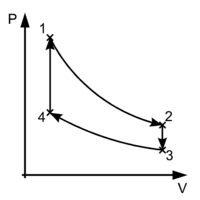
ونظرا لأن التغير الكلي في حالات الدورة خلال الدورة الترموديناميكية يكون مساويا للصفر، فهي تشكل دورة في شكل الضغط والحجم. في شكل الضغط والحجم يبين المحور Y الضغط (P) والمحور X يبين الحجم (V). وتعين المساحة المحصورة في الدورة مقدار الشغل (W) الناتج من الدورة:
هذا الشغل يكون مساويا للحرارة Q المعطاة إلى النظام:
تماثل المعادلة 2 دورة عملية متساوية درجة الحرارة: ومع أن الطاقة الداخلية في النظام تتغير أثناء عمليات الدورة إلا أنه عند انتهاء الدورة تكون الطاقة الداخلية للنظام هي نفسها عن بدء العملية.
إذا سارت الدورة في اتجاه عقرب الساعة يكون الشغل W موجب الإشارة، وهي تمثل آلة حرارية. وإذا سارت الدورة بعكس اتجاه عقرب الساعة، يكون الشغل W سالب الإشارة، وتمثل الدورة عندئذ طلمبة حرارية.
الطلمبة الحرارية: نبدأ عند النقطة 4 ونزيد الحجم (نؤدي شغلا) حتى النقطة 3 مع المحافظة على درجة حرارة ثابتة. عند 3 نثبت الحجم ونبدأ في رفع الضغط (نؤدي شغلا) حتى النقطة 2، فيعمل الضغط على زيادة حرارة الغاز. من النقطة 2 نكبس الحجم (نؤدي شغلا) فيزداد الضغط وتزداد درجة حرارة الغاز حتى نصل إلى النقطة 1. عند النقطة 1 نقلل الضغط مع ثبات الحجم (نؤدي شغلا). أي أن «الطلمبة الحرارية» تحول الشغل الميكانيكي إلى حرارة.
دورة القدرة

دورة القدرة هي أساس عمل الآلة الحرارية التي تمد معظم العالم ب الطاقة الكهربائية وتشغل معظم السيارات والعربات ذات محرك. ويمكن تصنيف دورات القدرة بحسب نوع المحرك الذي يعمل، وأكثر المحركات استهداما هو محرك الاحتراق الداخلي ودورته تسمى أوتو سيكل، وعلى نمطها يعمل محرك الجازولين ومحرك الديزل. ومن المحركات التي تمثل آلات الاحتراق الخارجي نعرف مثلا توربين الغاز ودورة رانكن التي تمثل توربين بخاري.

وعلى سبيل المثال، الشغل الميكانيكي المؤدي بواسطة تغيرات الضغط والحجم طبقا لدورة آلة حرارية تشتمل على 4 عمليات ترموديناميكية (قارن الشكل):
حيث:
وإذا لم يحدث تغير في الحجم في العمليتين 4->1 و2->3, تتبسط المعادلة (3) إلى الآتي:
دورات طلمبة حرارية
تمثل دورات المضخة الحرارية المضخة الحرارية والثلاجة. والفرق بينهما هو أن المضخة الحرارة تعمل على رفع درجة حرارة المكان المراد تسخينه بينما تعمل الثلاجة أو أي جهاز تبريد على تبريد مكان نريد خفض درجة حرارته.
وتتكون دورة التبريد من دورة ضغط بخار والتي تتمثل في ثلاجة وتعمل بواسطة وسط تبريد يغير أطواره بين الحالة السائلة والحالة الغازية. ويتم التبريد فيها عن طريق تبخير السائل. ويمكن عن طريق تبريد الغاز إلى تسييل الغاز، كما في الغاز النفطي المسال.
نماذج لآلات عملية
 أمثلة لأنظمة حقيقية ممثلة بعملية مثالية: مخطط الضغط والحجم PV diagram، ومخطط درجة الحرارة والإنتروبي TS diagram لدورة برايتون، كنماذج لعمليات حقيقية للتوربين الغازي. |
تستخدم دورة الحركة الحرارية لتمثيل جهاز حقيقي، وعادة تحدد لها مبدئيا بعض الافتراضات.[1] ويساعد تبسيط الافتراضات على تقليل مشاكل الضبط والتحكم، فتسهل بالتالي التحكم في سير العملية.[1] وعلى سبيل المثال كما هو مبين في الشكل، نجد أن التوربين الغازي أو محرك نفاث يمكن تمثيلهما بواسطة دورة برايتون. ويتكون المحرك من عدة مراحل، وتمثل كل منها على حدة كعملية ترموديناميكية مثالية. وعلى الرغم من أن كل مرحلة نجريها على وسط الشغل قد يكون جهازا معقدا في حقيقة امره ولكن تمثيله كعمليات مثالية تقربنا بالفعل إلى سلوكها الحقيقي. وافتراض آخر يتعلق بالغاز العادم الذي قد نعيده إلى المدخل رغم فقدانه جزءا من حرارته، فيعتبر هذا أيضا نوعا من المثالية في آداء الدورة.
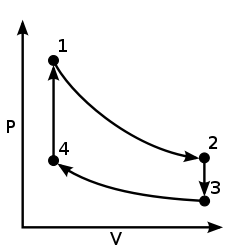
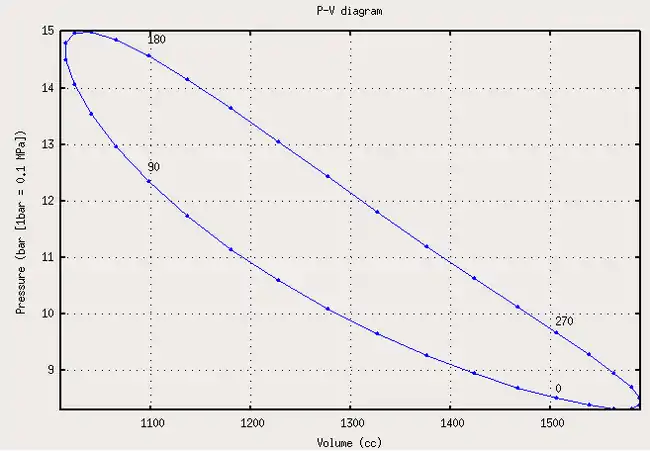
والفرق بين دورة مثالية ودوره حقيقية قد يكون كبيرا، وعلى سبيل المثال توضح الأشكال التالية الفرق بين الشغل الناتج المحسوب لدورة ستيرلينغ والأداء الحقيقي لآلة ستيرلينغ:[1]
 |
 |
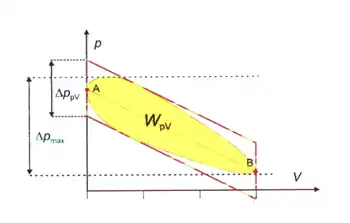 |
| دورة ستيرلينج مثالية | الأداء المعتاد | الشغل المثالي (أحمر)والمعتاد (أصفر) ويتبين الفرق بينهما |
الشغل الناتج هو المساحة داخل الدورة، ومنها يظهر الفرق الكبير بين الشغل الناتج المحسوب بواسطة الدورة المثالية والشغل الفعلي الناتج من آلة حقيقية. كما نلاحظ أن العمليات المنفردة الحقيقية تختلف عن نظيراتها المثالية، مثلما في حالة التمدد في حجم ثابت (العملية 1 - 2) حيث تتم العملية واقعيا مع قدر من زيادة في الحجم.
انظر أيضا
مراجع
- Cengel, Yunus A.; Boles, Michael A. (2002). Thermodynamics: an engineering approach. Boston: McGraw-Hill. pp. 452. ISBN 0-07-238332-1.
- بوابة هندسة ميكانيكية
- بوابة الكيمياء
- بوابة كيمياء فيزيائية
- بوابة الفيزياء